Asthma-Behandlung: Combivent 50/20mcg Levosalbutamol Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalation Aerosol
Bronchodilatator-Aerosol Nur zur oralen Inhalation
BEZEICHNUNG
COMBIVENT Aerosol zur Inhalation ist eine Kombination aus Ipratropiumbromid (als Monohydrat) und Albuterolsulfat.
Ipratropiumbromid ist ein anticholinerger Bronchodilatator, chemisch beschrieben als 8-Azoniabicyclo[3.2.1]octan, 3-(3-Hydroxy-1-oxo-2-phenylpropoxy)-8-methyl8-(1-methylethyl)-, Bromidmonohydrat, ( 3-endo, 8-syn)-: eine synthetische quaternäre Ammoniumverbindung, die chemisch mit Atropin verwandt ist. Ipratropiumbromid ist eine weiße bis cremefarbene kristalline Substanz, gut löslich in Wasser und Methanol, schwer löslich in Ethanol und unlöslich in lipophilen Lösungsmitteln wie Ether, Chloroform und Fluorkohlenwasserstoffen.
Die Strukturformel lautet:
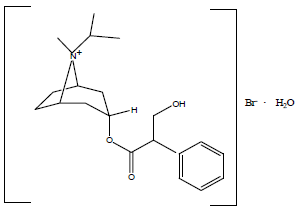 C20H30BrNO3·H2O Ipratropiumbromid Mol. Gew. 430.4
C20H30BrNO3·H2O Ipratropiumbromid Mol. Gew. 430.4
Albuterolsulfat, chemisch bekannt als (1,3-Benzoldimethanol, α'-[[(1,1dimethylethyl)amino]methyl]-4-hydroxysulfat (2:1)(Salz), (±)- ist relativ selektiv beta2-adrenerger Bronchodilatator. Albuterol ist der offizielle generische Name in den Vereinigten Staaten. Der von der Weltgesundheitsorganisation empfohlene Name für das Medikament ist Salbutamol. Albuterolsulfat ist ein weißes bis cremefarbenes kristallines Pulver, das in Wasser leicht löslich und in Alkohol leicht löslich ist. Chloroform und Ether.Die Strukturformel ist:
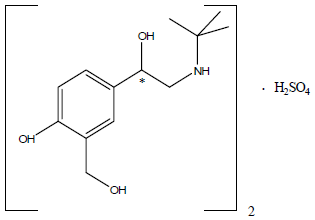 (C13H21NO3)2•H2SO4 Albuterolsulfat Mol. Gew. 576.7
(C13H21NO3)2•H2SO4 Albuterolsulfat Mol. Gew. 576.7
Combivent® (Ipratropiumbromid und Albuterolsulfat) Aerosol zur Inhalation enthält eine mikrokristalline Suspension von Ipratropiumbromid und Albuterolsulfat in einer unter Druck stehenden Dosieraerosoleinheit zur oralen Inhalation. Das 200er Inhalationsgerät hat ein Nettogewicht von 14,7 Gramm. Bei jedem Sprühstoß werden 21 µg Ipratropiumbromid und 120 µg Albuterolsulfat aus dem Ventil dosiert und 18 µg Ipratropiumbromid und 103 µg Albuterolsulfat (entspricht 90 µg Albuterolbase) aus dem Mundstück abgegeben. Die Hilfsstoffe sind Dichlordifluormethan, Dichlortetrafluorethan und Trichlormonofluormethan als Treibmittel und Sojalecithin.
INDIKATIONEN
COMBIVENT Aerosol zur Inhalation ist indiziert zur Anwendung bei Patienten mit chronisch obstruktiver Lungenerkrankung (COPD), die regelmäßig einen Aerosol-Bronchodilatator erhalten, weiterhin Anzeichen von Bronchospasmen haben und einen zweiten Bronchodilatator benötigen.
DOSIERUNG UND ANWENDUNG
Die Dosis von COMBIVENT® Inhalationsaerosol beträgt zwei Inhalationen viermal täglich. Die Patienten können nach Bedarf zusätzliche Inhalationen durchführen; Die Gesamtzahl der Inhalationen sollte jedoch 12 in 24 Stunden nicht überschreiten. Die Sicherheit und Wirksamkeit zusätzlicher Dosen von COMBIVENT Inhalationsaerosol über 12 Sprühstöße/24 Stunden hinaus wurde nicht untersucht. Auch die Sicherheit und Wirksamkeit von zusätzlichen Dosen von Ipratropium oder Albuterol zusätzlich zu den empfohlenen Dosen von Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol wurden nicht untersucht. Es wird empfohlen, vor der ersten Anwendung und in Fällen, in denen das Aerosol länger als 24 Stunden nicht verwendet wurde, dreimal „Probesprühen“ durchzuführen. Nicht in die Augen sprühen.
WIE GELIEFERT
COMBIVENT Inhalationsaerosol wird als Dosierinhalator mit einem weißen Mundstück geliefert, das eine durchsichtige, farblose Hülle und eine orangefarbene Schutzkappe hat. Der COMBIVENT 20-mcg-Inhalationsaerosolbehälter darf nur mit dem COMBIVENT 20-mcg-Inhalationsaerosol-Mundstück und nicht mit anderen Mundstücken verwendet werden. Dieses Mundstück sollte nicht mit anderen Aerosol-Medikamenten verwendet werden. Bei jedem Sprühstoß werden 21 µg Ipratropiumbromid und 120 µg Albuterolsulfat aus dem Ventil dosiert und 18 µg Ipratropiumbromid und 103 µg Albuterolsulfat (entspricht 90 µg Albuterolbase) aus dem Mundstück abgegeben.
Jeder 14,7-Gramm-Kanister enthält ausreichend Medikament für 200 Sprühstöße ( NDC 0597-001314).
Warnung: Der Kanister sollte entsorgt werden, nachdem die angegebene Anzahl von Sprühstößen verwendet wurde. Die korrekte Menge des Medikaments bei jedem Sprühstoß kann nach diesem Zeitpunkt nicht mehr gewährleistet werden, auch wenn der Kanister nicht vollständig leer ist.
Bei 25 °C (77 °F) lagern; Exkursionen erlaubt bis 15°-30°C (59°-86°F) [sehen USP kontrollierte Raumtemperatur ]. Für beste Ergebnisse den Kanister vor Gebrauch bei Raumtemperatur lagern. Vermeiden Sie übermäßige Feuchtigkeit. Kanister vor Gebrauch mindestens 10 Sekunden kräftig schütteln.
Richten Sie medizinische Anfragen an: http://us.boehringer-ingelheim.com, (800) 542-6257 oder (800) 459-9906 TTY.
Notiz: Die folgende eingerückte Erklärung wird vom Luftreinhaltegesetz der Bundesregierung für alle Produkte verlangt, die Fluorchlorkohlenwasserstoffe (FCKW) enthalten oder daraus hergestellt werden:
Warnung: Enthält Trichlormonofluormethan (CFC-11), Dichlordifluormethan (CFC-12) und Dichlortetrafluorethan (CFC-114), Substanzen, die die öffentliche Gesundheit und die Umwelt schädigen, indem sie das Ozon in der oberen Atmosphäre zerstören.
Ein ähnlicher Hinweis wie oben Warnung wurde in die Patienteninformationen dieses Produkts gemäß den Vorschriften der Environmental Protection Agency (EPA) aufgenommen. Die Warnung des Patienten besagt, dass der Patient seinen Arzt konsultieren sollte, wenn es Fragen zu Alternativen gibt.
Inhalt unter Druck: Nicht durchstechen. Nicht in der Nähe von Hitze oder offenem Feuer verwenden oder lagern. Temperaturen über 120 °F können zum Platzen führen. Werfen Sie den Inhalator niemals in ein Feuer oder eine Verbrennungsanlage.
Vertrieb durch: Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 USA. Ipratropiumbromid lizenziert von: Boehringer Ingelheim International GmbH. Überarbeitet: August 2012
NEBENWIRKUNGEN
Informationen zu Nebenwirkungen von Combivent® (Ipratropiumbromid und Albuterolsulfat) Aerosol zur Inhalation stammen aus zwei 12-wöchigen kontrollierten klinischen Studien (N = 358 für COMBIVENT Aerosol zur Inhalation), wie in Tabelle 1 dargestellt.
Zusätzliche Nebenwirkungen, die bei weniger als zwei Prozent der Patienten in der COMBIVENT-Inhalationsaerosol-Behandlungsgruppe berichtet wurden, umfassen Ödeme, Müdigkeit, Bluthochdruck, Schwindel, Nervosität, Parästhesien, Tremor, Dysphonie, Schlaflosigkeit, Durchfall, Mundtrockenheit, Dyspepsie, Erbrechen, Arrhythmie, Herzklopfen, Tachykardie, Arthralgie, Angina pectoris, vermehrter Auswurf, Geschmacksstörungen und Harnwegsinfektion/Dysurie.
Allergische Reaktionen wie Hautreaktionen einschließlich Hautausschlag, Pruritus und Urtikaria (einschließlich Riesenurtikaria), Angioödeme einschließlich Zunge, Lippen und Gesicht, Laryngospasmus und anaphylaktische Reaktionen wurden im Zusammenhang mit Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol berichtet , in einigen Fällen mit positiver Rechallenge. Viele dieser Patienten hatten in der Vorgeschichte Allergien gegen andere Arzneimittel und/oder Lebensmittel, einschließlich Sojabohnen (siehe KONTRAINDIKATIONEN ).
Post-Marketing-Erfahrung
In einer 5-jährigen placebokontrollierten Studie kam es bei COPD-Patienten, die Atrovent® (Ipratropiumbromid) Inhalationsaerosol CFC erhielten, zu Krankenhauseinweisungen wegen supraventrikulärer Tachykardie und/oder Vorhofflimmern mit einer Inzidenzrate von 0,5 %.
Weitere Nebenwirkungen, die aus der veröffentlichten Literatur und/oder Beobachtungen nach Markteinführung bei der Anwendung von Ipratropiumbromid-haltigen Produkten (einzeln oder in Kombination mit Albuterol) identifiziert wurden, umfassen: Überempfindlichkeit, Pharynxödem, Mundödem, Harnverhalt, Mydriasis, Bronchospasmus ( einschließlich paradoxem Bronchospasmus), Fälle von Präzipitation oder Verschlechterung eines Engwinkelglaukoms, Glaukom, erhöhter Augeninnendruck, akuter Augenschmerz, Halosehen, verschwommenes Sehen, Akkommodationsstörung, Augenreizung, Hornhautödem, Bindehauthyperämie, verstopfte Nase, Austrocknen von Sekreten , Schleimhautgeschwüre, Stomatitis, Reizung durch Aerosol, Rachenreizung, trockener Rachen, Keuchen, Verschlimmerung von COPD-Symptomen, Heiserkeit, Herzklopfen, Sodbrennen, Benommenheit, ZNS-Stimulation, Koordinationsschwierigkeiten, Hitzewallungen, Alopezie, Hypotonie, Ödeme, Magen-Darm-Beschwerden (Durchfall, Übelkeit, Erbrechen), gastrointestinale Motilitätsstörung, Verstopfung, Hypokaliämie, psychische Störung, Hyperhidrose, Muskelkrämpfe, Muskelschwäche, Myalgie, Asthenie, myokardiale Ischämie, verminderter diastolischer Blutdruck und erhöhter systolischer Blutdruck.
Bei der Anwendung von Albuterol-haltigen Produkten wurde über metabolische Azidose berichtet.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
COMBIVENT Inhalationsaerosol wurde gleichzeitig mit anderen Arzneimitteln angewendet, darunter sympathomimetische Bronchodilatatoren, Methylxanthine und orale und inhalative Steroide, die üblicherweise zur Behandlung von chronisch obstruktiven Lungenerkrankungen eingesetzt werden. Mit Ausnahme von Albuterol gibt es keine formalen Studien, die die Interaktionseffekte von COMBIVENT Inhalationsaerosol und diesen Arzneimitteln in Bezug auf Sicherheit und Wirksamkeit vollständig bewerten.
Anticholinergika
Es besteht die Möglichkeit einer additiven Wechselwirkung mit gleichzeitig angewendeten Anticholinergika. Vermeiden Sie daher die gleichzeitige Anwendung von COMBIVENT 50 mg Aerosol zur Inhalation mit anderen Arzneimitteln, die Anticholinergika enthalten.
Beta-adrenerge Wirkstoffe
Bei gleichzeitiger Anwendung von COMBIVENT Inhalation Aerosol und anderen Sympathomimetika ist aufgrund des erhöhten Risikos von unerwünschten kardiovaskulären Wirkungen Vorsicht geboten.
Betarezeptorenblocker und Albuterol hemmen die Wirkung voneinander. Betarezeptorenblocker sollten bei Patienten mit hyperreaktiven Atemwegen mit Vorsicht angewendet werden.
Diuretika
Die EKG-Veränderungen und/oder Hypokaliämie, die aus der Verabreichung von nicht kaliumsparenden Diuretika (wie Schleifen- oder Thiaziddiuretika) resultieren können, können durch Beta-Agonisten akut verschlechtert werden, insbesondere wenn die empfohlene Dosis des Beta-Agonisten überschritten wird. Obwohl die klinische Bedeutung dieser Wirkungen nicht bekannt ist, ist bei der gleichzeitigen Anwendung von Arzneimitteln, die Beta-Agonisten enthalten, wie z. B. COMBIVENT Inhalationsaerosol, mit nicht kaliumsparenden Diuretika Vorsicht geboten. Erwägen Sie die Überwachung des Kaliumspiegels.
Monoaminoxidase-Hemmer oder trizyklische Antidepressiva
COMBIVENT Inhalationsaerosol sollte bei Patienten, die mit Monoaminoxidase-Hemmern oder trizyklischen Antidepressiva behandelt werden, mit äußerster Vorsicht oder innerhalb von zwei Wochen nach Absetzen solcher Mittel verabreicht werden, da die Wirkung von Albuterol auf das Herz-Kreislauf-System verstärkt werden kann. Erwägen Sie eine alternative Therapie bei Patienten, die MAOs oder trizyklische Antidepressiva einnehmen.
WARNUNGEN
VORSICHTSMASSNAHMEN
Allgemein
Informationen für Patienten
Die Patienten sollten davor gewarnt werden, das Aerosol in ihre Augen zu sprühen, und darauf hingewiesen werden, dass dies zu Präzipitation oder Verschlechterung eines Engwinkelglaukoms, Mydriasis, erhöhtem Augeninnendruck, akuten Augenschmerzen oder -beschwerden, vorübergehendem verschwommenem Sehen, visuellen Halos oder Verfärbungen führen kann Bilder in Verbindung mit roten Augen aufgrund von Bindehaut- und Hornhautverstopfung. Die Patienten sollten auch darauf hingewiesen werden, dass sie sofort ihren Arzt aufsuchen sollten, wenn eine Kombination dieser Symptome auftritt.
Die Wirkung von COMBIVENT 20 µg Inhalationsaerosol sollte 4 bis 5 Stunden oder länger anhalten. COMBIVENT Inhalationsaerosol sollte nicht häufiger als empfohlen angewendet werden. Erhöhen Sie die Dosis oder Häufigkeit von COMBIVENT Inhalationsaerosol nicht ohne Rücksprache mit Ihrem Arzt. Wenn Sie feststellen, dass die Behandlung mit COMBIVENT 20 µg Aerosol zur Inhalation zur Linderung der Symptome nachlässt, Ihre Symptome sich verschlimmern und/oder Sie das Produkt häufiger als gewöhnlich anwenden müssen, sollten Sie sofort einen Arzt aufsuchen. Während Sie COMBIVENT Inhalationsaerosol einnehmen, sollten andere inhalative Arzneimittel nur nach Anweisung Ihres Arztes eingenommen werden. Wenn Sie schwanger sind oder stillen, wenden Sie sich bezüglich der Anwendung von COMBIVENT Inhalation Aerosol an Ihren Arzt. Zur sachgemäßen Anwendung von Combivent® (Ipratropiumbromid und Albuterolsulfat) Aerosol zur Inhalation gehört das Verständnis der Art und Weise, wie es verabreicht werden sollte (siehe Gebrauchsanweisung des Patienten ).
Da bei der Anwendung von COMBIVENT 20 mcg Schwindel, Akkommodationsstörungen, Mydriasis und verschwommenes Sehen auftreten können, sollten Patienten davor gewarnt werden, Aktivitäten nachzugehen, die Gleichgewicht und Sehschärfe erfordern, wie Autofahren oder Bedienen von Geräten oder Maschinen.
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Ipratropiumbromid
Zweijährige orale Karzinogenitätsstudien an Ratten und Mäusen haben bei Dosen bis zu 6 mg/kg keine karzinogene Wirkung gezeigt. Diese Dosis entspricht bei Ratten und Mäusen etwa dem 230- bzw. 110-Fachen der maximal empfohlenen täglichen Inhalationsdosis von Ipratropiumbromid bei Erwachsenen auf mg/m²-Basis. Die Ergebnisse verschiedener Mutagenitätsstudien (Ames-Test, Maus-Dominant-Letal-Test, Maus-Mikronukleus-Test und Chromosomenaberration des Knochenmarks bei chinesischen Hamstern) waren negativ.
Die Fertilität männlicher oder weiblicher Ratten bei oralen Dosen von bis zu 50 mg/kg (etwa das 1900-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) wurde durch die Verabreichung von Ipratropiumbromid nicht beeinflusst. Bei einer oralen Dosis von 500 mg/kg (etwa das 19.000-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) führte Ipratropiumbromid zu einer Abnahme der Empfängnisrate.
Alberol
Wie andere Wirkstoffe seiner Klasse verursachte Albuterol in einer 2-Jahres-Studie an Ratten bei Futterdosen von 2, 10 und 50 mg/kg (ca. 65- und 330-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis). In einer anderen Studie wurde dieser Effekt durch die gleichzeitige Gabe von Propranolol blockiert. Die Relevanz dieser Befunde für den Menschen ist nicht bekannt. Eine 18-monatige Studie an Mäusen mit Nahrungsdosen von bis zu 500 mg/kg (ungefähr das 1600-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) und eine 99-wöchige Studie an Hamstern mit oralen Dosen von bis zu 50 mg /kg (ungefähr das 220-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) ergab keinen Hinweis auf eine tumorerzeugende Wirkung. Studien mit Albuterol ergaben keine Hinweise auf Mutagenese.
Reproduktionsstudien an Ratten mit Albuterolsulfat ergaben keine Hinweise auf eine Beeinträchtigung der Fertilität.
Schwangerschaft
COMBIVENT Inhalationsaerosol
Teratogene Wirkungen: Schwangerschaftskategorie C
Es liegen keine angemessenen und gut kontrollierten Studien mit Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol, Ipratropiumbromid oder Albuterolsulfat bei Schwangeren vor. Reproduktionsstudien an Tieren wurden mit COMBIVENT Inhalationsaerosol nicht durchgeführt. Albuterolsulfat hat sich jedoch bei Mäusen und Kaninchen als teratogen erwiesen. COMBIVENT Inhalationsaerosol sollte während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.
Ipratropiumbromid
Teratogene Wirkungen
Orale Reproduktionsstudien wurden mit Dosen von 10 mg/kg bei Mäusen, 1000 mg/kg bei Ratten und 125 mg/kg bei Kaninchen durchgeführt. Diese Dosen entsprechen bei jeder Spezies etwa dem 190-, 38.000- bzw. 9400-fachen der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis. Inhalative Reproduktionsstudien wurden an Ratten und Kaninchen mit Dosen von 1,5 und 1,8 mg/kg (ungefähr das 55- und 140-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) durchgeführt. Diese Studien ergaben keine Hinweise auf teratogene Wirkungen infolge von Ipratropiumbromid. Bei oralen Dosen von 90 mg/kg und mehr bei Ratten (ungefähr das 3.400-Fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) wurde Embryotoxizität in Form einer erhöhten Resorption beobachtet. Dieser Effekt wird aufgrund der hohen Dosen, bei denen er beobachtet wurde, und der unterschiedlichen Verabreichungswege als nicht relevant für die Anwendung beim Menschen angesehen.
Alberol
Teratogene Wirkungen
Albuterol hat sich bei Mäusen und Kaninchen als teratogen erwiesen. Eine Reproduktionsstudie an CD-1-Mäusen, denen Albuterol subkutan (0,025, 0,25 und 2,5 mg/kg) verabreicht wurde, zeigte eine Gaumenspaltenbildung bei 5 von 111 (4,5 %) Föten bei 0,25 mg/kg (entsprechend der maximal empfohlenen täglichen Inhalationsdosis in Erwachsene auf mg/m²-Basis) und bei 10 von 108 (9,3 %) Föten mit 2,5 mg/kg (ungefähr das Achtfache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis). Bei 0,025 mg/kg (weniger als die maximal empfohlene tägliche Inhalationsdosis bei Erwachsenen) wurde keine beobachtet. Gaumenspalten traten auch bei 22 von 72 (30,5 %) Feten auf, die mit 2,5 mg/kg Isoproterenol behandelt wurden (positive Kontrolle). Eine Reproduktionsstudie mit oralem Albuterol bei holländischen Stride-Kaninchen ergab bei 7 von 19 (37 %) Föten bei 50 mg/kg (ungefähr das 660-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis) eine Cranioschisis.
Arbeit und Lieferung
Aufgrund der möglichen Beeinträchtigung der Uteruskontraktilität durch Beta-Agonisten sollte die Anwendung von Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol zur Behandlung von COPD während der Wehen auf Patientinnen beschränkt werden, bei denen der Nutzen das Risiko eindeutig überwiegt.
Stillende Mutter
Es ist nicht bekannt, ob die Bestandteile von COMBIVENT Inhalationsaerosol in die Muttermilch übergehen.
Ipratropiumbromid
Da fettunlösliche quartäre Kationen in die Muttermilch übergehen, ist Vorsicht geboten, wenn COMBIVENT Inhalationsaerosol einer stillenden Mutter verabreicht wird.
Alberol
Aufgrund des in Tierversuchen für Albuterol nachgewiesenen tumorerzeugenden Potenzials sollte unter Berücksichtigung der Bedeutung des Arzneimittels für die Mutter eine Entscheidung getroffen werden, ob das Stillen beendet oder das Arzneimittel abgesetzt werden soll.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit bei Kindern und Jugendlichen wurden nicht nachgewiesen.
ÜBERDOSIS
Es wird erwartet, dass die Auswirkungen einer Überdosierung hauptsächlich auf Albuterolsulfat zurückzuführen sind. Eine akute Überdosierung mit Ipratropiumbromid durch Inhalation ist unwahrscheinlich, da Ipratropiumbromid systemisch nach Aerosol- oder oraler Verabreichung nicht gut resorbiert wird. Orale mediane letale Dosen von Ipratropiumbromid lagen bei Mäusen über 1001 mg/kg (etwa das 19.000-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis); 1663 mg/kg bei Ratten (etwa das 62.000-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis); und 400 mg/kg bei Hunden (etwa das 50.000-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen, auf mg/m²-Basis). Während die orale mittlere letale Dosis von Albuterolsulfat bei Mäusen und Ratten größer als 2000 mg/kg war (etwa das 6600- bzw. 13.000-fache der maximal empfohlenen täglichen Inhalationsdosis bei Erwachsenen auf mg/m²-Basis), war die inhalative mittlere letale Dosis größer konnte nicht ermittelt werden. Manifestationen einer Überdosierung mit Albuterol können Angina pectoris, Bluthochdruck, Hypokaliämie, Tachykardie mit Frequenzen von bis zu 200 Schlägen pro Minute, metabolische Azidose und Übertreibung der unter NEBENWIRKUNGEN aufgeführten pharmakologischen Wirkungen umfassen. Wie bei allen sympathomimetischen Aerosol-Medikamenten können Herzstillstand und sogar der Tod mit Missbrauch in Verbindung gebracht werden. Eine Dialyse ist keine geeignete Behandlung für eine Überdosierung von Albuterol als Inhalationsaerosol; die umsichtige Anwendung eines kardiovaskulären Betarezeptorenblockers wie Metoprololtartrat kann angezeigt sein.
KONTRAINDIKATIONEN
COMBIVENT Inhalationsaerosol ist kontraindiziert bei Patienten mit bekannter Überempfindlichkeit gegen Sojalecithin oder verwandte Nahrungsmittel wie Sojabohnen und Erdnüsse. COMBIVENT Inhalationsaerosol ist auch bei Patienten kontraindiziert, die gegen andere Bestandteile des Arzneimittels oder gegen Atropin oder seine Derivate überempfindlich sind.
KLINISCHE PHARMAKOLOGIE
COMBIVENT 50 mg Aerosol zur Inhalation ist eine Kombination aus dem anticholinergen Bronchodilatator Ipratropiumbromid und dem beta2-adrenergen Bronchodilatator Albuterolsulfat.
Wirkmechanismus
Ipratropiumbromid
Ipratropiumbromid ist ein Anticholinergikum (Parasympatholytikum), das auf der Grundlage von Tierversuchen vagal vermittelte Reflexe zu hemmen scheint, indem es die Wirkung von Acetylcholin, dem Überträgerstoff, der an den neuromuskulären Verbindungen in der Lunge freigesetzt wird, antagonisiert. Anticholinergika verhindern den Anstieg der intrazellulären Konzentration von Ca++, der durch die Wechselwirkung von Acetylcholin mit den Muskarinrezeptoren auf der glatten Muskulatur der Bronchien verursacht wird.
Alberolsulfat
In-vitro-Studien und pharmakologische In-vivo-Studien haben gezeigt, dass Albuterol im Vergleich zu Isoproterenol eine bevorzugte Wirkung auf beta2-adrenerge Rezeptoren hat. Obwohl anerkannt ist, dass beta2-adrenerge Rezeptoren die vorherrschenden Rezeptoren auf der glatten Muskulatur der Bronchien sind, weisen neuere Daten darauf hin, dass es im menschlichen Herzen eine Population von beta2-Rezeptoren gibt, die zwischen 10 % und 50 % der kardialen beta-adrenergen Rezeptoren ausmachen. Die genaue Funktion dieser Rezeptoren ist jedoch noch nicht geklärt (vgl WARNUNGEN ).
Die Aktivierung von beta2-adrenergen Rezeptoren auf der glatten Muskulatur der Atemwege führt zur Aktivierung der Adenylylcyclase und zu einem Anstieg der intrazellulären Konzentration von zyklischem 3',5'-Adenosinmonophosphat (zyklisches AMP). Dieser Anstieg von zyklischem AMP führt zur Aktivierung von Proteinkinase A, die die Phosphorylierung von Myosin hemmt und die intrazellulären ionischen Calciumkonzentrationen senkt, was zu einer Entspannung führt. Albuterol entspannt die glatte Muskulatur aller Atemwege, von der Luftröhre bis zu den terminalen Bronchiolen. Albuterol wirkt als funktioneller Antagonist zur Entspannung der Atemwege unabhängig vom beteiligten Spasmogen und schützt so vor allen bronchokonstriktorischen Herausforderungen. Erhöhte Konzentrationen von zyklischem AMP sind auch mit der Hemmung der Freisetzung von Mediatoren aus Mastzellen in den Atemwegen verbunden.
Albuterol hat in den meisten klinischen Studien gezeigt, dass es bei vergleichbaren Dosen eine stärkere entspannende Wirkung auf die glatte Muskulatur der Bronchien hat als Isoproterenol, während es weniger kardiovaskuläre Wirkungen hervorruft. Alle beta-adrenergen Arzneimittel, einschließlich Albuterolsulfat, können jedoch bei einigen Patienten eine signifikante kardiovaskuläre Wirkung hervorrufen (siehe VORSICHTSMASSNAHMEN ).
COMBIVENT 20mcg Aerosol zur Inhalation
Es wird erwartet, dass Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol das Ansprechen auf die Behandlung bei Patienten mit chronisch obstruktiver Lungenerkrankung (COPD) maximiert, indem es Bronchospasmen durch zwei deutlich unterschiedliche Mechanismen reduziert, anticholinergisch (parasympatholytisch) und sympathomimetisch. Die gleichzeitige Verabreichung eines Anticholinergikums (Ipratropiumbromid) und eines Beta2-Sympathomimetikums (Albuterolsulfat) soll dem Patienten zugute kommen, indem eine stärkere bronchodilatatorische Wirkung erzielt wird, als wenn eines der beiden Arzneimittel allein in der empfohlenen Dosierung angewendet wird.
Pharmakokinetik
Ipratropiumbromid
Ein Großteil einer verabreichten Dosis wird geschluckt, wie Studien zur fäkalen Ausscheidung gezeigt haben. Ipratropiumbromid ist ein quartäres Amin. Es wird weder von der Oberfläche der Lunge noch vom Gastrointestinaltrakt leicht in den systemischen Kreislauf aufgenommen, wie durch Blutspiegel- und renale Ausscheidungsstudien bestätigt wurde. Die Plasmaspiegel von Ipratropiumbromid lagen unter der Empfindlichkeitsgrenze des Assays von 100 pg/ml.
Die Eliminationshalbwertszeit beträgt etwa 2 Stunden nach Inhalation oder intravenöser Verabreichung. Ipratropiumbromid wird minimal (0 bis 9 % in vitro) an Plasmaalbumin und α1-saures Glykoprotein gebunden. Es wird teilweise zu inaktiven Esterhydrolyseprodukten metabolisiert. Nach intravenöser Verabreichung wird etwa die Hälfte der Dosis unverändert im Urin ausgeschieden. Autoradiographische Studien an Ratten haben gezeigt, dass Ipratropiumbromid die Blut-Hirn-Schranke nicht durchdringt.
Alberolsulfat
Albuterol wirkt bei den meisten Patienten länger als Isoproterenol, da es weder ein Substrat für die zellulären Aufnahmeprozesse für Katecholamine noch für den Metabolismus durch die Catechol-O-Methyltransferase ist. Stattdessen wird der Wirkstoff konjugativ zu Albuterol-4'-O-sulfat metabolisiert.
In einer pharmakokinetischen Studie an 12 gesunden männlichen Probanden mit zwei Inhalationen von Albuterolsulfat, 103 µg Dosis/Inhalation durch das Mundstück, wurden innerhalb von drei Albuterol-Spitzenkonzentrationen im Plasma von 419 bis 802 pg/ml (Mittelwert 599 ± 122 pg/ml) erreicht Stunden nach der Verabreichung. Nach dieser Einzeldosis-Verabreichung wurden 30,8 ± 10,2 % der geschätzten Mundstückdosis unverändert im 24-Stunden-Urin ausgeschieden. Da Albuterolsulfat schnell und vollständig resorbiert wird, konnte in dieser Studie nicht zwischen pulmonaler und gastrointestinaler Resorption unterschieden werden.
Die intravenöse Pharmakokinetik von Albuterol wurde in einer vergleichbaren Gruppe von 16 gesunden männlichen Probanden untersucht; die mittlere terminale Halbwertszeit nach einer 30-minütigen Infusion von 1,5 mg betrug 3,9 Stunden mit einer mittleren Clearance von 439 ml/min/1,73 m².
Intravenöse Studien mit Albuterol an Ratten zeigten, dass Albuterol die Blut-Hirn-Schranke passierte und Konzentrationen im Gehirn erreichte, die etwa 5 % der Plasmakonzentrationen ausmachten. In Strukturen außerhalb der Blut-Hirn-Schranke (Zirbeldrüse und Hypophyse) erreichte das Medikament mehr als das 100-fache der Konzentration im gesamten Gehirn.
Studien an trächtigen Ratten mit tritiiertem Albuterol zeigten, dass etwa 10 % der zirkulierenden maternalen Droge auf den Fötus übertragen wurden. Die Disposition in der fetalen Lunge war vergleichbar mit der mütterlichen Lunge, aber die fetale Leberdisposition betrug 1 % der mütterlichen Leberspiegel.
Studien an Labortieren (Minischweine, Nagetiere und Hunde) haben das Auftreten von Herzrhythmusstörungen und plötzlichem Herztod (mit histologischem Nachweis einer Myokardnekrose) gezeigt, wenn Beta-Agonisten und Methylxanthine gleichzeitig verabreicht wurden. Die Bedeutung dieser Befunde bei Anwendung auf den Menschen ist unbekannt.
COMBIVENT 50mg Aerosol zur Inhalation
In einer pharmakokinetischen Crossover-Studie an 12 gesunden männlichen Probanden wurde das Absorptions- und Ausscheidungsmuster von zwei Inhalationen von Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol mit den beiden Wirkstoffen einzeln verglichen, die gleichzeitige Verabreichung von Ipratropiumbromid und Albuterolsulfat von einer einzigen Kanister veränderte die systemische Resorption beider Komponenten nicht signifikant.
Die Ipratropiumbromidspiegel blieben unterhalb der Nachweisgrenze (
Besondere Populationen
Die Pharmakokinetik von Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol oder Ipratropiumbromid wurde bei Patienten mit Leber- oder Niereninsuffizienz oder bei älteren Patienten nicht untersucht (siehe VORSICHTSMASSNAHMEN ).
Arzneimittelwechselwirkungen
Es wurden keine spezifischen pharmakokinetischen Studien durchgeführt, um mögliche Arzneimittelwechselwirkungen zu bewerten.
Pharmakodynamik
Ipratropiumbromid
Die Bronchodilatation nach Inhalation von Ipratropiumbromid ist in erster Linie eine lokale, ortsspezifische Wirkung, keine systemische.
Kontrollierte klinische Studien haben gezeigt, dass Ipratropiumbromid weder die mukoziliäre Clearance noch das Volumen oder die Viskosität von respiratorischen Sekreten verändert. In Studien ohne Positivkontrolle veränderte Ipratropiumbromid die Pupillengröße, die Akkommodation oder die Sehschärfe nicht (vgl NEBENWIRKUNGEN ).
Beatmungs-/Perfusionsstudien haben keine klinisch signifikanten Auswirkungen auf den pulmonalen Gasaustausch oder die arterielle Sauerstoffspannung gezeigt. In der empfohlenen Dosierung verursacht Ipratropiumbromid keine klinisch signifikanten Veränderungen der Pulsfrequenz oder des Blutdrucks.
Klinische Versuche
In zwei 12-wöchigen randomisierten, doppelblinden, aktiv kontrollierten klinischen Studien wurde die bronchodilatatorische Wirksamkeit von COMBIVENT 20 µg Inhalationsaerosol (358 Patienten) bei 1067 Patienten mit chronisch obstruktiver Lungenerkrankung (COPD) im Vergleich zu seinem Bestandteil Ipratropiumbromid untersucht (362 Patienten) und Albuterolsulfat (347 Patienten).
Serielle FEV1-Messungen (unten als prozentuale Veränderung gegenüber dem Ausgangswert am Testtag angegeben) zeigten, dass COMBIVENT Inhalationsaerosol bei separater Gabe eine signifikant stärkere Verbesserung der Lungenfunktion bewirkte als entweder Ipratropiumbromid oder Albuterolsulfat. Die mediane Zeit bis zum Einsetzen eines 15 %igen Anstiegs des FEV1 betrug 15 Minuten und die mediane Zeit bis zum FEV1-Spitzenwert eine Stunde für COMBIVENT 20 µg Inhalationsaerosol und seine Bestandteile. Die mediane Wirkungsdauer, gemessen als FEV1, betrug 4 bis 5 Stunden für COMBIVENT Inhalationsaerosol im Vergleich zu 4 Stunden für Ipratropiumbromid und 3 Stunden für Albuterolsulfat.
Prozentuale Veränderung des angepassten mittleren FEV1 gegenüber dem Ausgangswert am Testtag – Endpunktanalyse des auswertbaren Datensatzes 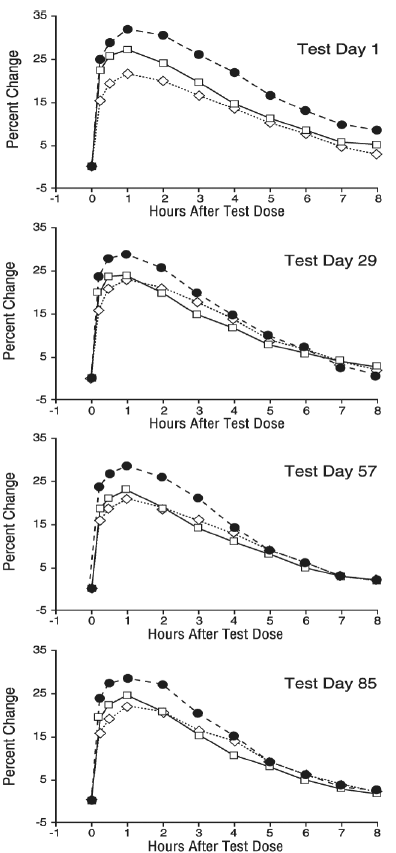
Diese Studien zeigten, dass jeder Bestandteil von Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol zur Verbesserung der Lungenfunktion beitrug, die durch die Kombination hervorgerufen wurde, insbesondere während der ersten 4 bis 5 Stunden nach der Verabreichung, und dass COMBIVENT Inhalationsaerosol signifikant wirksamer war als allein verabreichtes Ipratropiumbromid oder Albuterolsulfat.
In den 2 kontrollierten 12-wöchigen Studien bewirkte COMBIVENT 50 mg Inhalationsaerosol keine Veränderung der sekundären Wirksamkeitsparameter, einschließlich Symptom-Scores, globaler Beurteilung durch den Arzt und morgendlichem PEFR, die alle während des Studienzeitraums überwacht wurden.
INFORMATIONEN ZUM PATIENTEN
Gebrauchsanweisung des Patienten
Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalation Aerosol
Lesen Sie die vollständigen Anweisungen vor der Verwendung sorgfältig durch
Wenden Sie COMBIVENT 50 mg Inhalationsaerosol genau nach Anweisung Ihres Arztes an. Ändern Sie nicht Ihre Dosis oder wie oft Sie COMBIVENT 20 µg Inhalationsaerosol anwenden, ohne mit Ihrem Arzt zu sprechen. Sprechen Sie mit Ihrem Arzt, wenn Sie Fragen zu Ihrem Gesundheitszustand oder Ihrer Behandlung haben.
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen. COMBIVENT 50 mg Aerosol zur Inhalation und einige andere Arzneimittel können miteinander interagieren. Wenden Sie keine anderen inhalativen Arzneimittel zusammen mit COMBIVENT 20 µg Inhalationsaerosol an, es sei denn, Ihr Arzt hat es Ihnen verordnet.
1. Setzen Sie den Metallkanister in das durchsichtige Ende des Mundstücks ein (siehe Abbildung 1). Stellen Sie sicher, dass der Kanister vollständig und fest in das Mundstück eingesetzt ist. Der COMBIVENT Inhalationsaerosolbehälter darf nur mit dem COMBIVENT Inhalationsaerosol-Mundstück verwendet werden. Dieses Mundstück sollte nicht mit anderen inhalativen Arzneimitteln verwendet werden.
Abbildung 1 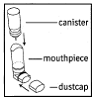
2. Orange Staubschutzkappe entfernen. Wenn sich die Kappe nicht auf dem Mundstück befindet, vergewissern Sie sich vor der Verwendung, dass sich nichts im Mundstück befindet. Für beste Ergebnisse sollte der Kanister vor Gebrauch Raumtemperatur haben.
3. Schütteln und Probesprühen. Führen Sie diesen Schritt vor der ersten Verwendung durch und immer dann, wenn das Aerosol länger als 24 Stunden nicht verwendet wurde; Fahren Sie andernfalls direkt mit Schritt 4 fort.
Nachdem Sie den Kanister mindestens 10 Sekunden lang kräftig geschüttelt haben (siehe Schritt 4 für Anweisungen zum Schütteln), sprühen Sie 3 Mal „testweise“ in die Luft. Nicht in die Augen sprühen.
4. Kanister mindestens 10 Sekunden lang kräftig schütteln. Kanister wie in Abbildung 2 dargestellt halten.
WICHTIG: Kräftiges Schütteln für mindestens 10 Sekunden vor jedem Sprühen ist sehr wichtig für die richtige Produktleistung.
Führen Sie für beste Ergebnisse die Schritte 5 und 6 innerhalb von 30 Sekunden nach dem Schütteln des Kanisters durch.
Figur 2 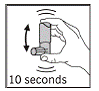
5. Atmen Sie tief durch den Mund aus (ausatmen). Halten Sie den Kanister wie in Abbildung 3 gezeigt aufrecht zwischen Daumen und Finger(n), nehmen Sie das Mundstück in den Mund und schließen Sie die Lippen. Halten Sie Ihre Augen geschlossen, damit kein Arzneimittel in Ihre Augen gesprüht wird. Combivent® (Ipratropiumbromid und Albuterolsulfat) Aerosol zur Inhalation kann verschwommenes Sehen, Engwinkelglaukom oder eine Verschlechterung dieses Zustands oder Augenschmerzen verursachen, wenn das Arzneimittel in Ihre Augen gesprüht wird.
Figur 3 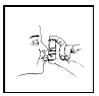
6. Atmen Sie langsam durch den Mund ein (inhalieren) und sprühen Sie gleichzeitig das Produkt in den Mund.
Um das Produkt zu sprühen, drücken Sie den Kanister einmal fest gegen das Mundstück, wie in Abbildung 4 gezeigt. Atmen Sie weiter tief ein.
Figur 4 
7. Halten Sie den Atem 10 Sekunden lang an, nehmen Sie das Mundstück aus dem Mund und atmen Sie langsam aus, wie in Abbildung 5.
Abbildung 5 
8. Warten Sie etwa 2 Minuten, schütteln Sie den Inhalator erneut mindestens 10 Sekunden lang kräftig (wie in Schritt 4 beschrieben) und wiederholen Sie die Schritte 5 bis 7.
9. Setzen Sie die orangefarbene Staubschutzkappe nach Gebrauch wieder auf.
10. Halten Sie das Mundstück sauber. Mit heißem Wasser waschen. Bei Verwendung von Seife gründlich mit klarem Wasser nachspülen. Vor Gebrauch gründlich trocknen. Setzen Sie die Kappe nach dem Trocknen wieder auf das Mundstück, wenn Sie das Arzneimittel nicht verwenden.
11. Notieren Sie die Anzahl der verwendeten Sprühstöße und entsorgen Sie sie nach 200 Sprühstößen. Auch wenn der Kanister nicht leer ist, können Sie nach 200 Sprühstößen nicht sicher sein, wie viel Arzneimittel in jedem Sprühstoß enthalten ist.
12. Wenn Ihre verschriebene Dosis keine Linderung bringt oder sich Ihre Atembeschwerden verschlimmern, suchen Sie sofort medizinische Hilfe auf.
Notiz: Der folgende eingerückte Hinweis wird vom Luftreinhaltegesetz der Bundesregierung für alle Produkte verlangt, die Fluorchlorkohlenwasserstoffe (FCKW) enthalten oder daraus hergestellt werden:
Dieses Produkt enthält Trichlormonofluormethan (CFC-11), Dichlordifluormethan (CFC-12) und Dichlortetrafluorethan (CFC-114), Substanzen, die die Umwelt schädigen, indem sie Ozon in der oberen Atmosphäre zerstören.
Der Inhalt von Combivent® (Ipratropiumbromid und Albuterolsulfat) Inhalationsaerosol steht unter Druck. Kanister nicht durchstechen. Nicht in der Nähe von Hitze oder offenem Feuer verwenden oder lagern. Temperaturen über 120 °F können zum Platzen führen. Werfen Sie den Behälter niemals in ein Feuer oder eine Verbrennungsanlage.
Bewahren Sie COMBIVENT Inhalationsaerosol außerhalb der Reichweite von Kindern auf.
Nicht in die Augen sprühen.
Richten Sie medizinische Anfragen an: http://us.boehringer-ingelheim.com, (800) 542-6257 oder (800) 459-9906 TTY.
Bei 25 °C (77 °F) lagern; Exkursionen erlaubt bis 15°-30°C (59°-86°F) [sehen USP kontrollierte Raumtemperatur ]. Für beste Ergebnisse den Kanister vor Gebrauch bei Raumtemperatur lagern. Vermeiden Sie übermäßige Feuchtigkeit.