Furadantin 100mg Nitrofurantoin Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Furadantin 100 mg und wie wird es angewendet?
Furadantin (Nitrofurantoin-Suspension zum Einnehmen) ist ein Antibiotikum zur Behandlung von Harnwegsinfektionen. Furadantin ist in generischer Form erhältlich.
Welche Nebenwirkungen hat Furadantin?
Häufige Nebenwirkungen von Furadantin sind:
Informieren Sie Ihren Arzt, wenn bei Ihnen seltene, aber sehr schwerwiegende Nebenwirkungen von Furadantin auftreten, einschließlich:
BEZEICHNUNG
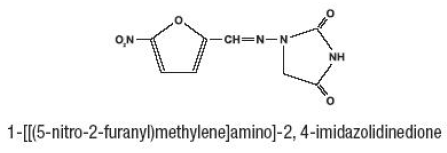
Furadantin (Nitrofurantoin), eine synthetische Chemikalie, ist eine stabile, gelbe, kristalline Verbindung. Furadantin ist ein antibakterielles Mittel für spezifische Harnwegsinfektionen. Furadantin ist als 25 mg/5 ml flüssige Suspension zur oralen Verabreichung erhältlich.
Inaktive Zutaten
Furadantin Suspension zum Einnehmen enthält Carboxymethylcellulose-Natrium, Zitronensäure, Aromen, Glycerin, Magnesium-Aluminium-Silikat, Methylparaben, Propylparaben, gereinigtes Wasser, Natriumcitrat und Sorbitol.
INDIKATIONEN
Furadantin ist speziell für die Behandlung von Harnwegsinfektionen angezeigt, wenn diese auf empfindliche Stämme von Escherichia coli, Enterokokken, Staphylococcus aureus und bestimmte empfindliche Stämme von Klebsiella- und Enterobacter-Arten zurückzuführen sind.
Nitrofurantoin ist nicht angezeigt zur Behandlung von Pyelonephritis oder perinephrischen Abszessen.
Nitrofurantoinen fehlt die breitere Gewebeverteilung anderer Therapeutika, die für Harnwegsinfektionen zugelassen sind. Folglich viele Patienten, die mit behandelt werden Furadantin sind für das Fortbestehen oder Wiederauftreten einer Bakteriurie prädisponiert. Urinproben für Kultur- und Empfindlichkeitstests sollten vor und nach Abschluss der Therapie entnommen werden. Wenn nach der Behandlung mit Furadantin , sollten andere Therapeutika mit einer breiteren Gewebeverteilung ausgewählt werden. In Anbetracht der Verwendung von Furadantin , sollten niedrigere Eradikationsraten gegen das erhöhte Potenzial für systemische Toxizität und für die Entwicklung einer antimikrobiellen Resistenz abgewogen werden, wenn Wirkstoffe mit einer breiteren Gewebeverteilung verwendet werden.
DOSIERUNG UND ANWENDUNG
Furadantin sollte zusammen mit Nahrung verabreicht werden, um die Arzneimittelabsorption und bei einigen Patienten die Verträglichkeit zu verbessern.
Erwachsene
50-100 mg viermal täglich – die niedrigere Dosierung wird bei unkomplizierten Harnwegsinfektionen empfohlen.
Pädiatrische Patienten
5-7 mg/kg Körpergewicht alle 24 Stunden, verteilt auf vier Einzeldosen (kontraindiziert unter einem Monat).
Die folgende Tabelle basiert auf einem durchschnittlichen Gewicht in jedem Bereich, bei dem 5 bis 6 mg/kg Körpergewicht alle 24 Stunden in vier aufgeteilten Dosen verabreicht wurden. Es kann verwendet werden, um eine durchschnittliche Dosis von zu berechnen Furadantin Suspension zum Einnehmen (25 mg/5 ml) für pädiatrische Patienten.
Die Therapie sollte für eine Woche oder für mindestens 3 Tage fortgesetzt werden, nachdem die Sterilität des Urins erreicht wurde. Eine fortgesetzte Infektion weist auf die Notwendigkeit einer Neubewertung hin.
Für eine Langzeit-Suppressionstherapie bei Erwachsenen kann eine Dosisreduktion auf 50-100 mg vor dem Schlafengehen angemessen sein. Für eine langfristige Suppressionstherapie bei pädiatrischen Patienten können Dosen von nur 1 mg/kg alle 24 Stunden, verabreicht in einer Einzeldosis oder in zwei getrennten Dosen, angemessen sein. SEHEN ABSCHNITT WARNHINWEISE ZU RISIKEN IM ZUSAMMENHANG MIT DER LANGZEITTHERAPIE .
WIE GELIEFERT
Furadantin Orale Suspension ist erhältlich in:
NDC 70199-006-32 Braune PET-Flasche mit 230 ml
Vermeiden Sie starkes Licht, das das Medikament verdunkeln kann. Es ist bei Lagerung zwischen 20° und 25°C (68°-77°F) stabil; Exkursionen erlaubt bis 15°-30°C (59°-86°F) [Siehe USP kontrollierte Raumtemperatur ]. Vor Frost schützen. Kräftig schütteln. In einen dichten, lichtbeständigen Kunststoff- (PET) oder Glasbehälter geben.
Innerhalb von 30 Tagen verwenden.
Außerhalb der Reichweite von Kindern aufbewahren.
Hergestellt für: Casper Pharma LLC, East Brunswick NJ 08816. Überarbeitet: Dez 2020
NEBENWIRKUNGEN
Atmung
CHRONISCHE, SUBAKUTE ODER AKUTE PULMONALE HYPERSENSIBILITÄTSREAKTIONEN KÖNNEN AUFTRETEN.
CHRONISCHE LUNGENREAKTIONEN KÖNNEN IM ALLGEMEINEN BEI PATIENTEN AUFTRETEN, DIE KONTINUIERLICH 6 MONATE ODER LÄNGER BEHANDELT WERDEN. Unwohlsein, Belastungsdyspnoe, Husten und Lungenfunktionsstörungen sind häufige Erscheinungen, die schleichend auftreten können. RADIOLOGISCHE UND HISTOLOGISCHE ERGEBNISSE EINER DIFFUSE INTERSTITIAL PNEUMONITIS ODER FIBROSE ODER BEIDES SIND AUCH HÄUFIGE Manifestationen der chronischen Lungenreaktion. FIEBER IST SELTEN PROMINENT.
DER SCHWER DER CHRONISCHEN LUNGENREAKTIONEN UND IHRER AUFLÖSUNGSGRAD SCHEINT MIT DER DAUER DER THERAPIE NACH DEM ERSCHEINEN DER ERSTEN KLINISCHEN ANZEICHEN IN ZUSAMMENHANG ZU STEHEN. AUCH NACH BEENDIGUNG DER THERAPIE KANN DIE LUNGENFUNKTION DAUERHAFT BESCHRÄNKT SEIN. DAS RISIKO IST GRÖSSER, WENN CHRONISCHE LUNGENREAKTIONEN NICHT FRÜHZEITIG ERKANNT WERDEN.
Bei subakuten Lungenreaktionen treten Fieber und Eosinophilie seltener auf als bei der akuten Form. Nach Beendigung der Therapie kann die Genesung mehrere Monate dauern. Wenn die Symptome nicht als arzneimittelbedingt erkannt werden und die Nitrofurantoin-Therapie nicht beendet wird, können sich die Symptome verschlimmern.
Akute pulmonale Reaktionen äußern sich häufig in Fieber, Schüttelfrost, Husten, Brustschmerzen, Dyspnoe, Lungeninfiltration mit Konsolidierung des Pleuraergusses im Röntgenbild und Eosinophilie.
Akute Reaktionen treten normalerweise innerhalb der ersten Behandlungswoche auf und sind nach Beendigung der Therapie reversibel. Die Auflösung ist oft dramatisch. (sehen WARNUNGEN )
EKG-Veränderungen (z. B. unspezifische ST/T-Wellen-Veränderungen, Schenkelblock) wurden im Zusammenhang mit pulmonalen Reaktionen berichtet.
Zyanose wurde selten berichtet.
Leber
Leberreaktionen, einschließlich Hepatitis, cholestatischer Gelbsucht, chronisch aktiver Hepatitis und hepatischer Neurose, treten selten auf. (sehen WARNUNGEN )
Neurologische
Es ist eine periphere Neuropathie aufgetreten, die schwerwiegend oder irreversibel werden kann. Es wurden Todesfälle gemeldet. Erkrankungen wie Nierenfunktionsstörung (Kreatinin-Clearance unter 60 ml pro Minute oder klinisch signifikant erhöhtes Serumkreatinin), Anämie, Diabetes mellitus, Elektrolytstörungen, Vitamin-B-Mangel und schwächende Erkrankungen können die Möglichkeit einer peripheren Neuropathie erhöhen (siehe WARNUNGEN )
Bei der Anwendung von Nitrofurantoin wurde auch über Asthenie, Schwindel, Nystagmus, Schwindel, Kopfschmerzen und Benommenheit berichtet.
Selten wurde über gutartige intrakranielle Hypertonie (Pseudotumor cerebri), Verwirrtheit, Depression, Optikusneuritis und psychotische Reaktionen berichtet. Vorgewölbte Fontanellen als Zeichen einer gutartigen intrakraniellen Hypertonie bei Säuglingen wurden selten berichtet.
Dermatologisch
Selten wurde über exfoliative Dermatitis und Erythema multiforme (einschließlich Stevens-Johnson-Syndrom) berichtet. Es wurde auch über vorübergehende Alopezie berichtet.
Allergisch
Es wurde über ein Lupus-ähnliches Syndrom im Zusammenhang mit Lungenreaktionen auf Nitrofurantoin berichtet. Auch Angioödem; makulopapulöse, erythematöse oder ekzematöse Eruptionen; Juckreiz; Urtikaria; Anaphylaxie; Arthralgie; Myalgie; Drogenfieber; und Vaskulitis (manchmal verbunden mit Lungenreaktionen) wurden berichtet. Überempfindlichkeitsreaktionen sind die häufigsten spontan gemeldeten unerwünschten Ereignisse in der weltweiten Postmarketing-Erfahrung mit Nitrofurantoin-Formulierungen.
Magen-Darm
Am häufigsten treten Übelkeit, Erbrechen und Anorexie auf. Bauchschmerzen und Durchfall sind weniger häufige Magen-Darm-Reaktionen. Diese dosisabhängigen Reaktionen können durch Dosisreduktion minimiert werden. Sialadenitis und Pankreatitis wurden berichtet. Es gab sporadische Berichte über pseudomembranöse Kolitis bei der Anwendung von Nitrofurantoin. Das Auftreten pseudomembranöser Colitis-Symptome kann während oder nach einer antimikrobiellen Behandlung auftreten. (sehen WARNUNGEN )
Hämatologisch
Zyanose als Folge einer Methämoglobinämie wurde selten berichtet.
Sonstig
Wie bei anderen antimikrobiellen Wirkstoffen können Superinfektionen durch resistente Organismen, z. B. Pseudomonas-Spezies oder Candida-Spezies, auftreten. Es gibt sporadische Berichte über Clostridium-difficile-Superinfektionen oder pseudomembranöse Kolitis bei der Anwendung von Nitrofurantoin.
Unerwünschte Ereignisse im Labor
Die folgenden unerwünschten Laborereignisse wurden bei der Anwendung von Nitrofurantoin berichtet; erhöhter AST (SGOT), erhöhter ALT (SGPT), erniedrigter Hämoglobinwert, erhöhter Phosphor im Serum, Eosinophilie, Glucose-6-Phosphat-Dehydrogenase-Mangelanämie (vgl WARNUNGEN ), Agranulozytose, Leukopenie, Granulozytopenie, hämolytische Anämie, Thrombozytopenie, Megaloblastenanämie. In den meisten Fällen bildeten sich diese hämatologischen Anomalien nach Beendigung der Therapie zurück. Aplastische Anämie wurde selten berichtet.
Um VERMUTLICHE NEBENWIRKUNGEN zu melden, wenden Sie sich an Casper Pharma LLC. unter 1-844-5-CASPER (1-844-522-7737) oder FDA unter 1-800-FDA-1088 oder www.fda.gov/medwatch.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Antazida, die Magnesiumtrisilikat enthalten, verringern bei gleichzeitiger Verabreichung mit Nitrofurantoin sowohl die Geschwindigkeit als auch das Ausmaß der Resorption. Der Mechanismus für diese Wechselwirkung ist wahrscheinlich die Adsorption von Nitrofurantoin auf der Oberfläche von Magnesiumtrisilicat.
Urikosurika wie Probenecid und Sulfinpyrazon können die renale tubuläre Sekretion von Nitrofurantoin hemmen. Der daraus resultierende Anstieg der Nitrofurantoin-Serumspiegel kann die Toxizität erhöhen, und die verringerten Urinspiegel könnten seine Wirksamkeit als antibakterielles Mittel im Harntrakt verringern.
Wechselwirkungen zwischen Arzneimitteln und Labortests
Als Folge des Vorhandenseins von Nitrofurantoin kann es zu einer falsch-positiven Reaktion auf Glucose im Urin kommen. Dies wurde mit Lösungen von Benedict und Fehling beobachtet, nicht jedoch mit dem enzymatischen Glucosetest.
WARNUNGEN
Lungenreaktionen
AKUTE, SUBAKUTE ODER CHRONISCHE LUNGENREAKTIONEN WURDEN BEI MIT NITROFURANTOIN BEHANDELTEN PATIENTEN BEOBACHTET. WENN DIESE REAKTIONEN AUFTRETEN, SOLLTE FURADANTIN 100 mg ABGESETZT UND GEEIGNETE MASSNAHMEN ERGREIFEN WERDEN. BERICHTE HABEN LUNGENREAKTIONEN ALS BEITRAGENDE TODESURSACHE ANGEGEBEN.
CHRONISCHE LUNGENREAKTIONEN (DIFFUSE INTERSTITIAL PNEUMONITIS ODER LUNGENFIBROSE ODER BEIDES) KÖNNEN SICH SCHLECHTEN ENTWICKELN. DIESE REAKTIONEN TRETEN SELTEN UND ALLGEMEIN BEI PATIENTEN AUF, DIE EINE THERAPIE FÜR 6 MONATE ODER LÄNGER ERHALTEN. EINE ENGE ÜBERWACHUNG DES LUNGENZUSTANDS VON PATIENTEN, DIE EINE LANGZEITTHERAPIE ERHALTEN, IST GEWÄHRLEISTET UND ERFORDERT, DASS DER NUTZEN DER THERAPIE GEGEN POTENZIELLE RISIKEN ABGEWEGT WIRD. (Siehe ATEMREAKTIONEN.)
Hepatotoxizität
Leberreaktionen, einschließlich Hepatitis, cholestatischer Gelbsucht, chronisch aktiver Hepatitis und Lebernekrose, treten selten auf. Es wurden Todesfälle gemeldet. Der Beginn einer chronisch aktiven Hepatitis kann schleichend sein, und die Patienten sollten regelmäßig auf Veränderungen in biochemischen Tests überwacht werden, die auf eine Leberschädigung hinweisen würden. Wenn eine Hepatitis auftritt, sollte das Medikament sofort abgesetzt und geeignete Maßnahmen ergriffen werden.
Neuropathie
Es ist eine periphere Neuropathie aufgetreten, die schwerwiegend oder irreversibel werden kann. Es wurden Todesfälle gemeldet. Erkrankungen wie Nierenfunktionsstörung (Kreatinin-Clearance unter 60 ml pro Minute oder klinisch signifikant erhöhtes Serumkreatinin), Anämie, Diabetes mellitus, Elektrolytstörungen, Vitamin-B-Mangel und schwächende Erkrankungen können das Auftreten einer peripheren Neuropathie verstärken. Patienten, die eine Langzeittherapie erhalten, sollten regelmäßig auf Veränderungen der Nierenfunktion überwacht werden.
Optikusneuritis wurde in Postmarketing-Erfahrungen mit Nitrofurantoin-Formulierungen selten berichtet.
Hämolytische Anämie
Fälle von hämolytischer Anämie vom Primaquin-Sensitivitätstyp wurden durch Nitrofurantoin induziert. Die Hämolyse scheint mit einem Glucose-6-Phosphat-Dehydrogenase-Mangel in den roten Blutkörperchen der betroffenen Patienten verbunden zu sein. Dieser Mangel findet sich bei 10 Prozent der Schwarzen und einem kleinen Prozentsatz der ethnischen Gruppen mediterraner und nahöstlicher Herkunft. Hämolyse ist eine Indikation zum Absetzen Furadantin Die Hämolyse hört auf, wenn das Medikament abgesetzt wird.
Clostridium difficile-assoziierter Durchfall
Clostridium difficile-assoziierte Diarrhoe (CDAD) wurde bei der Anwendung von fast allen antibakteriellen Mitteln berichtet, einschließlich Furadantin Suspension zum Einnehmen, und kann im Schweregrad von leichtem Durchfall bis hin zu tödlicher Kolitis reichen. Die Behandlung mit antibakteriellen Mitteln verändert die normale Flora des Dickdarms, was zu einem übermäßigen Wachstum von C. difficile führt.
C. difficile produziert die Toxine A und B, die zur Entstehung von CDAD beitragen. Hypertoxin produzierende Stämme von C. difficile verursachen eine erhöhte Morbidität und Mortalität, da diese Infektionen gegenüber einer antimikrobiellen Therapie refraktär sein können und eine Kolektomie erfordern können. CDAD muss bei allen Patienten in Betracht gezogen werden, bei denen nach der Anwendung von Antibiotika Durchfall auftritt. Eine sorgfältige Anamnese ist erforderlich, da berichtet wurde, dass CDAD mehr als zwei Monate nach der Verabreichung von Antibiotika auftritt.
Wenn CDAD vermutet oder bestätigt wird, muss die laufende Anwendung von Antibiotika, die nicht gegen C. difficile gerichtet sind, möglicherweise eingestellt werden. Je nach klinischer Indikation sollte ein angemessenes Flüssigkeits- und Elektrolytmanagement, eine Proteinergänzung, eine antibiotische Behandlung von C. difficile und eine chirurgische Untersuchung eingeleitet werden.
VORSICHTSMASSNAHMEN
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Nitrofurantoin war nicht karzinogen, wenn es 44,5 Wochen lang an weibliche Holtzman-Ratten oder 75 Wochen lang an weibliche Sprague-Dawley-Ratten verfüttert wurde. Zwei chronische Bioassays an Nagetieren mit männlichen und weiblichen Sprague-Dawley-Ratten und zwei chronische Bioassays an Swiss-Mäusen und an BDF1-Mäusen ergaben keine Hinweise auf Karzinogenität.
Nitrofurantoin lieferte Hinweise auf eine karzinogene Aktivität bei weiblichen B6C3F1-Mäusen, wie durch erhöhte Inzidenzen von tubulären Adenomen, gutartigen Mischtumoren und Granulosazelltumoren der Eierstöcke gezeigt wurde. Bei männlichen F344/N-Ratten gab es eine erhöhte Inzidenz von gelegentlichen tubulären Nierenzelltumoren, Osteosarkomen des Knochens und Neoplasmen des subkutanen Gewebes. In einer Studie mit subkutaner Verabreichung von 75 mg/kg Nitrofurantoin an trächtige weibliche Mäuse wurden Lungenpapillenadenome unbekannter Bedeutung in der F1-Generation beobachtet.
Es wurde gezeigt, dass Nitrofurantoin Punktmutationen in bestimmten Stämmen von Salmonella typhimurium und Vorwärtsmutationen in L5178Y-Maus-Lymphomzellen induziert. Nitrofurantoin induzierte eine erhöhte Anzahl von Schwesterchromatid-Austauschen und Chromosomenaberrationen in Eierstockzellen des chinesischen Hamsters, jedoch nicht in menschlichen Zellen in Kultur. Die Ergebnisse des geschlechtsgebundenen rezessiven letalen Assays bei Drosophila waren nach Verabreichung von Nitrofurantoin durch Fütterung oder Injektion negativ. Nitrofurantoin induzierte keine vererbbare Mutation in den untersuchten Nagetiermodellen.
Die Bedeutung von Karzinogenitäts- und Mutagenitätsbefunden in Bezug auf die therapeutische Anwendung von Nitrofurantoin beim Menschen ist nicht bekannt.
Die Verabreichung hoher Dosen von Nitrofurantoin an Ratten führt zu einem vorübergehenden Stillstand der Spermatogenese; dies ist nach Absetzen des Medikaments reversibel. Dosen von 10 mg/kg/Tag oder mehr bei gesunden Männern können in bestimmten unvorhersehbaren Fällen zu einem leichten bis mäßigen Spermienstillstand mit einer Abnahme der Spermienzahl führen.
Schwangerschaft
Teratogene Wirkungen
Mehrere Reproduktionsstudien wurden an Kaninchen und Ratten mit Dosierungen bis zum Sechsfachen der Humandosis durchgeführt und ergaben keine Hinweise auf eine Beeinträchtigung der Fertilität oder eine Schädigung des Fötus durch Nitrofurantoin. In einer einzigen veröffentlichten Studie, die an Mäusen mit dem 68-Fachen der menschlichen Dosis (basierend auf mg/kg, die dem Muttertier verabreicht wurde) durchgeführt wurde, wurden Wachstumsverzögerungen und eine geringe Inzidenz von geringfügigen und häufigen Missbildungen beobachtet. Bei der 25-fachen Humandosis wurden jedoch keine Fehlbildungen des Fötus beobachtet; die Relevanz dieser Befunde für den Menschen ist ungewiss. Es gibt jedoch keine adäquaten und gut kontrollierten Studien bei Schwangeren. Da Reproduktionsstudien an Tieren die menschliche Reaktion nicht immer vorhersagen, sollte dieses Medikament während der Schwangerschaft nur angewendet werden, wenn dies eindeutig erforderlich ist.
Nicht teratogene Wirkungen
In einer veröffentlichten transplazentaren Kanzerogenitätsstudie wurde gezeigt, dass Nitrofurantoin bei Mäusen der F1-Generation bei Dosen, die das 19-fache der Humandosis auf mg/kg-Basis betragen, papilläre Adenome der Lunge induziert. Der Zusammenhang zwischen diesem Befund und einer möglichen Karzinogenese beim Menschen ist derzeit nicht bekannt. Aufgrund der Ungewissheit hinsichtlich der Auswirkungen dieser Tierdaten auf den Menschen sollte dieses Arzneimittel während der Schwangerschaft nur angewendet werden, wenn dies eindeutig erforderlich ist.
Arbeit und Lieferung
Sehen KONTRAINDIKATIONEN .
Stillende Mutter
Nitrofurantoin wurde in Spuren in der Muttermilch nachgewiesen. Aufgrund der Möglichkeit schwerwiegender Nebenwirkungen von Nitrofurantoin bei gestillten Säuglingen unter einem Monat sollte eine Entscheidung getroffen werden, ob das Stillen oder das Arzneimittel abgesetzt werden soll, wobei die Bedeutung des Arzneimittels für die Mutter zu berücksichtigen ist. (sehen KONTRAINDIKATIONEN )
Pädiatrische Verwendung
Sicherheit und Wirksamkeit von Furadantin bei Neugeborenen unter einem Monat wurden nicht festgestellt. (sehen KONTRAINDIKATIONEN )
ÜBERDOSIS
Gelegentliche Fälle von akuter Überdosierung von Furadantin haben außer Erbrechen zu keinen spezifischen Symptomen geführt. Die Induktion von Erbrechen wird empfohlen. Es gibt kein spezifisches Antidot, aber es sollte eine hohe Flüssigkeitsaufnahme aufrechterhalten werden, um die Ausscheidung des Arzneimittels über den Urin zu fördern. Es ist dialysierbar.
KONTRAINDIKATIONEN
Anurie, Oligurie oder signifikante Beeinträchtigung der Nierenfunktion (Kreatinin-Clearance unter 60 ml pro Minute oder klinisch signifikant erhöhtes Serumkreatinin) sind Kontraindikationen. Die Behandlung dieses Patiententyps birgt aufgrund der beeinträchtigten Ausscheidung des Arzneimittels ein erhöhtes Toxizitätsrisiko.
Aufgrund der Möglichkeit einer hämolytischen Anämie aufgrund unreifer Erythrozyten-Enzymsysteme (Glutathion-Instabilität) ist das Medikament bei schwangeren Patientinnen am Termin (38.–42. Schwangerschaftswoche), während der Wehen und Entbindung oder wenn der Beginn der Wehen unmittelbar bevorsteht, kontraindiziert. Aus dem gleichen Grund ist das Medikament bei Neugeborenen unter einem Monat kontraindiziert.
Furadantin ist kontraindiziert bei Patienten mit cholestatischer Gelbsucht/Leberfunktionsstörung in Verbindung mit Nitrofurantoin in der Vorgeschichte. Furadantin ist auch bei Patienten mit bekannter Überempfindlichkeit gegenüber Nitrofurantoin kontraindiziert.
KLINISCHE PHARMAKOLOGIE
Oral verabreicht Furadantin wird leicht absorbiert und schnell im Urin ausgeschieden. Die Blutkonzentrationen bei therapeutischer Dosierung sind normalerweise niedrig. Es ist im Urin sehr gut löslich, dem es eine braune Farbe verleihen kann.
Nach einem Dosierungsschema von 100 mg 4-mal täglich über 7 Tage betrug die durchschnittliche Wiederfindung des Arzneimittels im Urin (0-24 Stunden) an Tag 1 und Tag 7 42,7 % und 43,6 %.
Im Gegensatz zu vielen Arzneimitteln kann die Anwesenheit von Nahrungsmitteln oder Mitteln, die die Magenentleerung verzögern, die Bioverfügbarkeit von erhöhen Furadantin , vermutlich durch eine bessere Auflösung in Magensäften.
Mikrobiologie
Wirkungsweise
Nitrofurantoin wird durch eine Vielzahl von Enzymen, einschließlich bakterieller Flavoproteine, zu reaktiven Zwischenprodukten reduziert, die Makromoleküle wie DNA und Proteine schädigen.
Kreuzresistenz
Obwohl eine Kreuzresistenz mit anderen Antibiotika auftreten kann, wurde eine Kreuzresistenz mit Sulfonamiden nicht beobachtet.
Wechselwirkung mit anderen antimikrobiellen Mitteln
Antagonismus wurde in vitro zwischen Nitrofurantoin und Chinolon-Antibiotika nachgewiesen. Nitrofurantoin in Form einer Nitrofurantoin-Suspension zum Einnehmen hat sich sowohl in vitro als auch bei klinischen Infektionen als wirksam gegen die meisten der folgenden Bakterien erwiesen: (Siehe INDIKATIONEN UND VERWENDUNG ).
Gram-positive Aerobier
Staphylococcus aureusEnterococcus-Spezies
Gramnegative Aeroben
Escherichia coli
HINWEIS: Einige Stämme von Enterobacter-Arten und Klebsiella-Arten sind resistent gegen Nitrofurantoin.
Die folgenden In-vitro-Daten sind verfügbar, ihre klinische Bedeutung ist jedoch nicht bekannt. Nitrofurantoin zeigt in vitro Aktivität gegen die folgenden Bakterien; Die Sicherheit und Wirksamkeit von Nitrofurantoin bei der Behandlung klinischer Infektionen durch diese Bakterien wurden jedoch nicht in angemessenen und gut kontrollierten klinischen Studien nachgewiesen.
Gram-positive Aerobier
Koagulase-negative Staphylokokken (einschließlich Staphylococcus epidermidis und Staphylococcus saprophyticus)Streptococcus agalactiaeStreptokokken der Viridans-Gruppe
Gramnegative Aeroben
Citrobacter koseriCitrobacter freundiiKlebsiella oxytoca
Nitrofurantoin ist gegen die meisten Stämme von Proteus-Spezies oder Serratia-Spezies nicht aktiv. Es hat keine Aktivität gegen Pseudomonas-Spezies.
Empfindlichkeitsprüfung
Spezifische Informationen zu den Interpretationskriterien von Empfindlichkeitstests und zugehörigen Testmethoden und Qualitätskontrollstandards, die von der FDA für dieses Medikament anerkannt sind, finden Sie unter: http://www.fda.gov/STIC.
INFORMATIONEN ZUM PATIENTEN
Patienten sollten zur Einnahme geraten werden Furadantin mit Nahrung, um die Toleranz weiter zu verbessern und die Arzneimittelabsorption zu verbessern. Die Patienten sollten angewiesen werden, den gesamten Therapieverlauf zu Ende zu führen; Sie sollten jedoch angewiesen werden, sich an ihren Arzt zu wenden, falls während der Therapie ungewöhnliche Symptome auftreten sollten.
Durchfall ist ein häufiges Problem, das durch Antibiotika verursacht wird und normalerweise endet, wenn das Antibiotikum abgesetzt wird. Manchmal können Patienten nach Beginn der Behandlung mit Antibiotika wässrigen und blutigen Stuhl (mit oder ohne Magenkrämpfe und Fieber) sogar noch zwei oder mehr Monate nach Einnahme der letzten Dosis des Antibiotikums entwickeln. In diesem Fall sollten die Patienten so schnell wie möglich ihren Arzt kontaktieren.
Die Patienten sollten darauf hingewiesen werden, während der Einnahme keine Antazidumpräparate mit Magnesiumtrisilicat zu verwenden Furadantin .