Mobic 7.5mg, 15mg Meloxicam Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Mobic 15 mg und wie wird es angewendet?
Mobic 7,5 mg ist ein verschreibungspflichtiges nichtsteroidales entzündungshemmendes Arzneimittel zur Behandlung der Symptome von Osteoarthritis, rheumatoider Arthritis und mäßigen bis starken Schmerzen. Mobic 7,5 mg kann allein oder mit anderen Medikamenten verwendet werden.
Mobic ist ein nichtsteroidales Antirheumatikum (NSAID).
Es ist nicht bekannt, ob Mobic bei Kindern mit einem Gewicht von weniger als 60 kg sicher und wirksam ist.
Was sind die möglichen Nebenwirkungen von Mobic 7,5 mg?
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigsten Nebenwirkungen von Mobic 15 mg gehören:
Teilen Sie dem Arzt mit, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Mobic. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
WARNUNG
RISIKO SCHWERER KARDIOVASKULÄRER UND GASTROINTESTINALER EREIGNISSE
Kardiovaskuläre thrombotische Ereignisse
Magen-Darm-Blutungen, Ulzerationen und Perforationen
BEZEICHNUNG
MOBIC (Meloxicam) ist ein nichtsteroidales Antirheumatikum (NSAID). Jede pastellgelbe 15-mg-MOBIC-Tablette enthält 7,5 mg oder 15 mg Meloxicam zur oralen Verabreichung. Meloxicam wird chemisch als 4-Hydroxy-2-methyl-N-(5methyl2thiazolyl)-2H-1,2-benzothiazin-3-carboxamid-1,1-dioxid bezeichnet. Das Molekulargewicht beträgt 351,4. Seine empirische Formel ist C14H13N3O4S2 und es hat die folgende Strukturformel:
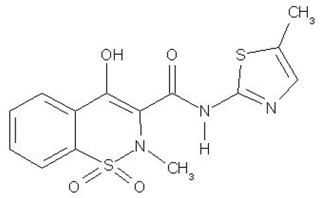
Meloxicam ist ein pastellgelber Feststoff, praktisch unlöslich in Wasser, wobei eine höhere Löslichkeit in starken Säuren und Basen beobachtet wird. Es ist sehr wenig löslich in Methanol. Meloxicam hat einen scheinbaren Verteilungskoeffizienten (log P)app = 0,1 in n-Octanol/Puffer pH 7,4. Meloxicam hat pKa-Werte von 1,1 und 4,2.
MOBIC 15 mg ist als Tablette zur oralen Verabreichung mit 7,5 mg oder 15 mg Meloxicam erhältlich.
Zu den inaktiven Bestandteilen in MOBIC 15 mg Tabletten gehören kolloidales Siliciumdioxid, Crospovidon, Lactose-Monohydrat, Magnesiumstearat, mikrokristalline Cellulose, Povidon und Natriumcitrat-Dihydrat.
INDIKATIONEN
Arthrose (OA)
MOBIC ist angezeigt zur Linderung der Anzeichen und Symptome von Arthrose [siehe Klinische Studien
Rheumatoide Arthritis (RA)
MOBIC ist angezeigt zur Linderung der Anzeichen und Symptome der rheumatoiden Arthritis [siehe Klinische Studien ].
Juvenile rheumatoide Arthritis (JRA) pauziartikulärer und polyartikulärer Verlauf
MOBIC 7,5 mg ist indiziert zur Linderung der Anzeichen und Symptome einer pauziartikulären oder polyartikulären juvenilen rheumatoiden Arthritis bei Patienten, die ≥ 60 kg wiegen [siehe DOSIERUNG UND ANWENDUNG und Klinische Studien ].
DOSIERUNG UND ANWENDUNG
Allgemeine Dosierungsanleitung
Wägen Sie die potenziellen Vorteile und Risiken von MOBIC und anderen Behandlungsoptionen sorgfältig ab, bevor Sie sich für die Anwendung von MOBIC entscheiden. Verwenden Sie die niedrigste wirksame Dosis für die kürzeste Dauer im Einklang mit den individuellen Behandlungszielen des Patienten [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Nachdem Sie das Ansprechen auf die Initialtherapie mit MOBIC beobachtet haben, passen Sie die Dosis an die individuellen Bedürfnisse des Patienten an.
Bei Erwachsenen beträgt die maximal empfohlene orale Tagesdosis von MOBIC 15 mg, unabhängig von der Formulierung. Bei Patienten mit Hämodialyse wird eine maximale Tagesdosis von 7,5 mg empfohlen [siehe Verwendung in bestimmten Bevölkerungsgruppen und KLINISCHE PHARMAKOLOGIE
MOBIC kann unabhängig vom Zeitpunkt der Mahlzeiten eingenommen werden.
Arthrose
Zur Linderung der Anzeichen und Symptome von Osteoarthritis beträgt die empfohlene orale Anfangs- und Erhaltungsdosis von MOBIC 7,5 mg einmal täglich. Bei manchen Patienten kann eine Erhöhung der Dosis auf 15 mg einmal täglich einen zusätzlichen Nutzen bringen.
Rheumatoide Arthritis
Zur Linderung der Anzeichen und Symptome der rheumatoiden Arthritis beträgt die empfohlene orale Anfangs- und Erhaltungsdosis von MOBIC 7,5 mg einmal täglich 7,5 mg. Bei manchen Patienten kann eine Erhöhung der Dosis auf 15 mg einmal täglich einen zusätzlichen Nutzen bringen.
Juvenile rheumatoide Arthritis (JRA) pauziartikulärer und polyartikulärer Verlauf
Für die Behandlung der juvenilen rheumatoiden Arthritis beträgt die empfohlene orale Dosis von MOBIC 7,5 mg 7,5 mg einmal täglich bei Kindern mit einem Gewicht von ≥ 60 kg. In klinischen Studien wurde kein zusätzlicher Nutzen durch eine Erhöhung der Dosis auf über 7,5 mg nachgewiesen.
MOBIC-Tabletten sollten bei Kindern mit einem Körpergewicht
Nierenfunktionsstörung
Die Anwendung von MOBIC 15 mg bei Patienten mit schwerer Nierenfunktionsstörung wird nicht empfohlen.
Bei Patienten unter Hämodialyse beträgt die maximale Dosis von MOBIC 7,5 mg pro Tag [siehe KLINISCHE PHARMAKOLOGIE ].
Nichtaustauschbarkeit mit anderen Formulierungen von Meloxicam
MOBIC-Tabletten haben keine gleichwertige systemische Exposition gegenüber anderen zugelassenen Formulierungen von oralem Meloxicam gezeigt. Daher sind MOBIC 7,5 mg Tabletten nicht mit anderen Formulierungen des oralen Meloxicam-Produkts austauschbar, selbst wenn die Gesamtstärke in Milligramm gleich ist. Ersetzen Sie ähnliche Dosisstärken von MOBIC 7,5 mg Tabletten nicht durch andere Formulierungen von oralen Meloxicam-Produkten.
WIE GELIEFERT
Darreichungsformen und Stärken
MOBIC (Meloxicam) Tabletten:
Lagerung und Handhabung
MOBISCH ist als pastellgelbe, runde, bikonvexe, unbeschichtete Tablette mit 7,5 mg Meloxicam oder als pastellgelbe, längliche, bikonvexe, unbeschichtete Tablette mit 15 mg Meloxicam erhältlich. Die 7,5-mg-Tablette ist auf der einen Seite mit dem Boehringer Ingelheim-Logo und auf der anderen Seite mit dem Buchstaben „M“ bedruckt. Die 15-mg-Tablette ist auf der einen Seite mit dem Tablettencode „15“ und auf der anderen Seite mit dem Buchstaben „M“ eingeprägt.
MOBIC (Meloxicam) Tabletten 7,5 mg: NDC 0597-0029-01; Flaschen zu 100
MOBIC (Meloxicam) Tabletten 15 mg: NDC 0597-0030-01; Flaschen zu 100
Lagerung
Bei 20 °C bis 25 °C (68 °F bis 77 °F) lagern; Exkursionen erlaubt bis 15°C bis 30°C (59°F bis 86°F) [siehe USP kontrollierte Raumtemperatur ]. Bewahren Sie MOBIC-Tabletten an einem trockenen Ort auf.
Geben Sie die Tabletten in einen dichten Behälter.
Bewahren Sie dieses und alle Medikamente außerhalb der Reichweite von Kindern auf.
Vertrieb durch: Boehringer Ingelheim Pharmaceuticals, Inc. Ridgefield, CT 06877 USA. Überarbeitet: April 2021
NEBENWIRKUNGEN
Die folgenden Nebenwirkungen werden in anderen Abschnitten der Kennzeichnung ausführlicher erörtert:
Erfahrung mit klinischen Studien
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in den klinischen Studien zu einem Medikament beobachteten Nebenwirkungsraten nicht direkt mit den Raten in den klinischen Studien zu einem anderen Medikament verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Erwachsene
Arthrose und rheumatoide Arthritis
Die Datenbank der klinischen Phase-2/3-Studien von MOBIC umfasst 10.122 OA-Patienten und 1012 RA-Patienten, die mit MOBIC 7,5 mg/Tag behandelt wurden, 3505 OA-Patienten und 1351 RA-Patienten, die mit MOBIC 15 mg/Tag behandelt wurden. MOBIC wurde in diesen Dosen 661 Patienten mindestens 6 Monate lang und 312 Patienten mindestens ein Jahr lang verabreicht. Ungefähr 10.500 dieser Patienten wurden in zehn placebo- und/oder wirkstoffkontrollierten Osteoarthritis-Studien behandelt, und 2.363 dieser Patienten wurden in zehn placebo- und/oder wirkstoffkontrollierten Studien zur rheumatoiden Arthritis behandelt. Gastrointestinale (GI) unerwünschte Ereignisse waren die am häufigsten gemeldeten unerwünschten Ereignisse in allen Behandlungsgruppen in allen Studien mit MOBIC 15 mg.
Eine 12-wöchige multizentrische, doppelblinde, randomisierte Studie wurde bei Patienten mit Arthrose des Knies oder der Hüfte durchgeführt, um die Wirksamkeit und Sicherheit von MOBIC 7,5 mg mit Placebo und mit einer aktiven Kontrolle zu vergleichen. Zwei 12-wöchige multizentrische, doppelblinde, randomisierte Studien wurden bei Patienten mit rheumatoider Arthritis durchgeführt, um die Wirksamkeit und Sicherheit von MOBIC mit Placebo zu vergleichen.
Tabelle 1a zeigt Nebenwirkungen, die bei ≥ 2 % der MOBIC-Behandlungsgruppen in einer 12-wöchigen placebo- und aktivkontrollierten Arthrosestudie auftraten.
Tabelle 1b zeigt unerwünschte Ereignisse, die in zwei 12-wöchigen Placebo-kontrollierten Studien zu rheumatoider Arthritis bei ≥ 2 % der MOBIC-7,5-mg-Behandlungsgruppen auftraten.
Die Nebenwirkungen, die unter MOBIC 15 mg bei ≥ 2 % der Patienten auftraten, die kurzzeitig (4 bis 6 Wochen) und langfristig (6 Monate) in aktiv kontrollierten Osteoarthritis-Studien behandelt wurden, sind in Tabelle 2 aufgeführt.
Höhere Dosen von MOBIC (22,5 mg und mehr) wurden mit einem erhöhten Risiko für schwerwiegende gastrointestinale Ereignisse in Verbindung gebracht; Daher sollte die Tagesdosis von MOBIC 15 mg 15 mg nicht überschreiten.
Pädiatrie
Pauziartikulärer und polyartikulärer Verlauf Juvenile rheumatoide Arthritis (JRA)
387 Patienten mit JRA mit pauziartikulärem und polyartikulärem Verlauf wurden in drei klinischen Studien mit MOBIC 15 mg in Dosen von 0,125 bis 0,375 mg/kg pro Tag behandelt. Diese Studien bestanden aus zwei 12-wöchigen multizentrischen, doppelblinden, randomisierten Studien (eine mit einer 12-wöchigen unverblindeten Verlängerung und eine mit einer 40-wöchigen Verlängerung) und einer 1-jährigen unverblindeten PK-Studie. Die Nebenwirkungen, die in diesen pädiatrischen Studien mit MOBIC 15 mg beobachtet wurden, waren ihrer Art nach ähnlich wie in klinischen Studien mit Erwachsenen, obwohl es Unterschiede in der Häufigkeit gab. Insbesondere die folgenden häufigsten unerwünschten Ereignisse, Bauchschmerzen, Erbrechen, Durchfall, Kopfschmerzen und Fieber, traten in den Studien mit Kindern häufiger auf als in den Studien mit Erwachsenen. Ausschlag wurde bei sieben (
Die folgende Liste enthält unerwünschte Arzneimittelwirkungen, die bei
Körper als Ganzes: Allergische Reaktion, Gesichtsödem, Müdigkeit, Fieber, Hitzewallungen, Unwohlsein, Synkope, Gewichtsabnahme, Gewichtszunahme
Herz-Kreislauf: Angina pectoris, Herzinsuffizienz, Hypertonie, Hypotonie, Myokardinfarkt, Vaskulitis
Zentrales und peripheres Nervensystem: Krämpfe, Parästhesien, Zittern, Schwindel
Magen-Darm : Kolitis, Mundtrockenheit, Zwölffingerdarmgeschwür, Aufstoßen, Ösophagitis, Magengeschwür, Gastritis, gastroösophagealer Reflux, gastrointestinale Blutung, Hämatemesis, hämorrhagisches Zwölffingerdarmgeschwür, hämorrhagisches Magengeschwür, Darmperforation, Meläna, Pankreatitis, perforiertes Zwölffingerdarmgeschwür, perforiertes Magengeschwür, Stomatitis ulzerativ
Herzfrequenz und Rhythmus: Arrhythmie, Herzklopfen, Tachykardie
Hämatologisch : Leukopenie, Purpura, Thrombozytopenie
Leber und Gallensystem: ALT erhöht, AST erhöht, Bilirubinämie, GGT erhöht, Hepatitis
Stoffwechsel und Ernährung : Austrocknung
Psychiatrisch : anormales Träumen, Angst, gesteigerter Appetit, Verwirrtheit, Depression, Nervosität, Schläfrigkeit
Atmung : Asthma, Bronchospasmus, Dyspnoe
Haut und Anhängsel: Alopezie, Angioödem, bullöser Hautausschlag, Lichtempfindlichkeitsreaktion, Juckreiz, vermehrtes Schwitzen, Urtikaria
Besondere Sinne: Sehstörungen, Konjunktivitis, Geschmacksstörungen, Tinnitus
Harnsystem: Albuminurie, BUN erhöht, Kreatinin erhöht, Hämaturie, Nierenversagen
Postmarketing-Erfahrung
Die folgenden Nebenwirkungen wurden während der Anwendung von MOBIC nach der Zulassung festgestellt. Da diese Reaktionen freiwillig aus einer Population unbekannter Größe gemeldet werden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder einen kausalen Zusammenhang mit der Arzneimittelexposition herzustellen. Entscheidungen darüber, ob ein unerwünschtes Ereignis aus Spontanmeldungen in die Kennzeichnung aufgenommen werden soll, basieren typischerweise auf einem oder mehreren der folgenden Faktoren: (1) Schwere des Ereignisses, (2) Anzahl der Meldungen oder (3) Stärke des kausalen Zusammenhangs mit dem Arzneimittel. Zu den Nebenwirkungen, die weltweit nach Markteinführung oder in der Literatur berichtet wurden, gehören: akuter Harnverhalt; Agranulozytose; Stimmungsschwankungen (z. B. Stimmungsaufhellung); anaphylaktoide Reaktionen einschließlich Schock; Erythema multiforme; exfoliative Dermatitis; interstitielle Nephritis; Gelbsucht; Leberversagen; Stevens-Johnson-Syndrom; toxische epidermale Nekrolyse und weibliche Unfruchtbarkeit.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Siehe Tabelle 3 für klinisch signifikante Arzneimittelwechselwirkungen mit Meloxicam. Siehe auch WARNUNGEN UND VORSICHTSMASSNAHMEN und KLINISCHE PHARMAKOLOGIE .
WARNUNGEN
Eingeschlossen als Teil der VORSICHTSMASSNAHMEN Sektion.
VORSICHTSMASSNAHMEN
Kardiovaskuläre thrombotische Ereignisse
Klinische Studien mit mehreren COX-2-selektiven und nicht-selektiven NSAIDs mit einer Dauer von bis zu drei Jahren haben ein erhöhtes Risiko für schwerwiegende kardiovaskuläre (CV) thrombotische Ereignisse, einschließlich Myokardinfarkt (MI) und Schlaganfall, die tödlich sein können, gezeigt. Basierend auf den verfügbaren Daten ist unklar, ob das Risiko für kardiovaskuläre thrombotische Ereignisse bei allen NSAIDs ähnlich ist. Der relative Anstieg schwerer kardiovaskulärer thrombotischer Ereignisse gegenüber dem Ausgangswert, der durch die Verwendung von NSAIDs hervorgerufen wird, scheint bei Patienten mit und ohne bekannte kardiovaskuläre Erkrankung oder Risikofaktoren für kardiovaskuläre Erkrankungen ähnlich zu sein. Allerdings hatten Patienten mit bekannter kardiovaskulärer Erkrankung oder Risikofaktoren aufgrund ihrer erhöhten Baseline-Rate eine höhere absolute Inzidenz von übermäßigen schwerwiegenden kardiovaskulären thrombotischen Ereignissen. Einige Beobachtungsstudien ergaben, dass dieses erhöhte Risiko für schwerwiegende kardiovaskuläre thrombotische Ereignisse bereits in den ersten Behandlungswochen einsetzte. Der Anstieg des kardiovaskulären Thromboserisikos wurde am konsistentesten bei höheren Dosen beobachtet.
Um das potenzielle Risiko eines unerwünschten kardiovaskulären Ereignisses bei NSAID-behandelten Patienten zu minimieren, verwenden Sie die niedrigste wirksame Dosis für die kürzestmögliche Dauer. Ärzte und Patienten sollten während des gesamten Behandlungsverlaufs auf die Entwicklung solcher Ereignisse achten, auch wenn zuvor keine kardiovaskulären Symptome aufgetreten sind. Die Patienten sollten über die Symptome schwerwiegender kardiovaskulärer Ereignisse und die zu ergreifenden Maßnahmen informiert werden, wenn sie auftreten.
Es gibt keine konsistenten Beweise dafür, dass die gleichzeitige Anwendung von Aspirin das erhöhte Risiko schwerer kardiovaskulärer thrombotischer Ereignisse im Zusammenhang mit der Anwendung von NSAR mindert. Die gleichzeitige Anwendung von Aspirin und einem NSAID wie Meloxicam erhöht das Risiko schwerwiegender gastrointestinaler (GI) Ereignisse [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Status nach Koronararterien-Bypass-Operation (CABG).
Zwei große, kontrollierte klinische Studien mit einem COX-2-selektiven NSAID zur Behandlung von Schmerzen in den ersten 10–14 Tagen nach einer CABG-Operation ergaben eine erhöhte Inzidenz von Myokardinfarkt und Schlaganfall. NSAIDs sind bei CABG kontraindiziert [vgl KONTRAINDIKATIONEN ].
Post-MI-Patienten
Beobachtungsstudien, die im dänischen Nationalregister durchgeführt wurden, haben gezeigt, dass Patienten, die mit NSAIDs in der Zeit nach einem Myokardinfarkt behandelt wurden, ab der ersten Behandlungswoche ein erhöhtes Risiko für einen Reinfarkt, einen kardiovaskulären Tod und eine Gesamtmortalität hatten. In derselben Kohorte betrug die Inzidenz von Todesfällen im ersten Jahr nach MI 20 pro 100 Personenjahre bei NSAID-behandelten Patienten im Vergleich zu 12 pro 100 Personenjahre bei nicht-NSAID-exponierten Patienten. Obwohl die absolute Todesrate nach dem ersten Jahr nach dem Myokardinfarkt etwas zurückging, blieb das erhöhte relative Todesrisiko bei NSAID-Anwendern mindestens über die nächsten vier Jahre der Nachbeobachtung bestehen.
Vermeiden Sie die Anwendung von MOBIC 15 mg bei Patienten mit kürzlich erlittenem Herzinfarkt, es sei denn, der Nutzen überwiegt voraussichtlich das Risiko wiederkehrender kardiovaskulärer thrombotischer Ereignisse. Wenn MOBIC 15 mg bei Patienten mit kürzlich aufgetretenem MI angewendet wird, müssen die Patienten auf Anzeichen einer kardialen Ischämie überwacht werden.
Magen-Darm-Blutungen, Ulzerationen und Perforationen
NSAIDs, einschließlich Meloxicam, können schwerwiegende Nebenwirkungen im Magen-Darm-Trakt (GI) verursachen, darunter Entzündungen, Blutungen, Geschwüre und Perforationen der Speiseröhre, des Magens, des Dünndarms oder des Dickdarms, die tödlich sein können. Diese schwerwiegenden unerwünschten Ereignisse können jederzeit mit oder ohne Warnsymptome bei Patienten auftreten, die mit NSAIDs behandelt werden. Nur jeder fünfte Patient, der unter NSAID-Therapie ein schwerwiegendes unerwünschtes Ereignis im oberen Gastrointestinaltrakt entwickelt, ist symptomatisch. Geschwüre im oberen Gastrointestinaltrakt, starke Blutungen oder Perforationen, die durch NSAIDs verursacht wurden, traten bei etwa 1 % der Patienten auf, die 3 bis 6 Monate behandelt wurden, und bei etwa 2 % bis 4 % der Patienten, die ein Jahr behandelt wurden. Allerdings ist auch eine kurzzeitige NSAID-Therapie nicht ohne Risiko.
Risikofaktoren für GI-Blutungen, Ulzerationen und Perforationen
Patienten mit Magengeschwüren und/oder gastrointestinalen Blutungen in der Vorgeschichte, die NSAR einnahmen, hatten ein mehr als 10-fach erhöhtes Risiko für die Entwicklung einer gastrointestinalen Blutung im Vergleich zu Patienten ohne diese Risikofaktoren. Andere Faktoren, die das Risiko von GI-Blutungen bei mit NSAIDs behandelten Patienten erhöhen, umfassen eine längere Dauer der NSAID-Therapie; gleichzeitige Anwendung von oralen Kortikosteroiden, Aspirin, Antikoagulanzien oder selektiven Serotonin-Wiederaufnahmehemmern (SSRIs); Rauchen; Alkoholkonsum; älteres Alter; und schlechter allgemeiner Gesundheitszustand. Die meisten Postmarketing-Berichte über tödliche gastrointestinale Ereignisse traten bei älteren oder geschwächten Patienten auf. Darüber hinaus besteht bei Patienten mit fortgeschrittener Lebererkrankung und/oder Koagulopathie ein erhöhtes Risiko für gastrointestinale Blutungen.
Strategien zur Minimierung der GI-Risiken bei NSAID-behandelten Patienten
Hepatotoxizität
Erhöhungen von ALT oder AST (mindestens das Dreifache der oberen Normgrenze [ULN]) wurden in klinischen Studien bei etwa 1 % der mit NSAR behandelten Patienten berichtet. Darüber hinaus wurden seltene, manchmal tödliche Fälle von schwerer Leberschädigung, einschließlich fulminanter Hepatitis, Lebernekrose und Leberversagen, berichtet.
Erhöhungen von ALT oder AST (weniger als das Dreifache des ULN) können bei bis zu 15 % der mit NSAIDs einschließlich Meloxicam behandelten Patienten auftreten.
Informieren Sie die Patienten über die Warnzeichen und Symptome einer Hepatotoxizität (z. B. Übelkeit, Müdigkeit, Lethargie, Durchfall, Juckreiz, Gelbsucht, Druckschmerz im rechten oberen Quadranten und „grippeähnliche“ Symptome). Wenn sich klinische Anzeichen und Symptome entwickeln, die einer Lebererkrankung entsprechen, oder wenn systemische Manifestationen auftreten (z. B. Eosinophilie, Hautausschlag usw.), setzen Sie MOBIC sofort ab und führen Sie eine klinische Untersuchung des Patienten durch [siehe Verwendung in bestimmten Bevölkerungsgruppen und KLINISCHE PHARMAKOLOGIE ].
Hypertonie
NSAIDs, einschließlich MOBIC, können zu einem erneuten Auftreten oder einer Verschlechterung einer vorbestehenden Hypertonie führen, die beide zu einer erhöhten Inzidenz von kardiovaskulären Ereignissen beitragen können. Patienten, die Angiotensin-Converting-Enzyme (ACE)-Hemmer, Thiaziddiuretika oder Schleifendiuretika einnehmen, können bei der Einnahme von NSAIDs ein beeinträchtigtes Ansprechen auf diese Therapien haben [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Überwachen Sie den Blutdruck (BP) zu Beginn der NSAID-Behandlung und während des gesamten Therapieverlaufs.
Herzinsuffizienz und Ödem
Die Coxib and Traditional NSAID Trialists' Collaboration Meta-Analyse randomisierter kontrollierter Studien zeigte eine ungefähr zweifache Zunahme der Krankenhauseinweisungen wegen Herzinsuffizienz bei COX-2-selektiv behandelten Patienten und nicht-selektiv NSAID-behandelten Patienten im Vergleich zu Placebo-behandelten Patienten. In einer Studie des Dänischen Nationalen Registers bei Patienten mit Herzinsuffizienz erhöhte die Verwendung von NSAID das Risiko für Herzinfarkt, Krankenhauseinweisung wegen Herzinsuffizienz und Tod.
Darüber hinaus wurden bei einigen Patienten, die mit NSAIDs behandelt wurden, Flüssigkeitsretention und Ödeme beobachtet. Die Anwendung von Meloxicam kann die kardiovaskulären Wirkungen mehrerer Therapeutika abschwächen, die zur Behandlung dieser Erkrankungen eingesetzt werden (z. B. Diuretika, ACE-Hemmer oder Angiotensin-Rezeptorblocker [ARBs]) [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Vermeiden Sie die Anwendung von MOBIC 15 mg bei Patienten mit schwerer Herzinsuffizienz, es sei denn, der Nutzen überwiegt voraussichtlich das Risiko einer Verschlechterung der Herzinsuffizienz. Wenn MOBIC bei Patienten mit schwerer Herzinsuffizienz angewendet wird, überwachen Sie die Patienten auf Anzeichen einer Verschlechterung der Herzinsuffizienz.
Nierentoxizität und Hyperkaliämie
Nierentoxizität
Die langfristige Verabreichung von NSAIDs, einschließlich MOBIC, hat zu Nierenpapillennekrose, Niereninsuffizienz, akutem Nierenversagen und anderen Nierenschäden geführt.
Nierentoxizität wurde auch bei Patienten beobachtet, bei denen renale Prostaglandine eine kompensatorische Rolle bei der Aufrechterhaltung der Nierendurchblutung spielen. Bei diesen Patienten kann die Verabreichung eines NSAID eine dosisabhängige Verringerung der Prostaglandinbildung und sekundär des renalen Blutflusses verursachen, was eine offenkundige Nierendekompensation auslösen kann. Patienten mit dem größten Risiko für diese Reaktion sind Patienten mit eingeschränkter Nierenfunktion, Dehydratation, Hypovolämie, Herzinsuffizienz, Leberfunktionsstörungen, Patienten, die Diuretika und ACE-Hemmer oder ARBs einnehmen, sowie ältere Menschen. Auf das Absetzen der NSAID-Therapie folgt normalerweise die Wiederherstellung des Zustands vor der Behandlung.
Die renalen Wirkungen von MOBIC können das Fortschreiten der Nierenfunktionsstörung bei Patienten mit vorbestehender Nierenerkrankung beschleunigen. Da einige MOBIC-Metaboliten über die Nieren ausgeschieden werden, sind die Patienten auf Anzeichen einer Verschlechterung der Nierenfunktion zu überwachen.
Korrigieren Sie den Volumenstatus bei dehydrierten oder hypovolämischen Patienten vor der Einleitung von MOBIC. Überwachen Sie die Nierenfunktion bei Patienten mit eingeschränkter Nieren- oder Leberfunktion, Herzinsuffizienz, Dehydratation oder Hypovolämie während der Anwendung von MOBIC [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Aus kontrollierten klinischen Studien liegen keine Informationen zur Anwendung von MOBIC 15 mg bei Patienten mit fortgeschrittener Nierenerkrankung vor. Vermeiden Sie die Anwendung von MOBIC 7,5 mg bei Patienten mit fortgeschrittener Nierenerkrankung, es sei denn, der Nutzen überwiegt voraussichtlich das Risiko einer Verschlechterung der Nierenfunktion. Wenn MOBIC bei Patienten mit fortgeschrittener Nierenerkrankung angewendet wird, überwachen Sie die Patienten auf Anzeichen einer Verschlechterung der Nierenfunktion [siehe KLINISCHE PHARMAKOLOGIE ].
Hyperkaliämie
Bei der Anwendung von NSAIDs wurde sogar bei einigen Patienten ohne Nierenfunktionsstörung über Anstiege der Serumkaliumkonzentration, einschließlich Hyperkaliämie, berichtet. Bei Patienten mit normaler Nierenfunktion wurden diese Wirkungen einem hyporeninämischen Hypoaldosteronismus-Zustand zugeschrieben.
Anaphylaktische Reaktionen
Meloxicam wurde mit anaphylaktischen Reaktionen bei Patienten mit und ohne bekannte Überempfindlichkeit gegen Meloxicam und bei Patienten mit Aspirin-empfindlichem Asthma in Verbindung gebracht [siehe KONTRAINDIKATIONEN und WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Suchen Sie Nothilfe auf, wenn eine anaphylaktische Reaktion auftritt.
Verschlimmerung von Asthma im Zusammenhang mit Aspirin-Empfindlichkeit
Eine Subpopulation von Patienten mit Asthma kann Aspirin-empfindliches Asthma haben, das eine durch Nasenpolypen komplizierte chronische Rhinosinusitis umfassen kann; schwerer, möglicherweise tödlicher Bronchospasmus; und/oder Intoleranz gegenüber Aspirin und anderen NSAIDs. Da bei solchen Aspirin-empfindlichen Patienten über Kreuzreaktivität zwischen Aspirin und anderen NSAIDs berichtet wurde, ist MOBIC bei Patienten mit dieser Form der Aspirin-Empfindlichkeit kontraindiziert [siehe KONTRAINDIKATIONEN ]. Wenn MOBIC 15 mg bei Patienten mit vorbestehendem Asthma (ohne bekannte Aspirin-Empfindlichkeit) angewendet wird, müssen die Patienten auf Veränderungen der Anzeichen und Symptome von Asthma überwacht werden.
Schwerwiegende Hautreaktionen
NSAIDs, einschließlich Meloxicam, können schwerwiegende Nebenwirkungen der Haut wie exfoliative Dermatitis, Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN) verursachen, die tödlich sein können. Diese schwerwiegenden Ereignisse können ohne Vorwarnung eintreten. Informieren Sie die Patienten über die Anzeichen und Symptome schwerwiegender Hautreaktionen und brechen Sie die Anwendung von MOBIC beim ersten Auftreten von Hautausschlag oder anderen Anzeichen einer Überempfindlichkeit ab. MOBIC ist kontraindiziert bei Patienten mit früheren schwerwiegenden Hautreaktionen auf NSAIDs [siehe KONTRAINDIKATIONEN ].
Arzneimittelreaktion mit Eosinophilie und systemischen Symptomen (DRESS)
Arzneimittelreaktionen mit Eosinophilie und systemischen Symptomen (DRESS) wurden bei Patienten berichtet, die NSAIDs wie MOBIC einnahmen. Einige dieser Ereignisse waren tödlich oder lebensbedrohlich. DRESS zeigt sich typischerweise, wenn auch nicht ausschließlich, durch Fieber, Hautausschlag, Lymphadenopathie und/oder Gesichtsschwellungen. Andere klinische Manifestationen können Hepatitis, Nephritis, hämatologische Anomalien, Myokarditis oder Myositis umfassen. Manchmal ähneln die Symptome von DRESS einer akuten Virusinfektion. Eosinophilie ist oft vorhanden. Da diese Störung in ihrem Erscheinungsbild variabel ist, können andere Organsysteme, die hier nicht aufgeführt sind, beteiligt sein. Es ist wichtig zu beachten, dass frühe Manifestationen einer Überempfindlichkeit, wie Fieber oder Lymphadenopathie, vorhanden sein können, auch wenn kein Hautausschlag erkennbar ist. Wenn solche Anzeichen oder Symptome vorhanden sind, brechen Sie MOBIC ab und untersuchen Sie den Patienten sofort.
Fötale Toxizität
Vorzeitiger Verschluss des fötalen Ductus Arteriosus
Vermeiden Sie die Anwendung von NSAIDs, einschließlich MOBIC, bei schwangeren Frauen ab der 30. Schwangerschaftswoche und später. NSAIDs, einschließlich MOBIC, erhöhen das Risiko eines vorzeitigen Verschlusses des fetalen Ductus arteriosus etwa in diesem Gestationsalter.
Oligohydramnion/Niereninsuffizienz bei Neugeborenen
Die Anwendung von NSAIDs, einschließlich MOBIC 15 mg, in der 20. Schwangerschaftswoche oder später in der Schwangerschaft kann zu einer fetalen Nierenfunktionsstörung führen, die zu Oligohydramnion und in einigen Fällen zu einer Nierenfunktionsstörung beim Neugeborenen führt. Diese Nebenwirkungen werden im Durchschnitt nach Tagen bis Wochen der Behandlung beobachtet, obwohl Oligohydramnion selten schon 48 Stunden nach Beginn der Behandlung mit NSAR berichtet wurde. Oligohydramnion ist oft, aber nicht immer, nach Absetzen der Behandlung reversibel. Zu den Komplikationen eines verlängerten Oligohydramnion können beispielsweise Extremitätenkontrakturen und eine verzögerte Lungenreifung gehören. In einigen Postmarketing-Fällen mit eingeschränkter Nierenfunktion bei Neugeborenen waren invasive Verfahren wie Austauschtransfusionen oder Dialyse erforderlich.
Wenn eine NSAID-Behandlung zwischen etwa der 20. und 30. Schwangerschaftswoche erforderlich ist, beschränken Sie die Anwendung von MOBIC auf die niedrigste wirksame Dosis und die kürzestmögliche Dauer. Erwägen Sie eine Ultraschallüberwachung des Fruchtwassers, wenn die Behandlung mit MOBIC 15 mg länger als 48 Stunden dauert. Setzen Sie MOBIC 15 mg ab, wenn Oligohydramnion auftritt, und folgen Sie der klinischen Praxis entsprechend [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
Hämatologische Toxizität
Anämie ist bei NSAID-behandelten Patienten aufgetreten. Dies kann auf okkulten oder groben Blutverlust, Flüssigkeitsretention oder eine unvollständig beschriebene Wirkung auf die Erythropoese zurückzuführen sein. Wenn bei einem mit MOBIC behandelten Patienten Anzeichen oder Symptome einer Anämie auftreten, sollten Hämoglobin oder Hämatokrit überwacht werden.
NSAIDs, einschließlich MOBIC 7,5 mg, können das Risiko von Blutungsereignissen erhöhen. Begleiterkrankungen wie Gerinnungsstörungen oder die gleichzeitige Anwendung von Warfarin, anderen Antikoagulanzien, Thrombozytenaggregationshemmern (z. B. Aspirin), Serotonin-Wiederaufnahmehemmern (SSRIs) und Serotonin-Noradrenalin-Wiederaufnahmehemmern (SNRIs) können dieses Risiko erhöhen. Überwachen Sie diese Patienten auf Anzeichen von Blutungen [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Maskierung von Entzündungen und Fieber
Die pharmakologische Aktivität von MOBIC 15 mg bei der Reduzierung von Entzündungen und möglicherweise Fieber kann den Nutzen diagnostischer Zeichen beim Nachweis von Infektionen verringern.
Laborüberwachung
Da schwere Magen-Darm-Blutungen, Hepatotoxizität und Nierenschäden ohne Warnsymptome oder -zeichen auftreten können, erwägen Sie eine regelmäßige Überwachung von Patienten unter NSAID-Langzeitbehandlung mit einem Blutbild und einem chemischen Profil [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Informationen zur Patientenberatung
Weisen Sie den Patienten an, die von der FDA zugelassene Patientenkennzeichnung ( Leitfaden für Medikamente ), die jeder ausgestellten Verschreibung beiliegt.
Informieren Sie Patienten, Familien oder ihre Betreuer über die folgenden Informationen, bevor Sie eine Therapie mit einem NSAID beginnen, und regelmäßig während der laufenden Therapie.
Kardiovaskuläre thrombotische Ereignisse
Weisen Sie die Patienten an, auf die Symptome kardiovaskulärer thrombotischer Ereignisse, einschließlich Schmerzen in der Brust, Kurzatmigkeit, Schwäche oder undeutliche Sprache, zu achten und jedes dieser Symptome unverzüglich ihrem medizinischen Betreuer zu melden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Magen-Darm-Blutungen, Ulzerationen und Perforationen
Raten Sie den Patienten, ihre Symptome von Ulzerationen und Blutungen, einschließlich Oberbauchschmerzen, Dyspepsie, Meläna und Hämatemesis, ihrem medizinischen Betreuer zu melden. Informieren Sie die Patienten bei gleichzeitiger Anwendung von niedrig dosiertem Aspirin zur Herzprophylaxe über das erhöhte Risiko für die Anzeichen und Symptome einer gastrointestinalen Blutung [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Hepatotoxizität
Informieren Sie die Patienten über die Warnzeichen und Symptome einer Hepatotoxizität (z. B. Übelkeit, Müdigkeit, Lethargie, Durchfall, Juckreiz, Gelbsucht, Druckschmerz im rechten oberen Quadranten und „grippeähnliche“ Symptome). Wenn diese auftreten, weisen Sie die Patienten an, MOBIC 7,5 mg abzusetzen und sich sofort medizinisch behandeln zu lassen [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Herzinsuffizienz und Ödem
Weisen Sie die Patienten an, auf die Symptome einer dekompensierten Herzinsuffizienz, einschließlich Kurzatmigkeit, unerklärliche Gewichtszunahme oder Ödeme, aufmerksam zu sein und sich an ihren Arzt zu wenden, wenn solche Symptome auftreten [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Anaphylaktische Reaktionen
Informieren Sie die Patienten über die Anzeichen einer anaphylaktischen Reaktion (z. B. Atembeschwerden, Schwellungen im Gesicht oder Rachen). Weisen Sie die Patienten an, sofort Nothilfe zu suchen, wenn diese auftreten [siehe KONTRAINDIKATIONEN und WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Schwerwiegende Hautreaktionen, einschließlich DRESS
Weisen Sie die Patienten an, die Einnahme von MOBIC sofort abzubrechen, wenn sie irgendeine Art von Hautausschlag oder Fieber entwickeln, und sich so schnell wie möglich an ihren Arzt zu wenden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Weibliche Fruchtbarkeit
Weisen Sie Frauen im gebärfähigen Alter, die eine Schwangerschaft wünschen, darauf hin, dass NSAIDs, einschließlich MOBIC 7,5 mg, mit einer reversiblen Verzögerung des Eisprungs verbunden sein können [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
Fötale Toxizität
Informieren Sie schwangere Frauen, dass sie die Anwendung von MOBIC 15 mg und anderen NSAIDs ab der 30. Schwangerschaftswoche wegen des Risikos eines vorzeitigen Verschlusses des fetalen Ductus arteriosus vermeiden sollten. Wenn eine Behandlung mit MOBIC 15 mg für eine schwangere Frau zwischen der 20. und 30. Schwangerschaftswoche erforderlich ist, weisen Sie sie darauf hin, dass sie möglicherweise auf Oligohydramnion überwacht werden muss, wenn die Behandlung länger als 48 Stunden andauert [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und Verwendung in bestimmten Bevölkerungsgruppen ].
Vermeiden Sie die gleichzeitige Anwendung von NSAIDs
Informieren Sie die Patienten darüber, dass die gleichzeitige Anwendung von MOBIC 15 mg mit anderen NSAIDs oder Salicylaten (z. B. Diflunisal, Salsalat) aufgrund des erhöhten Risikos einer gastrointestinalen Toxizität und einer geringen oder keinen Steigerung der Wirksamkeit nicht empfohlen wird [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ]. Weisen Sie die Patienten darauf hin, dass NSAIDs in „rezeptfreien“ Medikamenten zur Behandlung von Erkältungen, Fieber oder Schlaflosigkeit enthalten sein können.
Verwendung von NSAIDs und niedrig dosiertem Aspirin
Weisen Sie die Patienten darauf hin, kein niedrig dosiertes Aspirin gleichzeitig mit MOBIC 7,5 mg anzuwenden, bis sie mit ihrem Arzt gesprochen haben [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Für aktuelle Verschreibungsinformationen scannen Sie den Code oder rufen Sie Boehringer Ingelheim Pharmaceuticals, Inc. unter 1-800-542-6257 an.
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Karzinogenese
In Langzeit-Karzinogenitätsstudien an Ratten (104 Wochen) und Mäusen (99 Wochen), denen Meloxicam in oralen Dosen von bis zu 0,8 mg/kg/Tag bei Ratten und bis zu 8,0 mg/kg/Tag in verabreicht wurde, gab es keinen Anstieg der Tumorinzidenz Mäuse (bis zum 0,5- bzw. 2,6-Fachen der maximal empfohlenen Dosis beim Menschen [MRHD] von 15 mg/Tag MOBIC 7,5 mg, basierend auf dem Vergleich der Körperoberfläche [KOF]).
Mutagenese
Meloxicam war in einem Ames-Assay nicht mutagen und in einem Chromosomenaberrationsassay mit humanen Lymphozyten und einem In-vivo-Mikrokerntest im Knochenmark von Mäusen nicht klastogen.
Beeinträchtigung der Fruchtbarkeit
Meloxicam beeinträchtigte die männliche und weibliche Fertilität bei Ratten in oralen Dosen von bis zu 9 mg/kg/Tag bei Männchen und 5 mg/kg/Tag bei Weibchen (bis zu 5,8- bzw. 3,2-mal höher als die MRHD basierend auf BSA-Vergleich).
Verwendung in bestimmten Bevölkerungsgruppen
Schwangerschaft
Zusammenfassung der Risiken
Die Anwendung von NSAIDs, einschließlich MOBIC, kann einen vorzeitigen Verschluss des fetalen Ductus arteriosus und eine fetale Nierenfunktionsstörung verursachen, die zu Oligohydramnion und in einigen Fällen zu einer Nierenfunktionsstörung bei Neugeborenen führt. Begrenzen Sie aufgrund dieser Risiken die Dosis und Dauer der MOBIC-Anwendung auf etwa die 20. bis 30. Schwangerschaftswoche und vermeiden Sie die MOBIC-Anwendung in der 30. Schwangerschaftswoche und später in der Schwangerschaft (siehe Klinische Überlegungen , Daten ).
Vorzeitiger Verschluss des fötalen Ductus Arteriosus
Die Anwendung von NSAIDs, einschließlich MOBIC 15 mg, etwa in der 30. Schwangerschaftswoche oder später in der Schwangerschaft erhöht das Risiko eines vorzeitigen Verschlusses des fetalen Ductus arteriosus.
Oligohydramnion/Niereninsuffizienz bei Neugeborenen
Die Anwendung von NSAIDs in der 20. Schwangerschaftswoche oder später in der Schwangerschaft wurde mit Fällen von fetaler Nierenfunktionsstörung in Verbindung gebracht, die zu Oligohydramnion und in einigen Fällen zu Nierenfunktionsstörungen bei Neugeborenen führte.
Daten aus Beobachtungsstudien zu potenziellen embryofetalen Risiken der NSAID-Anwendung bei Frauen im ersten oder zweiten Trimenon der Schwangerschaft sind nicht schlüssig.
In Reproduktionsstudien an Tieren wurde embryofötaler Tod bei Ratten und Kaninchen beobachtet, die während der Organogenese mit Meloxicam in oralen Dosen behandelt wurden, die dem 0,65- und 6,5-Fachen der maximal empfohlenen Humandosis (MRHD) von MOBIC entsprachen. Bei Kaninchen, die während der gesamten Embryogenese mit Meloxicam in einer oralen Dosis behandelt wurden, die dem 78-fachen der MRHD entsprach, wurde eine erhöhte Inzidenz von septalen Herzfehlern beobachtet. In prä- und postnatalen Reproduktionsstudien gab es bei der 0,08-fachen MRHD von Meloxicam eine erhöhte Inzidenz von Dystokie, verzögerter Geburt und verringerter Überlebensrate der Nachkommen. Bei Ratten und Kaninchen, die während der Organogenese mit Meloxicam in einer oralen Dosis entsprechend dem 2,6- und 26-fachen der MRHD behandelt wurden, wurden keine teratogenen Wirkungen beobachtet [vgl Daten ].
Basierend auf Tierdaten wurde gezeigt, dass Prostaglandine eine wichtige Rolle bei der Gefäßpermeabilität des Endometriums, der Blastozystenimplantation und der Dezidualisierung spielen. In Tierversuchen führte die Verabreichung von Prostaglandinsynthesehemmern wie Meloxicam zu einem erhöhten Prä- und Postimplantationsverlust. Es wurde auch gezeigt, dass Prostaglandine eine wichtige Rolle bei der fötalen Nierenentwicklung spielen. In veröffentlichten Tierstudien wurde berichtet, dass Prostaglandinsynthesehemmer die Nierenentwicklung beeinträchtigen, wenn sie in klinisch relevanten Dosen verabreicht werden.
Das geschätzte Hintergrundrisiko schwerer Geburtsfehler und Fehlgeburten für die angegebene(n) Population(en) ist unbekannt. Alle Schwangerschaften haben ein Hintergrundrisiko für Geburtsfehler, Verlust oder andere nachteilige Folgen. In der US-Allgemeinbevölkerung liegt das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten bei klinisch erkannten Schwangerschaften bei 2 % bis 4 % bzw. 15 % bis 20 %.
Klinische Überlegungen
Fetale/neonatale Nebenwirkungen
Vorzeitiger Verschluss des fötalen Ductus Arteriosus
Vermeiden Sie die Anwendung von NSAIDs bei Frauen in der 30. Schwangerschaftswoche und später in der Schwangerschaft, da NSAIDs, einschließlich MOBIC 7,5 mg, einen vorzeitigen Verschluss des fetalen Ductus arteriosus verursachen können (siehe Daten ).
Oligohydramnion/Niereninsuffizienz bei Neugeborenen
Wenn ein NSAID etwa in der 20. Schwangerschaftswoche oder später in der Schwangerschaft erforderlich ist, beschränken Sie die Anwendung auf die niedrigste wirksame Dosis und die kürzestmögliche Dauer. Wenn sich die Behandlung mit MOBIC 15 mg über 48 Stunden hinaus erstreckt, sollten Sie eine Überwachung mit Ultraschall auf Oligohydramnion in Betracht ziehen. Wenn Oligohydramnion auftritt, setzen Sie MOBIC 7,5 mg ab und folgen Sie der klinischen Praxis entsprechend (siehe Daten ).
Arbeit oder Lieferung
Es liegen keine Studien zu den Wirkungen von MOBIC 7,5 mg während der Wehen oder der Geburt vor. In Tierversuchen hemmen NSAIDs, einschließlich Meloxicam, die Prostaglandinsynthese, verursachen verzögerte Geburten und erhöhen die Häufigkeit von Totgeburten.
Daten
Menschliche Daten
Vorzeitiger Verschluss des fötalen Ductus Arteriosus
In der veröffentlichten Literatur wird berichtet, dass die Anwendung von NSAIDs etwa in der 30. Schwangerschaftswoche und später in der Schwangerschaft zu einem vorzeitigen Verschluss des fetalen Ductus arteriosus führen kann.
Oligohydramnion/Niereninsuffizienz bei Neugeborenen
Veröffentlichte Studien und Postmarketing-Berichte beschreiben die mütterliche NSAID-Nutzung etwa in der 20. Schwangerschaftswoche oder später in der Schwangerschaft im Zusammenhang mit fetaler Nierenfunktionsstörung, die zu Oligohydramnion und in einigen Fällen zu neonataler Nierenfunktionsstörung führt. Diese Nebenwirkungen werden im Durchschnitt nach Tagen bis Wochen der Behandlung beobachtet, obwohl Oligohydramnion selten schon 48 Stunden nach Beginn der Behandlung mit NSAR berichtet wurde. In vielen Fällen, aber nicht in allen Fällen, war die Abnahme des Fruchtwassers vorübergehend und nach Absetzen des Medikaments reversibel. Es gab eine begrenzte Anzahl von Fallberichten über die Anwendung von mütterlichen NSAIDs und neonatale Nierenfunktionsstörungen ohne Oligohydramnion, von denen einige irreversibel waren. Einige Fälle von Nierenfunktionsstörungen bei Neugeborenen erforderten eine Behandlung mit invasiven Verfahren wie Austauschtransfusionen oder Dialyse.
Zu den methodischen Einschränkungen dieser Postmarketing-Studien und -Berichte gehört das Fehlen einer Kontrollgruppe; begrenzte Informationen zu Dosis, Dauer und Zeitpunkt der Arzneimittelexposition; und gleichzeitiger Einnahme anderer Medikamente. Diese Einschränkungen schließen eine verlässliche Schätzung des Risikos unerwünschter fetaler und neonataler Folgen bei mütterlicher NSAID-Nutzung aus. Da die veröffentlichten Sicherheitsdaten zu Folgen bei Neugeborenen hauptsächlich Frühgeborene betrafen, ist die Verallgemeinerbarkeit bestimmter berichteter Risiken für termingeborene Säuglinge, die NSAIDs durch mütterliche Anwendung ausgesetzt waren, ungewiss.
Tierdaten
Meloxicam war nicht teratogen, wenn es trächtigen Ratten während der fötalen Organogenese in oralen Dosen von bis zu 4 mg/kg/Tag verabreicht wurde (2,6-mal höher als die MRHD von 15 mg MOBIC, basierend auf einem KOF-Vergleich). Die Verabreichung von Meloxicam an trächtige Kaninchen während der gesamten Embryogenese führte bei einer oralen Dosis von 60 mg/kg/Tag (78-fach höher als die MRHD, basierend auf BSA-Vergleich) zu einer erhöhten Inzidenz von Septumdefekten des Herzens. Die Nicht-Effekt-Konzentration betrug 20 mg/kg/Tag (26-mal höher als die MRHD, basierend auf der BSA-Umrechnung). Bei Ratten und Kaninchen trat Embryoletalität bei oralen Meloxicam-Dosen von 1 mg/kg/Tag bzw. 5 mg/kg/Tag auf (0,65- bzw. 6,5-fach größer als die MRHD basierend auf KOF-Vergleich), wenn sie während der gesamten Organogenese verabreicht wurden .
Die orale Verabreichung von Meloxicam an trächtige Ratten während der späten Trächtigkeit bis zur Laktation erhöhte die Inzidenz von Dystokie, verzögerter Geburt und verringerter Überlebensrate der Nachkommen bei Meloxicam-Dosen von 0,125 mg/kg/Tag oder mehr (0,08-fache MRHD basierend auf BSA-Vergleich).
Stillzeit
Zusammenfassung der Risiken
Es liegen keine Humandaten darüber vor, ob Meloxicam in der Muttermilch vorhanden ist, oder zu den Auswirkungen auf gestillte Säuglinge oder auf die Milchproduktion. Die Entwicklungs- und Gesundheitsvorteile des Stillens sollten zusammen mit dem klinischen Bedarf der Mutter an MOBIC und möglichen nachteiligen Auswirkungen auf den gestillten Säugling durch MOBIC 15 mg oder durch den zugrunde liegenden Zustand der Mutter berücksichtigt werden.
Daten
Tierdaten
Meloxicam war in der Milch laktierender Ratten in höheren Konzentrationen als im Plasma vorhanden.
Weibchen und Männchen mit reproduktivem Potenzial
Unfruchtbarkeit
Frauen
Basierend auf dem Wirkmechanismus kann die Anwendung von Prostaglandin-vermittelten NSAIDs, einschließlich MOBIC, das Reißen von Ovarialfollikeln verzögern oder verhindern, was bei einigen Frauen mit reversibler Unfruchtbarkeit in Verbindung gebracht wurde. Veröffentlichte Tierstudien haben gezeigt, dass die Verabreichung von Prostaglandinsynthesehemmern das Potenzial hat, die für den Eisprung erforderliche Prostaglandin-vermittelte Follikelruptur zu stören. Kleine Studien an Frauen, die mit NSAR behandelt wurden, haben auch eine reversible Verzögerung des Eisprungs gezeigt. Erwägen Sie das Absetzen von NSAIDs, einschließlich MOBIC, bei Frauen, die Schwierigkeiten haben, schwanger zu werden, oder die sich einer Untersuchung auf Unfruchtbarkeit unterziehen.
Pädiatrische Verwendung
Die Sicherheit und Wirksamkeit von Meloxicam bei pädiatrischen JRA-Patienten im Alter von 2 bis 17 Jahren wurde in drei klinischen Studien untersucht [siehe DOSIERUNG UND ANWENDUNG , NEBENWIRKUNGEN und Klinische Studien ].
Geriatrische Verwendung
Ältere Patienten haben im Vergleich zu jüngeren Patienten ein größeres Risiko für NSAID-assoziierte schwerwiegende kardiovaskuläre, gastrointestinale und/oder renale Nebenwirkungen. Wenn der erwartete Nutzen für den älteren Patienten diese potenziellen Risiken überwiegt, beginnen Sie mit der Dosierung am unteren Ende des Dosierungsbereichs und überwachen Sie die Patienten auf Nebenwirkungen [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Leberfunktionsstörung
Bei Patienten mit leichter bis mittelschwerer Leberfunktionsstörung ist keine Dosisanpassung erforderlich. Patienten mit schwerer Leberfunktionsstörung wurden nicht ausreichend untersucht. Da Meloxicam erheblich in der Leber metabolisiert wird und eine Hepatotoxizität auftreten kann, sollte Meloxicam bei Patienten mit eingeschränkter Leberfunktion mit Vorsicht angewendet werden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und KLINISCHE PHARMAKOLOGIE ].
Nierenfunktionsstörung
Bei Patienten mit leichter bis mittelschwerer Nierenfunktionsstörung ist keine Dosisanpassung erforderlich. Patienten mit schwerer Nierenfunktionsstörung wurden nicht untersucht. Die Anwendung von MOBIC 7,5 mg bei Patienten mit schwerer Nierenfunktionsstörung wird nicht empfohlen. Bei Patienten unter Hämodialyse sollte Meloxicam 7,5 mg pro Tag nicht überschreiten. Meloxicam ist nicht dialysierbar [vgl DOSIERUNG UND ANWENDUNG und KLINISCHE PHARMAKOLOGIE ].
ÜBERDOSIS
Die Symptome nach einer akuten NSAID-Überdosierung beschränkten sich typischerweise auf Lethargie, Benommenheit, Übelkeit, Erbrechen und epigastrische Schmerzen, die im Allgemeinen mit unterstützender Behandlung reversibel waren. Magen-Darm-Blutungen sind aufgetreten. Bluthochdruck, akutes Nierenversagen, Atemdepression und Koma sind aufgetreten, aber selten [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Behandeln Sie Patienten mit symptomatischer und unterstützender Behandlung nach einer NSAID-Überdosierung. Es gibt keine spezifischen Gegenmittel. Erwägen Sie Erbrechen und/oder Aktivkohle (60 bis 100 Gramm bei Erwachsenen, 1 bis 2 Gramm pro kg Körpergewicht bei pädiatrischen Patienten) und/oder osmotische Abführmittel bei symptomatischen Patienten, die innerhalb von vier Stunden nach der Einnahme beobachtet wurden, oder bei Patienten mit einer starken Überdosierung ( 5- bis 10-fache der empfohlenen Dosierung). Forcierte Diurese, Alkalisierung des Urins, Hämodialyse oder Hämoperfusion sind aufgrund der hohen Proteinbindung möglicherweise nicht sinnvoll.
Es liegen nur begrenzte Erfahrungen mit einer Meloxicam-Überdosierung vor. Von Cholestyramin ist bekannt, dass es die Clearance von Meloxicam beschleunigt. Eine beschleunigte Elimination von Meloxicam durch orale Gaben von 4 g Cholestyramin dreimal täglich wurde in einer klinischen Studie nachgewiesen. Die Gabe von Cholestyramin kann nach einer Überdosierung sinnvoll sein.
Wenden Sie sich für weitere Informationen zur Behandlung einer Überdosierung an eine Giftnotrufzentrale (1-800-222-1222).
KONTRAINDIKATIONEN
MOBIC 15 mg ist bei folgenden Patienten kontraindiziert:
KLINISCHE PHARMAKOLOGIE
Wirkmechanismus
Meloxicam hat analgetische, entzündungshemmende und fiebersenkende Eigenschaften.
Der Wirkungsmechanismus von MOBIC ist wie bei anderen NSAIDs noch nicht vollständig geklärt, beinhaltet jedoch die Hemmung der Cyclooxygenase (COX-1 und COX-2).
Meloxicam ist ein potenter Inhibitor der Prostaglandinsynthese in vitro. Meloxicam-Konzentrationen, die während der Therapie erreicht wurden, haben in vivo Wirkungen hervorgerufen. Prostaglandine sensibilisieren afferente Nerven und potenzieren die Wirkung von Bradykinin bei der Schmerzauslösung in Tiermodellen. Prostaglandine sind Entzündungsmediatoren. Da Meloxicam ein Hemmer der Prostaglandinsynthese ist, kann seine Wirkungsweise auf einer Abnahme von Prostaglandinen in peripheren Geweben beruhen.
Pharmakokinetik
Absorption
Die absolute Bioverfügbarkeit von Meloxicam-Kapseln betrug 89 % nach einer oralen Einzeldosis von 30 mg im Vergleich zu einer intravenösen Bolusinjektion von 30 mg. Nach einmaliger intravenöser Gabe zeigte sich eine dosisproportionale Pharmakokinetik im Bereich von 5 mg bis 60 mg. Nach mehrfacher oraler Gabe war die Pharmakokinetik von Meloxicam-Kapseln im Bereich von 7,5 mg bis 15 mg dosisproportional. Die mittlere Cmax wurde innerhalb von vier bis fünf Stunden nach Einnahme einer 7,5-mg-Meloxicam-Tablette im nüchternen Zustand erreicht, was auf eine verlängerte Arzneimittelabsorption hinweist. Bei mehrfacher Gabe wurden Steady-State-Konzentrationen an Tag 5 erreicht. Ein zweiter Meloxicam-Konzentrationspeak tritt etwa 12 bis 14 Stunden nach der Gabe auf, was auf eine Rückführung in die Galle hindeutet.
Dosierungen von 7,5 mg/5 ml und 15 mg/10 ml Meloxicam-Suspension zum Einnehmen haben sich als bioäquivalent mit Meloxicam 7,5 mg bzw. 15 mg Kapseln erwiesen. Es hat sich gezeigt, dass Meloxicam-Kapseln mit MOBIC 7,5-mg-Tabletten bioäquivalent sind.
Lebensmittel- und Antazida-Effekte
Die Einnahme von Meloxicam-Kapseln nach einem fettreichen Frühstück (75 g Fett) führte zu einem Anstieg der mittleren Spitzenwerte des Arzneimittels (dh Cmax) um etwa 22 %, während das Ausmaß der Resorption (AUC) unverändert blieb. Die Zeit bis zur maximalen Konzentration (Tmax) wurde zwischen 5 und 6 Stunden erreicht. Im Vergleich dazu waren weder die AUC- noch die Cmax-Werte der Meloxicam-Suspension nach einer ähnlich fettreichen Mahlzeit betroffen, während die mittleren Tmax-Werte auf etwa 7 Stunden angestiegen waren. Bei gleichzeitiger Gabe von Antazida wurde keine pharmakokinetische Wechselwirkung festgestellt. Basierend auf diesen Ergebnissen kann MOBIC 15 mg unabhängig vom Zeitpunkt der Mahlzeiten oder der gleichzeitigen Verabreichung von Antazida verabreicht werden.
Verteilung
Das mittlere Verteilungsvolumen (Vss) von Meloxicam beträgt etwa 10 l. Meloxicam wird innerhalb des therapeutischen Dosisbereichs zu ~99,4 % an menschliche Plasmaproteine (hauptsächlich Albumin) gebunden. Der Anteil der Proteinbindung ist über den klinisch relevanten Konzentrationsbereich unabhängig von der Wirkstoffkonzentration, nimmt aber bei Patienten mit Nierenerkrankungen auf ~99 % ab. Die Penetration von Meloxicam in menschliche rote Blutkörperchen beträgt nach oraler Gabe weniger als 10 %. Nach einer radioaktiv markierten Dosis waren über 90 % der im Plasma nachgewiesenen Radioaktivität als unverändertes Meloxicam vorhanden.
Die Konzentrationen von Meloxicam in der Synovialflüssigkeit nach einer oralen Einzeldosis liegen im Bereich von 40 % bis 50 % der Konzentrationen im Plasma. Die freie Fraktion in Synovialflüssigkeit ist 2,5-mal höher als in Plasma, aufgrund des niedrigeren Albumingehalts in Synovialflüssigkeit im Vergleich zu Plasma. Die Bedeutung dieses Eindringens ist unbekannt.
Beseitigung
Stoffwechsel
Meloxicam wird weitgehend in der Leber metabolisiert. Zu den Meloxicam-Metaboliten gehört 5'-Carboxymeloxicam (60 % der Dosis), das aus dem P-450-vermittelten Stoffwechsel stammt, der durch Oxidation eines Zwischenmetaboliten, 5'-Hydroxymethylmeloxicam, gebildet wird, der ebenfalls in geringerem Maße (9 % der Dosis) ausgeschieden wird ). In-vitro-Studien weisen darauf hin, dass CYP2C9 (Cytochrom-P450-metabolisierendes Enzym) eine wichtige Rolle in diesem Stoffwechselweg mit einem geringen Beitrag des CYP3A4-Isozyms spielt. Die Peroxidase-Aktivität der Patienten ist wahrscheinlich für die beiden anderen Metaboliten verantwortlich, die 16 % bzw. 4 % der verabreichten Dosis ausmachen. Von allen vier Metaboliten ist keine pharmakologische Aktivität in vivo bekannt.
Ausscheidung
Die Ausscheidung von Meloxicam erfolgt überwiegend in Form von Metaboliten und tritt zu gleichen Teilen im Urin und im Stuhl auf. Nur Spuren der unveränderten Muttersubstanz werden im Urin (0,2 %) und Kot (1,6 %) ausgeschieden. Das Ausmaß der Urinausscheidung wurde für unmarkierte Mehrfachdosen von 7,5 mg bestätigt: 0,5 %, 6 % und 13 % der Dosis wurden im Urin in Form von Meloxicam gefunden, und die 5&bgr;-Hydroxymethyl- und 5&bgr; -Carboxy-Metabolite. Es gibt eine signifikante biliäre und/oder enterale Sekretion des Arzneimittels. Dies wurde nachgewiesen, als die orale Gabe von Cholestyramin nach einer intravenösen Einzeldosis Meloxicam die AUC von Meloxicam um 50 % senkte.
Die mittlere Eliminationshalbwertszeit (t1/2) liegt zwischen 15 und 20 Stunden. Die Eliminationshalbwertszeit ist über die Dosisstufen hinweg konstant, was auf eine lineare Metabolisierung innerhalb des therapeutischen Dosisbereichs hindeutet. Die Plasmaclearance liegt zwischen 7 und 9 ml/min.
Spezifische Populationen
Pädiatrie
Nach Gabe einer Einzeldosis (0,25 mg/kg) und nach Erreichen des Steady State (0,375 mg/kg/Tag) zeigte sich bei jüngeren Patienten (im Alter von 2 bis 6 Jahren) im Vergleich zu älteren Patienten ein allgemeiner Trend zu einer etwa 30 % niedrigeren Exposition Patienten (7 bis 16 Jahre). Die älteren Patienten hatten eine ähnliche (Einzeldosis) oder leicht verringerte (Steady State) Meloxicam-Exposition wie die erwachsenen Patienten, wenn AUC-Werte verwendet wurden, die auf eine Dosis von 0,25 mg/kg normalisiert wurden [siehe DOSIERUNG UND ANWENDUNG ]. Die mittlere Eliminationshalbwertszeit (SD) von Meloxicam betrug 15,2 (10,1) und 13,0 Stunden (3,0) für die 2- bis 6-jährigen Patienten bzw. die 7- bis 16-jährigen Patienten.
In einer Kovariatenanalyse unter Verwendung von Populations-Pharmakokinetik war das Körpergewicht, aber nicht das Alter, die einzige prädiktive Kovariate für Unterschiede in der scheinbaren oralen Plasmaclearance von Meloxicam. Die auf das Körpergewicht normalisierten scheinbaren oralen Clearance-Werte waren adäquate Prädiktoren für die Meloxicam-Exposition bei pädiatrischen Patienten.
Die Pharmakokinetik von MOBIC bei pädiatrischen Patienten unter 2 Jahren wurde nicht untersucht.
Geriatrie
Ältere Männer (≥ 65 Jahre) zeigten ähnliche Meloxicam-Plasmakonzentrationen und Steady-State-Pharmakokinetiken wie junge Männer. Ältere Frauen (≥ 65 Jahre) hatten nach Normalisierung des Körpergewichts eine um 47 % höhere AUCss und eine um 32 % höhere Cmax,ss im Vergleich zu jüngeren Frauen (≤ 55 Jahre). Trotz der erhöhten Gesamtkonzentrationen bei älteren Frauen war das Nebenwirkungsprofil bei beiden älteren Patientenpopulationen vergleichbar. Bei älteren weiblichen Patienten wurde im Vergleich zu älteren männlichen Patienten eine geringere freie Fraktion gefunden.
Sex
Junge Frauen wiesen im Vergleich zu jungen Männern etwas niedrigere Plasmakonzentrationen auf. Nach Einzeldosen von 7,5 mg MOBIC betrug die mittlere Eliminationshalbwertszeit 19,5 Stunden für die weibliche Gruppe im Vergleich zu 23,4 Stunden für die männliche Gruppe. Im Steady State waren die Daten ähnlich (17,9 Stunden gegenüber 21,4 Stunden). Dieser pharmakokinetische Unterschied aufgrund des Geschlechts ist wahrscheinlich von geringer klinischer Bedeutung. Es gab eine Linearität der Pharmakokinetik und keinen nennenswerten Unterschied in Cmax oder Tmax zwischen den Geschlechtern.
Leberfunktionsstörung
Nach einer Einzeldosis von 15 mg Meloxicam gab es keinen deutlichen Unterschied in den Plasmakonzentrationen bei Patienten mit leichter (Child-Pugh-Klasse I) oder mäßiger (Child-Pugh-Klasse II) Leberfunktionsstörung im Vergleich zu gesunden Probanden. Die Proteinbindung von Meloxicam wurde durch eine Leberfunktionsstörung nicht beeinflusst. Bei Patienten mit leichter bis mittelschwerer Leberfunktionsstörung ist keine Dosisanpassung erforderlich. Patienten mit schwerer Leberfunktionsstörung (Child-Pugh-Klasse III) wurden nicht ausreichend untersucht [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und Verwendung in bestimmten Bevölkerungsgruppen ].
Nierenfunktionsstörung
Die Pharmakokinetik von Meloxicam wurde bei Patienten mit leichter und mittelschwerer Nierenfunktionsstörung untersucht. Die Gesamtplasmakonzentrationen von Meloxicam nahmen ab und die Gesamtclearance von Meloxicam nahm mit dem Grad der Nierenfunktionsstörung zu, während die freien AUC-Werte in allen Gruppen ähnlich waren. Die höhere Meloxicam-Clearance bei Patienten mit eingeschränkter Nierenfunktion kann auf einen erhöhten Anteil an ungebundenem Meloxicam zurückzuführen sein, das für den hepatischen Metabolismus und die anschließende Ausscheidung verfügbar ist. Bei Patienten mit leichter bis mittelschwerer Nierenfunktionsstörung ist keine Dosisanpassung erforderlich. Patienten mit schwerer Nierenfunktionsstörung wurden nicht ausreichend untersucht. Die Anwendung von MOBIC bei Patienten mit schwerer Nierenfunktionsstörung wird nicht empfohlen [siehe DOSIERUNG UND ANWENDUNG , WARNUNGEN UND VORSICHTSMASSNAHMEN und Verwendung in bestimmten Bevölkerungsgruppen ].
Hämodialyse
Nach einer Einzeldosis Meloxicam waren die freien Cmax-Plasmakonzentrationen bei Patienten mit Nierenversagen unter chronischer Hämodialyse (1 % freier Anteil) höher als bei gesunden Probanden (0,3 % freier Anteil). Die Hämodialyse senkte die Gesamtkonzentration des Medikaments im Plasma nicht; daher sind nach der Hämodialyse keine zusätzlichen Dosen erforderlich. Meloxicam ist nicht dialysierbar [vgl DOSIERUNG UND ANWENDUNG und Verwendung in bestimmten Bevölkerungsgruppen ].
Arzneimittelwechselwirkungsstudien
Aspirin
Wenn NSAIDs mit Aspirin verabreicht wurden, wurde die Proteinbindung von NSAIDs reduziert, obwohl die Clearance von freiem NSAID nicht verändert wurde. Wenn MOBIC 15 mg zusammen mit Aspirin (dreimal täglich 1000 mg) an gesunde Probanden verabreicht wurde, führte dies tendenziell zu einem Anstieg der AUC (10 %) und Cmax (24 %) von Meloxicam. Die klinische Bedeutung dieser Wechselwirkung ist nicht bekannt. Siehe Tabelle 3 für klinisch signifikante Arzneimittelwechselwirkungen von NSAIDs mit Aspirin [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Cholestyramin
Eine viertägige Vorbehandlung mit Cholestyramin erhöhte die Clearance von Meloxicam signifikant um 50 %. Dies führte zu einer Verringerung von t1/2 von 19,2 Stunden auf 12,5 Stunden und zu einer 35 %igen Verringerung der AUC. Dies legt die Existenz eines Rezirkulationsweges für Meloxicam im Gastrointestinaltrakt nahe. Die klinische Relevanz dieser Wechselwirkung wurde nicht nachgewiesen.
Cimetidin
Die gleichzeitige Verabreichung von 200 mg Cimetidin viermal täglich veränderte die Pharmakokinetik einer Einzeldosis von 30 mg Meloxicam nicht.
Digoxin
Meloxicam 15 mg einmal täglich über 7 Tage veränderte das Plasmakonzentrationsprofil von Digoxin nach 7-tägiger Gabe von β-Acetyldigoxin in klinischen Dosen nicht. In-vitro-Tests ergaben keine proteinbindende Wechselwirkung zwischen Digoxin und Meloxicam.
Lithium
In einer an gesunden Probanden durchgeführten Studie waren die mittlere Lithiumkonzentration und AUC vor der Dosis bei Probanden, die Lithiumdosen von 804 bis 1072 mg zweimal täglich mit Meloxicam 15 mg einmal täglich erhielten, um 21 % erhöht, verglichen mit Probanden, die Lithium allein erhielten [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Methotrexat
In einer Studie mit 13 Patienten mit rheumatoider Arthritis (RA) wurden die Wirkungen mehrerer Meloxicam-Dosen auf die Pharmakokinetik von einmal wöchentlich eingenommenem Methotrexat untersucht. Meloxicam hatte keine signifikante Wirkung auf die Pharmakokinetik von Methotrexat-Einzeldosen. In vitro verdrängte Methotrexat Meloxicam nicht von seinen humanen Serumbindungsstellen [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Warfarin
Die Wirkung von Meloxicam auf die gerinnungshemmende Wirkung von Warfarin wurde an einer Gruppe gesunder Probanden untersucht, die tägliche Dosen Warfarin erhielten, die eine INR (International Normalized Ratio) zwischen 1,2 und 1,8 erzeugten. Bei diesen Probanden veränderte Meloxicam nicht die Pharmakokinetik von Warfarin und die durchschnittliche gerinnungshemmende Wirkung von Warfarin, bestimmt durch die Prothrombinzeit. Ein Proband zeigte jedoch einen Anstieg der INR von 1,5 auf 2,1. Vorsicht ist geboten, wenn MOBIC 15 mg zusammen mit Warfarin verabreicht wird, da bei Patienten unter Warfarin Änderungen der INR und ein erhöhtes Risiko für Blutungskomplikationen auftreten können, wenn ein neues Medikament eingeführt wird [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Klinische Studien
Arthrose und rheumatoide Arthritis
Die Anwendung von MOBIC 15 mg zur Behandlung der Anzeichen und Symptome von Osteoarthritis des Knies und der Hüfte wurde in einer 12-wöchigen, doppelblinden, kontrollierten Studie untersucht. MOBIC (3,75 mg, 7,5 mg und 15 mg täglich) wurde mit Placebo verglichen. Die vier primären Endpunkte waren die Gesamtbeurteilung durch den Prüfarzt, die Gesamtbeurteilung des Patienten, die Schmerzbeurteilung des Patienten und der Gesamt-WOMAC-Score (ein selbst auszufüllender Fragebogen zu Schmerz, Funktion und Steifheit). Patienten unter MOBIC 7,5 mg täglich und MOBIC 15 mg täglich zeigten eine signifikante Verbesserung bei jedem dieser Endpunkte im Vergleich zu Placebo.
Die Anwendung von MOBIC zur Behandlung von Anzeichen und Symptomen von Osteoarthritis wurde in sechs doppelblinden, aktiv kontrollierten Studien außerhalb der USA mit einer Dauer von 4 Wochen bis 6 Monaten bewertet. In diesen Studien war die Wirksamkeit von MOBIC in Dosen von 7,5 mg/Tag und 15 mg/Tag vergleichbar mit der von Piroxicam 20 mg/Tag und Diclofenac SR 100 mg/Tag und stimmte mit der in der US-Studie beobachteten Wirksamkeit überein.
Die Anwendung von MOBIC 7,5 mg zur Behandlung der Anzeichen und Symptome von rheumatoider Arthritis wurde in einer 12-wöchigen, doppelblinden, kontrollierten multinationalen Studie bewertet. MOBIC (7,5 mg, 15 mg und 22,5 mg täglich) wurde mit Placebo verglichen. Der primäre Endpunkt dieser Studie war die ACR20-Ansprechrate, ein zusammengesetztes Maß aus klinischen, Labor- und funktionellen Maßen des RA-Ansprechens. Patienten, die MOBIC 7,5 mg und 15 mg täglich erhielten, zeigten eine signifikante Verbesserung des primären Endpunkts im Vergleich zu Placebo. Bei der 22,5-mg-Dosis wurde im Vergleich zur 15-mg-Dosis kein inkrementeller Nutzen beobachtet.
Juvenile rheumatoide Arthritis (JRA) pauziartikulärer und polyartikulärer Verlauf
Die Anwendung von MOBIC 7,5 mg zur Behandlung der Anzeichen und Symptome pauziartikulärer oder polyartikulärer juveniler rheumatoider Arthritis bei Patienten ab 2 Jahren wurde in zwei 12-wöchigen, doppelblinden, parallelarmigen, aktiv kontrollierten Studien untersucht .
Beide Studien umfassten drei Arme: Naproxen und zwei Dosen Meloxicam. In beiden Studien begann die Meloxicam-Dosierung mit 0,125 mg/kg/Tag (maximal 7,5 mg) oder 0,25 mg/kg/Tag (maximal 15 mg) und die Naproxen-Dosierung begann mit 10 mg/kg/Tag. In einer Studie wurden diese Dosen während des 12-wöchigen Dosierungszeitraums verwendet, während in der anderen eine Titration nach 4 Wochen auf Dosen von 0,25 mg/kg/Tag und 0,375 mg/kg/Tag (maximal 22,5 mg) Meloxicam und 15 mg/kg vorgenommen wurde /Tag Naproxen.
Die Wirksamkeitsanalyse verwendete die ACR Pediatric 30 Responder-Definition, eine Kombination aus Eltern- und Prüfarztbeurteilungen, Anzahl der aktiven Gelenke und Gelenke mit eingeschränktem Bewegungsbereich und Erythrozytensedimentationsrate. Der Anteil der Responder war in beiden Studien in allen drei Gruppen ähnlich, und es wurde kein Unterschied zwischen den Meloxicam-Dosisgruppen beobachtet.
INFORMATIONEN ZUM PATIENTEN
Medikationsleitfaden für nichtsteroidale Antirheumatika (NSAIDs)
Was sind die wichtigsten Informationen, die ich über sogenannte nichtsteroidale Antirheumatika (NSAIDs) wissen sollte?
NSAIDs können schwerwiegende Nebenwirkungen haben, einschließlich:
Nehmen Sie NSAIDs nicht direkt vor oder nach einer Herzoperation ein, die als „Koronararterien-Bypass-Transplantation (CABG)“ bezeichnet wird.
Vermeiden Sie die Einnahme von NSAIDs nach einem kürzlich erlittenen Herzinfarkt, es sei denn, Ihr medizinischer Betreuer sagt es Ihnen. Sie haben möglicherweise ein erhöhtes Risiko für einen weiteren Herzinfarkt, wenn Sie NSAIDs nach einem kürzlich erlittenen Herzinfarkt einnehmen.
Das Risiko, ein Geschwür oder eine Blutung zu bekommen, steigt mit:
NSAIDs sollten nur verwendet werden:
Was sind NSAIDs?
NSAIDs werden zur Behandlung von Schmerzen und Rötungen, Schwellungen und Hitze (Entzündung) aufgrund von Erkrankungen wie verschiedenen Arten von Arthritis, Menstruationsbeschwerden und anderen Arten von kurzfristigen Schmerzen eingesetzt.
Wer sollte keine NSAIDs einnehmen?
Nehmen Sie keine NSAIDs ein:
Informieren Sie vor der Einnahme von NSAIDs Ihren Arzt über alle Ihre Erkrankungen, auch wenn Sie:
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen, einschließlich verschreibungspflichtiger oder rezeptfreier Arzneimittel, Vitamine oder pflanzlicher Nahrungsergänzungsmittel. NSAIDs und einige andere Arzneimittel können miteinander interagieren und schwerwiegende Nebenwirkungen verursachen. Beginnen Sie nicht mit der Einnahme eines neuen Arzneimittels, ohne vorher mit Ihrem Arzt gesprochen zu haben.
Welche Nebenwirkungen können NSAIDs haben?
NSAIDs können schwerwiegende Nebenwirkungen haben, einschließlich:
Siehe „Was sind die wichtigsten Informationen, die ich über sogenannte nichtsteroidale Antirheumatika (NSAIDs) wissen sollte?“
Andere Nebenwirkungen von NSAIDs sind: Magenschmerzen, Verstopfung, Durchfall, Gas, Sodbrennen, Übelkeit, Erbrechen und Schwindel.
Holen Sie sofort Hilfe, wenn Sie eines der folgenden Symptome bemerken:
Brechen Sie die Einnahme Ihres NSAID ab und rufen Sie sofort Ihren Arzt an, wenn Sie eines der folgenden Symptome bemerken:
Wenn Sie zu viel von Ihrem NSAID eingenommen haben, rufen Sie Ihren Arzt an oder holen Sie sich sofort medizinische Hilfe.
Dies sind nicht alle möglichen Nebenwirkungen von NSAIDs. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker nach NSAIDs.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
Weitere Informationen zu NSAIDs:
Allgemeine Informationen zur sicheren und wirksamen Anwendung von NSAIDs
Medikamente werden manchmal für andere als die in einem Medikationsleitfaden aufgeführten Zwecke verschrieben. Verwenden Sie NSAIDs nicht für einen Zustand, für den es nicht verschrieben wurde. Geben Sie NSAIDs nicht an andere Personen, selbst wenn sie die gleichen Symptome wie Sie haben. Es kann ihnen schaden.
Wenn Sie weitere Informationen zu NSAIDs wünschen, wenden Sie sich an Ihren Arzt. Sie können Ihren Apotheker oder Gesundheitsdienstleister um Informationen über NSAIDs bitten, die für medizinisches Fachpersonal geschrieben sind.
Dieser Medikationsleitfaden wurde von der US Food and Drug Administration genehmigt.