Zyloprim 100mg, 300mg Allopurinol Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist ZYLOPRIM (Allopurinol) und wie wird es angewendet?
DIES IST KEIN UNSCHÄDLICHES DROGEN. ES WIRD NICHT ZUR BEHANDLUNG VON ASYMPTOMATISCHER HYPERURIKÄMIE EMPFOHLEN.
ZYLOPRIM (Allopurinol) senkt die Harnsäurekonzentrationen im Serum und im Urin. Seine Anwendung sollte für jeden Patienten individuell angepasst werden und erfordert ein Verständnis seiner Wirkungsweise und Pharmakokinetik. ZYLOPRIM (Allopurinol) ist indiziert bei:
Was sind Nebenwirkungen von Zyloprim?
Häufige Nebenwirkungen von Zyloprim 100 mg sind:
Informieren Sie Ihren Arzt, wenn bei Ihnen seltene, aber sehr schwerwiegende Nebenwirkungen von Zyloprim 100 mg auftreten, einschließlich:
BEZEICHNUNG
ZYLOPRIM (Allopurinol) hat die folgende Strukturformel:
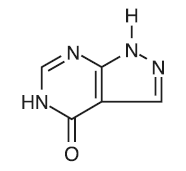
ZYLOPRIM (Allopurinol) ist chemisch als 1,5-Dihydro-4H-pyrazolo [3,4-d]pyrimidin-4-on bekannt. Es ist ein Xanthinoxidase-Hemmer, der oral verabreicht wird. Jede weiße Tablette mit Bruchrille enthält 100 mg Allopurinol und die sonstigen Bestandteile Lactose, Magnesiumstearat, Kartoffelstärke und Povidon. Jede eingekerbte Pfirsichtablette enthält 300 mg Allopurinol und die inaktiven Inhaltsstoffe Maisstärke, FD&C Yellow No. 6 Lake, Lactose, Magnesiumstearat und Povidon. Seine Löslichkeit in Wasser bei 37 °C beträgt 80,0 mg/dL und ist in einer alkalischen Lösung größer.
INDIKATIONEN
DIES IST KEIN UNSCHÄDLICHES DROGEN. ES WIRD NICHT ZUR BEHANDLUNG VON ASYMPTOMATISCHER HYPERURIKÄMIE EMPFOHLEN.
ZYLOPRIM (Allopurinol) senkt die Harnsäurekonzentrationen im Serum und im Urin. Seine Anwendung sollte für jeden Patienten individuell angepasst werden und erfordert ein Verständnis seiner Wirkungsweise und Pharmakokinetik (vgl KLINISCHE PHARMAKOLOGIE, KONTRAINDIKATIONEN, WARNHINWEISE und VORSICHTSMASSNAHMEN ). ZYLOPRIM (Allopurinol) ist angezeigt bei:
DOSIERUNG UND ANWENDUNG
Die Dosierung von ZYLOPRIM (Allopurinol) zur vollständigen Kontrolle der Gicht und zur Senkung der Serum-Harnsäure auf normale oder nahezu normale Werte hängt von der Schwere der Erkrankung ab. Der Durchschnitt liegt bei 200 bis 300 mg/Tag für Patienten mit leichter Gicht und 400 bis 600 mg/Tag für Patienten mit mittelschwerer tophaöser Gicht. Die geeignete Dosis kann in Teildosen oder als äquivalente Einzeldosis zusammen mit der 300-mg-Tablette verabreicht werden. Dosierungsanforderungen von mehr als 300 mg sollten in geteilten Dosen verabreicht werden. Die minimale wirksame Dosis beträgt 100 bis 200 mg täglich und die maximal empfohlene Dosis beträgt 800 mg täglich. Um die Möglichkeit eines Aufflammens akuter Gichtanfälle zu verringern, wird empfohlen, dass der Patient mit einer niedrigen ZYLOPRIM-Dosis (Allopurinol) (100 mg täglich) beginnt und diese in wöchentlichen Abständen um 100 mg erhöht, bis ein Serum-Harnsäurespiegel von 6 erreicht ist mg/dl oder weniger erreicht wird, ohne jedoch die empfohlene Höchstdosis zu überschreiten.
Normale Serumharnsäurespiegel werden normalerweise in 1 bis 3 Wochen erreicht. Die Obergrenze des Normalwerts liegt bei etwa 7 mg/dl für Männer und postmenopausale Frauen und 6 mg/dl für prämenopausale Frauen. Man sollte sich nicht zu sehr auf eine einzelne Bestimmung der Harnsäure im Serum verlassen, da die Bestimmung der Harnsäure aus technischen Gründen schwierig sein kann. Durch Auswahl der geeigneten Dosierung und bei bestimmten Patienten durch gleichzeitige Anwendung von Urikosurika ist es möglich, die Serum-Harnsäure auf normale oder, falls gewünscht, bis auf 2 bis 3 mg/dL zu senken und auf unbestimmte Zeit dort zu halten.
Bei einer Anpassung der Dosierung von ZYLOPRIM (Allopurinol) bei Patienten, die mit Colchicin und/oder entzündungshemmenden Mitteln behandelt werden, ist es ratsam, die letztere Therapie fortzusetzen, bis sich die Serum-Harnsäure normalisiert hat und keine akuten Gichtanfälle mehr aufgetreten sind mehrere Monate.
Bei der Umstellung eines Patienten von einem Urikosurikum auf ZYLOPRIM (Allopurinol) sollte die Dosis des Urikosurikums über einen Zeitraum von mehreren Wochen schrittweise reduziert und die Dosis von ZYLOPRIM (Allopurinol) schrittweise auf die zur Aufrechterhaltung eines normalen Serums erforderliche Dosis erhöht werden Harnsäurespiegel.
Es sollte auch beachtet werden, dass ZYLOPRIM (Allopurinol) im Allgemeinen besser vertragen wird, wenn es nach den Mahlzeiten eingenommen wird. Wünschenswert ist eine ausreichende Flüssigkeitsaufnahme für eine tägliche Harnausscheidung von mindestens 2 Litern und die Aufrechterhaltung eines neutralen oder vorzugsweise leicht alkalischen Urins.
Da ZYLOPRIM (Allopurinol) und seine Metaboliten hauptsächlich nur über die Niere ausgeschieden werden, kann es bei Nierenversagen zu einer Kumulation des Arzneimittels kommen, weshalb die Dosis von ZYLOPRIM (Allopurinol) reduziert werden sollte. Bei einer Kreatinin-Clearance von 10 bis 20 ml/min ist eine Tagesdosis von 200 mg ZYLOPRIM (Allopurinol) geeignet. Wenn die Kreatinin-Clearance weniger als 10 ml/min beträgt, sollte die Tagesdosis 100 mg nicht überschreiten. Bei extrem eingeschränkter Nierenfunktion (Kreatinin-Clearance unter 3 ml/min) muss das Intervall zwischen den Dosen möglicherweise ebenfalls verlängert werden.
Die richtige Größe und Häufigkeit der Dosierung, um die Serumharnsäure gerade im normalen Bereich zu halten, wird am besten bestimmt, indem der Serumharnsäurespiegel als Index verwendet wird.
Zur Vorbeugung einer Harnsäurenephropathie während der intensiven Therapie neoplastischer Erkrankungen ist eine Behandlung mit 600 bis 800 mg täglich für 2 oder 3 Tage zusammen mit einer hohen Flüssigkeitszufuhr ratsam. Ansonsten gelten ähnliche Erwägungen wie die obigen Empfehlungen zur Behandlung von Patienten mit Gicht für die Regulierung der Dosierung zu Erhaltungszwecken bei sekundärer Hyperurikämie.
Die empfohlene Dosis von ZYLOPRIM (Allopurinol) zur Behandlung rezidivierender Calciumoxalatsteine bei Patienten mit Hyperurikosurie beträgt 200 bis 300 mg/Tag in aufgeteilten Dosen oder als Einzeläquivalent. Diese Dosis kann abhängig von der resultierenden Kontrolle der Hyperurikosurie auf der Grundlage nachfolgender 24-Stunden-Harnsäurebestimmungen nach oben oder unten angepasst werden. Klinische Erfahrungen deuten darauf hin, dass Patienten mit rezidivierenden Calciumoxalatsteinen auch von Ernährungsumstellungen profitieren können, wie z. B. der Reduzierung von tierischem Eiweiß, Natrium, raffiniertem Zucker, oxalatreichen Lebensmitteln und übermäßiger Kalziumaufnahme sowie einer Erhöhung der oralen Flüssigkeiten und Ballaststoffe .
Kindern im Alter von 6 bis 10 Jahren mit sekundärer Hyperurikämie in Verbindung mit Malignomen können täglich 300 mg ZYLOPRIM (Allopurinol) verabreicht werden, während Kindern unter 6 Jahren im Allgemeinen 150 mg täglich verabreicht werden. Das Ansprechen wird nach etwa 48 Stunden Therapie beurteilt und gegebenenfalls eine Dosisanpassung vorgenommen.
WIE GELIEFERT
100 mg (weiße) flache zylindrische Tabletten mit Bruchkerbe mit dem Aufdruck „ZYLOPRIM (Allopurinol) 100“ auf einem erhabenen Sechseck, Flaschen mit 100 (NDC 65483-991-10).
Bei 15° bis 25°C (59° bis 77°F) an einem trockenen Ort lagern.
300 mg (Pfirsich) flache, zylindrische Tabletten mit Bruchkerbe mit dem Aufdruck „ZYLOPRIM (Allopurinol) 300“ auf einem erhabenen Sechseck, Flaschen mit 100 (NDC 65483-993-10) und 500 (NDC 65483-993-50).
Bei 15° bis 25°C (59° bis 77°F) an einem trockenen Ort lagern und vor Licht schützen.
Hergestellt von DSM Pharmaceuticals, Inc. Greenville, NC 27834 für Prometheus Laboratories Inc. San Diego, CA 92121. Oktober 2003. FDA Rev.-Datum: 17.07.2002
NEBENWIRKUNGEN
Daten, auf denen die folgenden Schätzungen der Häufigkeit von Nebenwirkungen basieren, stammen aus Erfahrungen, die in der Literatur, unveröffentlichten klinischen Studien und freiwilligen Berichten seit Beginn der Vermarktung von ZYLOPRIM (Allopurinol) berichtet wurden. Frühere Erfahrungen deuteten darauf hin, dass das häufigste Ereignis nach Beginn der Behandlung mit Allopurinol eine Zunahme akuter Gichtanfälle war (durchschnittlich 6 % in frühen Studien). Eine Analyse der aktuellen Verwendung legt nahe, dass die Inzidenz akuter Gichtanfälle auf weniger als 1 % zurückgegangen ist. Die Erklärung für diese Abnahme wurde nicht ermittelt, kann aber teilweise auf einen langsameren Beginn der Therapie zurückzuführen sein (siehe VORSICHTSMASSNAHMEN und DOSIERUNG UND ANWENDUNG ).
Die häufigste Nebenwirkung von ZYLOPRIM (Allopurinol) ist Hautausschlag. Hautreaktionen können schwerwiegend und manchmal tödlich sein. Daher sollte die Behandlung mit ZYLOPRIM (Allopurinol) sofort abgebrochen werden, wenn sich ein Hautausschlag entwickelt (siehe WARNUNGEN ). Einige Patienten mit der schwersten Reaktion hatten auch Fieber, Schüttelfrost, Arthralgien, cholestatische Gelbsucht, Eosinophilie und leichte Leukozytose oder Leukopenie. Unter 55 Patienten mit Gicht, die 3 bis 34 Monate (durchschnittlich mehr als 1 Jahr) mit ZYLO-PRIM behandelt und prospektiv nachbeobachtet wurden, beobachtete Rundles, dass 3 % der Patienten eine Arzneimittelreaktion entwickelten, bei der es sich überwiegend um einen juckenden makulopapulösen Hautausschlag handelte. manchmal schuppig oder exfolia-tiv. Bei der derzeitigen Verwendung wurden Hautreaktionen jedoch seltener als 1 % beobachtet. Die Erklärung für diesen Rückgang ist nicht offensichtlich. Die Inzidenz von Hautausschlägen kann bei Vorliegen einer Niereninsuffizienz erhöht sein. Bei Patienten, die Ampicillin oder Amoxicillin gleichzeitig mit ZYLOPRIM (Allopurinol) erhielten, wurde über eine erhöhte Häufigkeit von Hautausschlägen berichtet (s VORSICHTSMASSNAHMEN ).
Häufigste Reaktionen* Wahrscheinlich ursächlich verbunden:
Magen-Darm: Durchfall, Übelkeit, Anstieg der alkalischen Phosphatase, Anstieg von SGOT/SGPT.
Stoffwechsel und Ernährung: Akute Gichtanfälle.
Haut und Anhängsel: Ausschlag, makulopapulöser Ausschlag.
*Frühe klinische Studien und Inzidenzraten aus frühen klinischen Erfahrungen mit ZYLOPRIM (Allopurinol) deuteten darauf hin, dass diese Nebenwirkungen mit einer Rate von mehr als 1 % auftraten. Das am häufigsten beobachtete Ereignis waren akute Gichtanfälle nach Therapiebeginn. Analysen der derzeitigen Verwendung deuten darauf hin, dass die Inzidenz dieser Nebenwirkungen jetzt weniger als 1 % beträgt. Die Erklärung für diese Abnahme wurde nicht ermittelt, kann aber auf die folgende empfohlene Verwendung zurückzuführen sein (siehe NEBENWIRKUNGEN Einführung, INDIKATIONEN UND ANWENDUNG, VORSICHTSMASSNAHMEN, und DOSIERUNG UND ANWENDUNG ).
Inzidenz Weniger als 1 % Wahrscheinlich ursächlich verbunden:
Körper als Ganzes: Ekchymose, Fieber, Kopfschmerzen.
Herz-Kreislauf: Nekrotisierende Angiitis, Vaskulitis.
Magen-Darm: Lebernekrose, granulomatöse Hepatitis, Hepatomegalie, Hyperbilirubinämie, cholestatischer Ikterus, Erbrechen, intermittierende Bauchschmerzen, Gastritis, Dyspepsie.
Hämisch und lymphatisch: Thrombozytopenie, Eosinophilie, Leukozytose, Leukopenie.
Bewegungsapparat: Myopathie, Arthralgien.
Nervös: Periphere Neuropathie, Neuritis, Parästhesien, Somnolenz.
Atmung: Epistaxis.
Haut und Anhängsel: Erythema multiforme exsudativum (Stevens-Johnson-Syndrom), toxische epidermale Nekrolyse (Lyell-Syndrom), Überempfindlichkeitsvaskulitis, Purpura, vesikuläre bullöse Dermatitis, exfoliative Dermatitis, ekzematoide Dermatitis, Juckreiz, Urtikaria, Alopezie, Onycholyse, Lichen planus.
Besondere Sinne: Geschmacksverlust/Perversion.
Urogenital: Nierenversagen, Urämie (vgl VORSICHTSMASSNAHMEN ).
Inzidenz Weniger als 1 % Kausaler Zusammenhang unbekannt:
Körper als Ganzes: Unwohlsein.
Herz-Kreislauf: Perikarditis, periphere Gefäßerkrankung, Thrombophlebitis, Bradykardie, Vasodilatation.
Endokrin: Unfruchtbarkeit (männlich), Hyperkalzämie, Gynäkomastie (männlich).
Magen-Darm: Hämorrhagische Pankreatitis, Magen-Darm-Blutungen, Stomatitis, Speicheldrüsenschwellung, Hyperlipidämie, Zungenödem, Anorexie.
Hämisch und lymphatisch: Aplastische Anämie, Agranulozytose, eosinophile fibrohistiozytäre Läsion des Knochenmarks, Panzytopenie, Prothrombinabfall, Anämie, hämolytische Anämie, Retiku-Lozytose, Lymphadenopathie, Lymphozytose.
Bewegungsapparat: Myalgie.
Nervös: Optikusneuritis, Verwirrtheit, Schwindel, Schwindel, Fallfuß, Abnahme der Libido, Depression, Amnesie, Tinnitus, Asthenie, Schlaflosigkeit.
Atmung: Bronchospasmus, Asthma, Pharyngitis, Rhinitis.
Haut und Anhängsel: Furunkulose, Gesichtsödem, Schwitzen, Hautödem.
Besondere Sinne: Grauer Star, Makula-Retinitis, Iritis, Konjunktivitis, Amblyopie.
Urogenital: Nephritis, Impotenz, primäre Hämaturie, Albu-Minurie.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Bei Patienten, die Mercaptopurin oder IMU-RAN (Azathioprin) erhalten, erfordert die gleichzeitige Verabreichung von 300 bis 600 mg ZYLOPRIM (Allopurinol) pro Tag eine Dosisreduktion auf etwa ein Drittel bis ein Viertel der üblichen Dosis von Mercaptopurin oder Azathioprin. Eine spätere Dosisanpassung von Mercaptopurin oder Azathioprin sollte auf der Grundlage des therapeutischen Ansprechens und des Auftretens toxischer Wirkungen erfolgen (siehe KLINISCHE PHARMAKOLOGIE ).
Es wurde berichtet, dass ZYLOPRIM (Allopurinol) die Halbwertszeit des Antikoagulans Dicumarol verlängert. Die klinische Grundlage dieser Arzneimittelwechselwirkung wurde nicht ermittelt, sollte jedoch beachtet werden, wenn ZYLOPRIM (Allopurinol) Patienten verabreicht wird, die bereits eine Dicumarol-Therapie erhalten.
Da die Ausscheidung von Oxipurinol der von Urat ähnlich ist, erhöhen Urikosurika, die die Ausscheidung von Urat erhöhen, wahrscheinlich auch die Ausscheidung von Oxipurinol und senken somit den Grad der Hemmung der Xanthinoxidase. Die gleichzeitige Verabreichung von Urikosurika und ZYLOPRIM (Allopurinol) wurde mit einer Abnahme der Ausscheidung von Oxypurinen (Hypoxanthin und Xanthin) und einer Zunahme der Harnsäureausscheidung im Urin im Vergleich zu der mit ZYLOPRIM (Allopurinol) allein beobachteten in Verbindung gebracht. Obwohl klinische Beweise bisher weder bei Patienten unter ZYLO-PRIM allein noch in Kombination mit Urikosurika eine Ausfällung von Oxypurinen in der Niere gezeigt haben, sollte die Möglichkeit im Auge behalten werden.
Die Berichte, dass die gleichzeitige Anwendung von ZYLOPRIM (Allopurinol) und Thiazid-Diuretika bei einigen Patienten zur Verstärkung der Allopuri-Nol-Toxizität beitragen kann, wurden überprüft, um eine Ursache-Wirkungs-Beziehung und einen kausalen Mechanismus herzustellen. Die Durchsicht dieser Fallberichte zeigt, dass die Patienten hauptsächlich Thiazid-Diuretika gegen Bluthochdruck erhielten und dass Tests zum Ausschluss einer verminderten Nierenfunktion als Folge einer hypertensiven Nephropathie nicht oft durchgeführt wurden. Bei Patienten mit dokumentierter Niereninsuffizienz wurde jedoch der Empfehlung, die Dosis von ZYLOPRIM (Allopurinol) zu senken, nicht gefolgt. Obwohl ein kausaler Mechanismus und eine Ursache-Wirkungs-Beziehung nicht etabliert wurden, legen aktuelle Erkenntnisse nahe, dass die Nierenfunktion bei Patienten, die Thiaziddiuretika und ZYLOPRIM (Allopurinol) einnehmen, auch ohne Nierenversagen überwacht werden sollte, und die Dosierung sollte überwacht werden bei Patienten unter einer solchen Kombinationstherapie sogar noch konservativer angepasst werden, wenn eine verminderte Nierenfunktion festgestellt wird.
Bei Patienten, die Ampicillin oder Amoxicillin gleichzeitig mit ZYLOPRIM (Allopurinol) erhielten, wurde im Vergleich zu Patienten, die nicht beide Arzneimittel erhielten, über eine erhöhte Häufigkeit von Hautausschlägen berichtet. Die Ursache der gemeldeten Assoziation wurde nicht festgestellt.
Bei Patienten mit neoplastischen Erkrankungen, außer Leukämie, wurde in Gegenwart von ZYLOPRIM (Allopurinol) über eine verstärkte Knochenmarksuppression durch Cyclophosphamid und andere zytotoxische Wirkstoffe berichtet. In einer gut kontrollierten Studie an Patienten mit Lymphom unter Kombinationstherapie erhöhte ZYLOPRIM (Allopurinol) jedoch nicht die Marktoxizität von Patienten, die mit Cyclophosphamid, Doxorubicin, Bleomycin, Procarbazin und/oder Mechlorethamin behandelt wurden.
Es wurde gezeigt, dass die Umwandlung von Tolbutamid in inaktive Metaboliten durch Xanthinoxidase aus Rattenleber katalysiert wird. Die klinische Bedeutung dieser Beobachtungen, falls vorhanden, ist unbekannt.
Die Plasmahalbwertszeit von Chlorpropamid kann durch ZYLOPRIM (Allopurinol) verlängert werden, da ZYLOPRIM (Allopurinol) und Chlorpropamid um die Ausscheidung in den Nierentubuli konkurrieren können. Das Risiko einer Hypoglykämie als Folge dieses Mechanismus kann erhöht sein, wenn ZYLOPRIM (Allopurinol) und Chlorpropamid gleichzeitig bei Vorliegen einer Niereninsuffizienz gegeben werden.
Seltene Berichte weisen darauf hin, dass die Ciclosporinspiegel während einer gleichzeitigen Behandlung mit ZYLOPRIM (Allopurinol) erhöht sein können. Bei gleichzeitiger Anwendung dieser Arzneimittel sollte eine Überwachung der Ciclosporin-Spiegel und eine mögliche Anpassung der Ciclosporin-Dosierung in Betracht gezogen werden.
Arzneimittel-/Labortest-Wechselwirkungen: Es ist nicht bekannt, dass ZYLOPRIM (Allopurinol) die Genauigkeit von Labortests verändert.
WARNUNGEN
ZYLOPRIM (Allopurinol) SOLLTE BEIM ERSTEN ERSCHEINUNGSBILD EINES HAUTAUSSCHLAGS ODER ANDERER ANZEICHEN, DIE AUF EINE ALLERGISCHE REAKTION HINWEISEN KÖNNEN, ABGESETZT WERDEN. In einigen Fällen können auf einen Hautausschlag schwerwiegendere Überempfindlichkeitsreaktionen wie exfoliative, urtikarielle und purpurische Läsionen sowie Stevens-Johnson-Syndrom (Erythema multiforme exudativum) und/oder generalisierte Vaskulitis, irreversible Hepatotoxizität und, in seltenen Fällen der Tod.
Bei Patienten, die PURINETHOL® (Mercaptopurin) oder IMURAN® (Azathioprin) erhalten, erfordert die gleichzeitige Verabreichung von 300 bis 600 mg ZYLOPRIM (Allopurinol) pro Tag eine Dosisreduktion auf etwa ein Drittel bis ein Viertel der üblichen Dosis Mercaptopurin oder Azathioprin. Eine spätere Dosisanpassung von Mercaptopurin oder Azathioprin sollte auf der Basis des therapeutischen Ansprechens und des Auftretens toxischer Wirkungen erfolgen (siehe KLINISCHE PHARMAKOLOGIE ).
Einige Fälle von reversibler klinischer Hepatotoxizität wurden bei Patienten beobachtet, die ZYLOPRIM (Allopurinol) einnahmen, und bei einigen Patienten wurden asymptomatische Anstiege der alkalischen Phosphatase oder der Serumtransaminase im Serum beobachtet. Wenn sich bei Patienten unter ZYLOPRIM (Allopurinol) Anorexie, Gewichtsverlust oder Juckreiz entwickeln, sollte die Beurteilung der Leberfunktion Teil ihrer diagnostischen Abklärung sein. Bei Patienten mit vorbestehender Lebererkrankung werden in den frühen Phasen der Therapie regelmäßige Leberfunktionstests empfohlen.
Aufgrund des gelegentlichen Auftretens von Schläfrigkeit sollten die Patienten darauf hingewiesen werden, dass bei Aktivitäten, bei denen Wachsamkeit erforderlich ist, angemessene Vorsichtsmaßnahmen getroffen werden müssen.
Das Auftreten von Überempfindlichkeitsreaktionen auf ZYLOPRIM (Allopurinol) kann bei Patienten mit eingeschränkter Nierenfunktion, die gleichzeitig Thiazide und ZYLOPRIM (Allopurinol) erhalten, erhöht sein. Aus diesem Grund sollten solche Kombinationen in diesem klinischen Umfeld mit Vorsicht verabreicht und die Patienten engmaschig überwacht werden.
VORSICHTSMASSNAHMEN
Allgemein: Während der frühen Stadien der Verabreichung von ZYLOPRIM (Allopurinol) wurde über eine Zunahme akuter Gichtanfälle berichtet, selbst wenn normale oder subnormale Harnsäurespiegel im Serum erreicht wurden. Dementsprechend sollten Erhaltungsdosen von Colchicin im Allgemeinen prophylaktisch gegeben werden, wenn mit ZYLOPRIM (Allopurinol) begonnen wird. Darüber hinaus wird empfohlen, dass der Patient mit einer niedrigen Dosis ZYLOPRIM (Allopurinol) (100 mg täglich) beginnt und die Dosis in wöchentlichen Abständen um 100 mg erhöht, bis ein Serum-Harnsäurespiegel von 6 mg/dl oder weniger erreicht ist, jedoch nicht überschritten wird die maximal empfohlene Dosis (800 mg pro Tag). In einigen Fällen kann die Verwendung von Colchicin oder entzündungshemmenden Mitteln erforderlich sein, um Gichtanfälle zu unterdrücken. Die Attacken werden in der Regel nach mehrmonatiger Therapie kürzer und schwächer. Eine mögliche Erklärung für diese Episoden könnte die Mobilisierung von Harnsäure aus Gewebeablagerungen sein, die Schwankungen im Serum-Harnsäurespiegel verursachen. Selbst bei adäquater Therapie mit ZYLOPRIM (Allopurinol) kann es mehrere Monate dauern, bis der Harnsäurepool ausreichend abgebaut ist, um die akuten Attacken unter Kontrolle zu bringen.
Eine Flüssigkeitsaufnahme, die ausreicht, um eine tägliche Urinausscheidung von mindestens 2 Litern zu erzielen, und die Aufrechterhaltung eines neutralen oder vorzugsweise leicht alkalischen Urins sind wünschenswert, um (1) die theoretische Möglichkeit der Bildung von Xanthinsteinen unter dem Einfluss der Therapie mit ZYLOPRIM zu vermeiden (Allopurinol) und (2) helfen, die renale Präzipitation von Harnsäure bei Patienten zu verhindern, die gleichzeitig Urikosurika erhalten.
Einige Patienten mit vorbestehender Nierenerkrankung oder schlechter Harnsäure-Clearance haben einen Anstieg von BUN während der Verabreichung von ZYLOPRIM (Allopurinol) gezeigt. Obwohl der dafür verantwortliche Mechanismus nicht geklärt ist, sollten Patienten mit eingeschränkter Nierenfunktion während der frühen Stadien der Verabreichung von ZYLOPRIM (Allopurinol) sorgfältig überwacht und die Dosis verringert oder das Arzneimittel abgesetzt werden, wenn vermehrte Anomalien der Nierenfunktion auftreten und bestehen bleiben.
Nierenversagen wurde im Zusammenhang mit der Verabreichung von ZYLOPRIM (Allopurinol) bei Patienten mit Hyperurikämie als Folge neoplastischer Erkrankungen beobachtet. Bei den Patienten, deren Nierenfunktionsstörung nach Beginn der Behandlung mit ZYLOPRIM (Allopurinol) zunahm, traten Begleiterkrankungen wie multiples Myelom und dekompensierte Myokarderkrankung auf. Nierenversagen ist auch häufig mit Gicht-Nephropathie und selten mit Überempfindlichkeitsreaktionen im Zusammenhang mit ZYLOPRIM (Allopurinol) verbunden. Albuminurie wurde bei Patienten beobachtet, die nach chronischer Glomerulonephritis und chronischer Pyelonephritis eine klinische Gicht entwickelten.
Patienten mit eingeschränkter Nierenfunktion benötigen niedrigere Dosen von ZYLOPRIM (Allopurinol) als Patienten mit normaler Nierenfunktion. Bei allen Patienten mit eingeschränkter Nierenfunktion sollten zu Beginn der Therapie niedrigere Dosen als empfohlen angewendet und während der frühen Stadien der Anwendung von ZYLOPRIM (Allopurinol) engmaschig überwacht werden. Bei Patienten mit stark eingeschränkter Nierenfunktion oder verminderter Harnsäure-Clearance ist die Halbwertszeit von Oxipurinol im Plasma stark verlängert. Daher kann eine Dosis von 100 mg pro Tag oder 300 mg zweimal pro Woche oder vielleicht weniger ausreichen, um eine angemessene Xanthinoxidase-Hemmung aufrechtzuerhalten und den Harnsäurespiegel im Serum zu senken.
Knochenmarkdepression wurde bei Patienten berichtet, die ZYLOPRIM (Allopurinol) erhielten, von denen die meisten gleichzeitig Arzneimittel erhielten, die diese Reaktion hervorrufen könnten. Dies trat bereits 6 Wochen bis 6 Jahre nach Beginn der Behandlung mit ZYLOPRIM (Allopurinol) auf. In seltenen Fällen kann ein Patient während der alleinigen Behandlung mit ZYLOPRIM (Allopurinol) eine Knochenmarkdepression unterschiedlichen Grades entwickeln, die eine oder mehrere Zelllinien betrifft.
Labortests: Die richtige Dosierung und der Zeitplan zur Aufrechterhaltung der Serum-Harnsäure innerhalb des normalen Bereichs werden am besten bestimmt, indem die Serum-Harnsäure als Index verwendet wird.
Bei Patienten mit vorbestehender Lebererkrankung werden in der Anfangsphase der Therapie regelmäßige Leberfunktionstests empfohlen (s WARNUNGEN ).
ZYLOPRIM (Allopurinol) und sein primärer aktiver Metabolit, Oxipurinol, werden über die Nieren ausgeschieden; Daher haben Veränderungen der Nierenfunktion einen tiefgreifenden Einfluss auf die Dosierung. Bei Patienten mit eingeschränkter Nierenfunktion oder gleichzeitig bestehenden Erkrankungen, die die Nierenfunktion beeinträchtigen können, wie Bluthochdruck und Diabetes mellitus, sollten regelmäßige Laborparameter der Nierenfunktion, insbesondere BUN und Serum-Kreatinin oder Kreatinin-Clearance, durchgeführt und die Dosierung von ZYLOPRIM (Allopurinol ) neu bewertet.
Die Prothrombinzeit sollte bei Patienten, die Dicumarol erhalten und denen ZYLOPRIM (Allopurinol) verabreicht wird, regelmäßig neu bestimmt werden.
Schwangerschaft: Teratogene Wirkungen: Schwangerschaftskategorie C. Reproduktionsstudien wurden an Ratten und Kaninchen mit Dosierungen bis zum Zwanzigfachen der üblichen Dosis beim Menschen (5 mg/kg pro Tag) durchgeführt, und es wurde der Schluss gezogen, dass Allopurinol keine Beeinträchtigung der Fertilität oder Schädigung des Fötus verursachte . Es gibt einen veröffentlichten Bericht über eine Studie an trächtigen Mäusen, denen am 10. oder 13. Trächtigkeitstag 50 oder 100 mg/kg Allopurinol intraperitoneal verabreicht wurde. kg. Bei beiden Allopurinol-Dosen traten am 10. Trächtigkeitstag vermehrt äußere Missbildungen bei Föten und bei beiden Allopurinol-Dosen am 13. Trächtigkeitstag vermehrt Skelettmissbildungen bei Föten auf. Es kann nicht festgestellt werden, ob dies eine fetale Wirkung oder eine sekundäre Wirkung auf die Mutter darstellte Toxizität. Es gibt jedoch keine adäquaten oder gut kontrollierten Studien bei Schwangeren. Da Reproduktionsstudien an Tieren die menschliche Reaktion nicht immer vorhersagen, sollte dieses Medikament während der Schwangerschaft nur angewendet werden, wenn dies eindeutig erforderlich ist.
Die Erfahrung mit ZYLOPRIM (Allopurinol) während der Schwangerschaft beim Menschen war teilweise begrenzt, weil Frauen im gebärfähigen Alter selten eine Behandlung mit ZYLOPRIM (Allopurinol) benötigen. Es gibt zwei unveröffentlichte Berichte und eine veröffentlichte Veröffentlichung von Frauen, die normale Nachkommen zur Welt brachten, nachdem sie ZYLOPRIM (Allopurinol) während der Schwangerschaft erhalten hatten.
Stillende Mutter: Allopurinol und Oxipurinol wurden in der Milch einer Mutter gefunden, die ZYLOPRIM erhielt. Da die Wirkung von Allopurinol auf den Säugling nicht bekannt ist, ist Vorsicht geboten, wenn ZYLOPRIM (Allopurinol) einer stillenden Frau verabreicht wird.
Pädiatrische Verwendung: ZYLOPRIM (Allopurinol) ist selten für die Anwendung bei Kindern indiziert, mit Ausnahme von Kindern mit Hyperurikämie infolge einer Malignität oder bestimmter seltener angeborener Störungen des Purinstoffwechsels (siehe INDIKATIONEN und DOSIERUNG UND ANWENDUNG ).
ÜBERDOSIS
Massive Überdosierung oder akute Vergiftung durch ZYLOPRIM (Allopurinol) wurde nicht berichtet.
Bei Mäusen beträgt die 50 % tödliche Dosis (LD50) 160 mg/kg intraperitoneal (IP) mit Todesverzögerung bis zu 5 Tagen und 700 mg/kg oral (PO) (etwa das 140-fache der üblichen Dosis beim Menschen) mit Todesverzögerung bis 3 Tage. Bei Ratten beträgt die akute LD50 750 mg/kg IP und 6000 mg/kg PO (etwa das 1200-fache der Humandosis).
Zur Behandlung einer Überdosierung gibt es kein spezifisches Antidot für ZYLOPRIM (Allopurinol). Es liegen keine klinischen Erfahrungen mit der Behandlung eines Patienten vor, der große Mengen ZYLOPRIM (Allopurinol) eingenommen hat.
Sowohl ZYLOPRIM (Allopurinol) als auch Oxipurinol sind dialysierbar; Der Nutzen einer Hämodialyse oder Peritonealdialyse bei der Behandlung einer Überdosierung von ZYLOPRIM (Allopurinol) ist jedoch nicht bekannt.
KONTRAINDIKATIONEN
Patienten, die eine schwere Reaktion auf ZYLOPRIM (Allopurinol) entwickelt haben, sollten die Behandlung mit dem Arzneimittel nicht wieder aufnehmen.
KLINISCHE PHARMAKOLOGIE
ZYLOPRIM (Allopurinol) wirkt auf den Purinabbau, ohne die Biosynthese von Purinen zu stören. Es reduziert die Produktion von Harnsäure, indem es die biochemischen Reaktionen hemmt, die seiner Bildung unmittelbar vorausgehen. ZYLOPRIM (Allopurinol) ist ein strukturelles Analogon der natürlichen Purinbase Hypoxanthin. Es ist ein Inhibitor der Xanthinoxidase, des Enzyms, das für die Umwandlung von Hypoxanthin in Xanthin und von Xanthin in Harnsäure, dem Endprodukt des Purinstoffwechsels beim Menschen, verantwortlich ist. ZYLOPRIM (Allopurinol) wird zum entsprechenden Xanthin-Analogon Oxipurinol (Alloxanthin) metabolisiert, das ebenfalls ein Inhibitor der Xanthinoxidase ist.
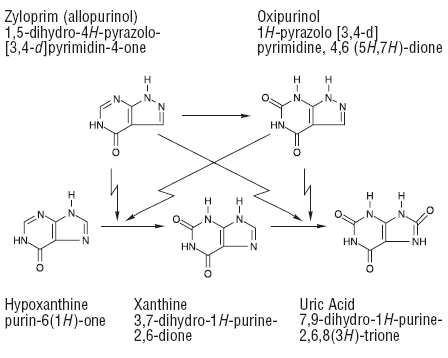
Es wurde gezeigt, dass die Wiederverwendung von sowohl Hypoxanthin als auch Xanthin für die Nukleotid- und Nukleinsäuresynthese deutlich verstärkt wird, wenn ihre Oxidationen durch ZYLOPRIM (Allopurinol) und Oxipurinol gehemmt werden. Diese Wiederverwendung unterbricht jedoch nicht den normalen Nukleinsäureanabolismus, da die Rückkopplungshemmung ein integraler Bestandteil der Purinbiosynthese ist. Als Folge der Xanthinoxidase-Hemmung liegt die Serumkonzentration von Hypoxanthin plus Xanthin bei Patienten, die ZYLOPRIM (Allopurinol) zur Behandlung von Hyperurikämie erhalten, normalerweise im Bereich von 0,3 bis 0,4 mg/dl im Vergleich zu einem normalen Spiegel von etwa 0,15 mg/dl. dl. Ein Maximum von 0,9 mg/dl dieser Oxypurine wurde berichtet, wenn der Serumurat durch hohe Dosen von ZYLOPRIM (Allopurinol) auf weniger als 2 mg/dl gesenkt wurde. Diese Werte liegen weit unter den Sättigungswerten, an denen eine Ausfällung zu erwarten wäre (über 7 mg/dL).
Die renale Clearance von Hypoxanthin und Xanthin ist mindestens zehnmal höher als die von Harnsäure. Der Anstieg von Xanthin und Hypoxanthin im Urin wurde nicht von Nephrolithiasis-Problemen begleitet. Xanthin-Kristallurie wurde nur bei drei Patienten berichtet. Zwei der Patienten hatten das Lesch-Nyhan-Syndrom, das durch eine übermäßige Harnsäureproduktion in Kombination mit einem Mangel des Enzyms Hypoxanthinguanin-Phosphoribosyltransferase (HGPRTase) gekennzeichnet ist. Dieses Enzym wird für die Umwandlung von Hypoxanthin, Xanthin und Guanin in ihre jeweiligen Nukleotide benötigt. Der dritte Patient hatte ein Lymphosarkom und produzierte aufgrund der schnellen Zelllyse während der Chemotherapie eine extrem große Menge an Harnsäure.
ZYLOPRIM (Allopurinol) wird zu etwa 90 % aus dem Gastrointestinaltrakt resorbiert. Maximale Plasmaspiegel treten im Allgemeinen nach 1,5 Stunden bzw. 4,5 Stunden für ZYLOPRIM (Allopurinol) bzw. Oxipurinol auf, und nach einer oralen Einzeldosis von 300 mg ZYLOPRIM (Allopurinol) erreichen maximale Plasmaspiegel etwa 3 µg/ml ZYLOPRIM (Allopurinol) und 6,5 µg/ml Oxipurinol werden produziert.
Ungefähr 20 % des eingenommenen ZYLOPRIM (Allopurinol) werden mit dem Stuhl ausgeschieden. Aufgrund seiner schnellen Oxidation zu Oxipurinol und einer renalen Clearance-Rate, die ungefähr der glomerulären Filtrationsrate entspricht, hat ZYLOPRIM (Allopurinol) eine Plasmahalbwertszeit von etwa 1 bis 2 Stunden. Oxipurinol hat jedoch eine längere Plasmahalbwertszeit (ca. 15 Stunden) und daher wird eine wirksame Hemmung der Xanthinoxidase über einen Zeitraum von 24 Stunden mit täglichen Einzeldosen von ZYLOPRIM (Allopurinol) aufrechterhalten. Während ZYLOPRIM (Allopurinol) im Wesentlichen durch glomeruläre Filtration ausgeschieden wird, wird Oxipurinol in den Nierentubuli auf ähnliche Weise wie die Reabsorption von Harnsäure reabsorbiert.
Die Clearance von Oxipurinol wird durch Urikosurika erhöht, und als Folge verringert die Zugabe eines Urikosurikums bis zu einem gewissen Grad die Hemmung der Xanthinoxidase durch Oxipurinol und erhöht bis zu einem gewissen Grad die Ausscheidung von Harnsäure im Urin. In der Praxis kann der Nettoeffekt einer solchen kombinierten Therapie bei einigen Patienten nützlich sein, um minimale Harnsäurespiegel im Serum zu erreichen, vorausgesetzt, die Gesamtharnsäurebelastung im Urin übersteigt nicht die Kompetenz der Nierenfunktion des Patienten.
Hyperurikämie kann primär sein, wie bei Gicht, oder sekundär bei Erkrankungen wie akuter und chronischer Leukämie, Polycythaemia vera, multiplem Myelom und Psoriasis. Es kann bei der Anwendung von Diuretika, während der Nierendialyse, bei Vorliegen einer Nierenschädigung, während Hungersnot oder Reduktionsdiäten und bei der Behandlung von neoplastischen Erkrankungen auftreten, bei denen es zu einer schnellen Auflösung von Gewebemassen kommen kann. Asymptomatische Hyperurikämie ist keine Indikation für eine Behandlung mit ZYLOPRIM (siehe INDIKATIONEN ).
Gicht ist eine Stoffwechselstörung, die durch Hyperurikämie und daraus resultierende Ablagerung von Mononatriumurat in den Geweben, insbesondere den Gelenken und Nieren, gekennzeichnet ist. Die Ätiologie dieser Hyperurikämie ist die Überproduktion von Harnsäure in Bezug auf die Fähigkeit des Patienten, sie auszuscheiden. Wenn die fortschreitende Harnsäureablagerung angehalten oder rückgängig gemacht werden soll, ist es notwendig, den Harnsäurespiegel im Serum unter den Sättigungspunkt zu senken, um die Harnsäureausfällung zu unterdrücken.
Die Verabreichung von ZYLOPRIM (Allopurinol) führt im Allgemeinen innerhalb von 2 bis 3 Tagen zu einem Abfall der Harnsäure sowohl im Serum als auch im Urin. Das Ausmaß dieser Abnahme kann nahezu beliebig manipuliert werden, da es dosisabhängig ist. Eine Behandlung mit ZYLOPRIM (Allopurinol) kann eine Woche oder länger erforderlich sein, bevor sich seine volle Wirkung zeigt; Ebenso kann die Harnsäure langsam auf die Werte vor der Behandlung zurückkehren (normalerweise nach einem Zeitraum von 7 bis 10 Tagen nach Beendigung der Behandlung). Dies spiegelt in erster Linie die Akkumulation und langsame Clearance von Oxipurinol wider. Bei manchen Patienten kommt es möglicherweise nicht zu einem dramatischen Abfall der Harnsäureausscheidung im Urin, insbesondere bei Patienten mit schwerer tophaöser Gicht. Es wurde postuliert, dass dies auf die Mobilisierung von Harnsäure aus Gewebeablagerungen zurückzuführen ist, wenn der Harnsäurespiegel im Serum zu sinken beginnt.
Die Wirkung von ZYLOPRIM (Allopurinol) unterscheidet sich von der von Urikosurika, die den Harnsäurespiegel im Serum senken, indem sie die Ausscheidung von Harnsäure über den Urin erhöhen. ZYLOPRIM (Allopurinol) senkt sowohl den Harnsäurespiegel im Serum als auch im Urin, indem es die Bildung von Harnsäure hemmt. Die Anwendung von ZYLOPRIM (Allopurinol) zur Blockierung der Harnsäurebildung vermeidet die Gefahr einer erhöhten renalen Harnsäureausscheidung durch Urikosurika.
ZYLOPRIM (Allopurinol) kann die Harnsäurespiegel im Serum und im Urin bei zuvor refraktären Patienten erheblich senken, selbst wenn eine Nierenschädigung vorliegt, die schwerwiegend genug ist, um Urikosurika praktisch unwirksam zu machen. Salicylate können wegen ihrer antirheumatischen Wirkung gemeinsam verabreicht werden, ohne die Wirkung von ZYLO-PRIM zu beeinträchtigen. Dies steht im Gegensatz zu der aufhebenden Wirkung von Salicylaten auf Urikosurika.
ZYLOPRIM (Allopurinol) hemmt auch die enzymatische Oxidation von Mercaptopurin, dem schwefelhaltigen Analogon von Hypoxanthin, zu 6-Thioursäure. Diese durch Xanthinoxidase katalysierte Oxidation inaktiviert Mercaptopurin. Daher kann die Hemmung einer solchen Oxidation durch ZYLOPRIM (Allopurinol) zu einer Verringerung der erforderlichen therapeutischen Dosis von Mercaptopurin um bis zu 75 % führen, wenn die beiden Verbindungen zusammen verabreicht werden.
INFORMATIONEN ZUM PATIENTEN
Patienten sollten über Folgendes informiert werden:
(1) Sie sollten darauf hingewiesen werden, ZYLOPRIM (Allopurinol) abzusetzen und beim ersten Anzeichen eines Hautausschlags, Schmerzen beim Wasserlassen, Blut im Urin, Augenreizung oder Anschwellen der Lippen oder des Mundes sofort ihren Arzt aufzusuchen. (2) Sie sollten daran erinnert werden, die bei Gichtanfällen verschriebene medikamentöse Therapie fortzusetzen, da sich der optimale Nutzen von ZYLOPRIM (Allopurinol) um 2 bis 6 Wochen verzögern kann (3) Sie sollten ermutigt werden, die Flüssigkeitsaufnahme während der Therapie zu erhöhen, um Nierensteinen vorzubeugen. (4) Wenn eine Einzeldosis ZYLOPRIM (Allopurinol) gelegentlich vergessen wird, besteht keine Notwendigkeit, die Dosis zum nächsten vorgesehenen Zeitpunkt zu verdoppeln (5) Es können bestimmte Risiken im Zusammenhang mit der gleichzeitigen Anwendung von ZYLOPRIM (Allopurinol) und Dicumarol bestehen , Sulfinpyrazon, Mercap-Topurin, Azathioprin, Ampicillin, Amoxicillin und Thiazid-Diuretika, und sie sollten die Anweisungen ihres Arztes befolgen.(6) Aufgrund des gelegentlichen Auftretens von Schläfrigkeit sollten Patienten Vorsichtsmaßnahmen treffen, wenn sie sich einlassen bei Aktivitäten, bei denen Aufmerksamkeit erforderlich ist. (7) Patienten können ZYLOPRIM (Allopurinol) nach den Mahlzeiten einnehmen, um Magenreizungen zu minimieren.