Astelin 10ml Azelastine Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Astelin 10 ml und wie wird es angewendet?
Astelin ist ein verschreibungspflichtiges Arzneimittel zur Behandlung der Symptome von Niesen, laufender oder verstopfter Nase (Rhinitis), die durch saisonale Allergien verursacht werden. Astelin kann allein oder mit anderen Medikamenten verwendet werden.
Astelin gehört zu einer Klasse von Medikamenten namens Allergie, Intranasal; Antihistaminika, Intranasal.
Es ist nicht bekannt, ob Astelin bei Kindern unter 5 Jahren sicher und wirksam ist.
Welche Nebenwirkungen kann Astelin 10ml haben?
Astelin 10 ml kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigsten Nebenwirkungen von Astelin gehören:
Teilen Sie dem Arzt mit, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Astelin. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
BEZEICHNUNG
Astelin (Azelastinhydrochlorid) Nasenspray, 137 Mikrogramm (mcg), ist ein Antihistaminikum, formuliert als abgemessene Sprühlösung zur intranasalen Verabreichung. Azelastinhydrochlorid liegt als weißes, fast geruchloses, kristallines Pulver mit bitterem Geschmack vor. Es hat ein Molekulargewicht von 418,37. Es ist in Wasser, Methanol und Propylenglycol kaum löslich und in Ethanol, Octanol und Glycerin etwas löslich. Es hat einen Schmelzpunkt von etwa 225°C und der pH-Wert einer gesättigten Lösung liegt zwischen 5,0 und 5,4. Sein chemischer Name ist (±)-1-(2H)-phthalazinon,4-[(4chlorphenyl)methyl]-2-(hexahydro-1-methyl-1H-azepin-4-yl)-monohydrochlorid. Seine Summenformel ist C22H24ClN3O•HCl mit der folgenden chemischen Struktur:
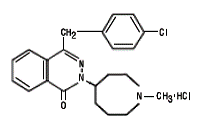
Astelin 10 ml Nasenspray enthält 0,1 % Azelastinhydrochlorid in einer wässrigen Lösung mit einem pH-Wert von 6,8 ± 0,3. Es enthält auch Benzalkoniumchlorid (125 mcg/ml), Dinatriumedetat, Hypromellose, Zitronensäure, dibasisches Natriumphosphat, Natriumchlorid und gereinigtes Wasser.
Nach dem Grundieren [vgl DOSIERUNG UND ANWENDUNG ] gibt jeder abgemessene Sprühstoß ein mittleres Volumen von 0,137 ml ab, das 137 µg Azelastinhydrochlorid (entsprechend 125 µg Azelastinbase) enthält. Die Flasche kann 200 dosierte Sprühstöße abgeben.
INDIKATIONEN
Astelin Nasenspray ist indiziert zur Behandlung der Symptome der saisonalen allergischen Rhinitis bei Erwachsenen und Kindern und Jugendlichen ab 5 Jahren und zur Behandlung der Symptome der vasomotorischen Rhinitis bei Erwachsenen und Jugendlichen ab 12 Jahren.
DOSIERUNG UND ANWENDUNG
Saisonale allergische Rhinitis
Die empfohlene Dosierung von Astelin 10 ml Nasenspray bei erwachsenen und jugendlichen Patienten ab 12 Jahren mit saisonaler allergischer Rhinitis beträgt ein oder zwei Sprühstöße pro Nasenloch zweimal täglich. Die empfohlene Dosierung von Astelin 10 ml Nasenspray bei pädiatrischen Patienten im Alter von 5 bis 11 Jahren beträgt zweimal täglich einen Sprühstoß pro Nasenloch.
Vasomotorische Rhinitis
Die empfohlene Dosierung von Astelin 10 ml Nasenspray bei Erwachsenen und jugendlichen Patienten ab 12 Jahren mit vasomotorischer Rhinitis beträgt zwei Sprühstöße pro Nasenloch zweimal täglich.
Wichtige Verwaltungsanweisungen
Astelin 10 ml Nasenspray nur intranasal verabreichen.
Grundierung: Astelin 10 ml Nasenspray vor dem ersten Gebrauch vorbereiten, indem 4 Sprühstöße abgegeben werden oder bis ein feiner Nebel erscheint. Wenn Astelin 10 ml Nasenspray 3 oder mehr Tage lang nicht verwendet wurde, mit 2 Sprühstößen erneut auffüllen oder bis ein feiner Nebel erscheint. Vermeiden Sie es, Astelin 10 ml Nasenspray in die Augen zu sprühen.
WIE GELIEFERT
Darreichungsformen und Stärken
Astelin 10 ml Nasenspray ist eine Nasenspraylösung. Jeder Sprühstoß Astelin Nasenspray gibt ein Volumen von 0,137 ml Lösung ab, die 137 µg Azelastinhydrochlorid enthält.
Lagerung und Handhabung
Astelin (Azelastinhydrochlorid) Nasenspray, 137 mcg wird als 30-ml-Packung geliefert ( NDC 0037-0241-30) mit 200 dosierten Sprühstößen in einer Flasche aus Polyethylen hoher Dichte (HDPE), die mit einer Pumpeinheit für Dosiersprays ausgestattet ist. Die Sprühpumpeneinheit besteht aus einer Nasenspraypumpe, die mit einem blauen Sicherheitsclip und einer blauen Staubabdeckung aus Kunststoff versehen ist. Der Nettoinhalt der Flasche beträgt 30 ml (Nettogewicht 30 g Lösung). Jede Flasche enthält 30 mg (1 mg/ml) Azelastinhydrochlorid. Nach dem Grundieren [vgl DOSIERUNG UND ANWENDUNG ] gibt jeder Sprühstoß einen feinen Nebel ab, der ein mittleres Volumen von 0,137 ml Lösung enthält, die 137 µg Azelastinhydrochlorid enthält. Die richtige Menge des Medikaments in jedem Sprühstoß kann vor dem ersten Füllen und nach 200 Sprühstößen nicht garantiert werden, auch wenn die Flasche nicht vollständig leer ist. Die Flasche sollte nach 200 Sprühstößen entsorgt werden. Astelin Nasenspray darf nach dem auf dem Arzneimitteletikett und der Faltschachtel aufgedruckten Verfallsdatum „EXP“ nicht mehr verwendet werden.
Lagerung
Bei kontrollierter Raumtemperatur von 20° bis 25°C (68° bis 77°F) lagern. Vor Frost schützen.
Hergestellt von: MEDA Pharmaceuticals Somerset, NJ 08873-4120. Überarbeitet: 10/2014
NEBENWIRKUNGEN
Die Anwendung von Astelin 10 ml Nasenspray wurde mit Somnolenz in Verbindung gebracht [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Erfahrung mit klinischen Studien
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in klinischen Studien mit einem Medikament beobachteten Nebenwirkungsraten nicht direkt mit den Raten in klinischen Studien mit einem anderen Medikament verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Saisonale allergische Rhinitis
Astelin 10 ml Nasenspray Zwei Sprühstöße pro Nasenloch zweimal täglich
Die Informationen zu Nebenwirkungen von Astelin 10 ml Nasenspray stammen aus sechs placebo- und wirkstoffkontrollierten klinischen Studien über 2 Tage bis 8 Wochen, an denen 391 Patienten im Alter von 12 Jahren und älter mit saisonaler allergischer Rhinitis teilnahmen, die Astelin 10 ml Nasenspray erhielten in einer Dosis von 2 Sprühstößen pro Nasenloch zweimal täglich. In Placebo-kontrollierten Wirksamkeitsstudien betrug die Inzidenz von Behandlungsabbrüchen aufgrund von Nebenwirkungen bei Patienten, die Astelin Nasenspray und Vehikel-Placebo erhielten, 2,2 % bzw. 2,8 %.
Tabelle 1 enthält Nebenwirkungen, die mit einer Häufigkeit von ≥ 2 % in der Behandlungsgruppe mit Astelin 10 ml Nasenspray 2 Sprühstöße pro Nasenloch zweimal täglich und häufiger als unter Placebo berichtet wurden.
Astelin 10 ml Nasenspray Zweimal täglich ein Sprühstoß pro Nasenloch
Die Informationen zu Nebenwirkungen von Astelin 10 ml Nasenspray in einer Dosis von einem Sprühstoß pro Nasenloch zweimal täglich stammen aus zwei placebokontrollierten 2-wöchigen klinischen Studien, an denen 276 Patienten ab 12 Jahren mit saisonaler allergischer Rhinitis teilnahmen. Die Inzidenz von Behandlungsabbrüchen aufgrund von Nebenwirkungen bei Patienten, die Astelin 10 ml Nasenspray und Vehikel-Placebo erhielten, betrug 0,0 % bzw. 0,8 %. Bitterer Geschmack wurde bei 8,3 % der Patienten berichtet, im Vergleich zu keinem in der Placebogruppe. Somnolenz wurde bei 0,4 % der Patienten berichtet, im Vergleich zu keinem in der Placebogruppe.
Insgesamt 176 Patienten im Alter von 5 bis 11 Jahren wurden Astelin 10 ml Nasenspray in einer Dosis von 1 Sprühstoß in jedes Nasenloch zweimal täglich in 3 placebokontrollierten Studien ausgesetzt. In diesen Studien traten Nebenwirkungen, die häufiger bei Patienten auftraten, die mit Astelin 10 ml Nasenspray behandelt wurden, als unter Placebo auf und waren in der obigen Tabelle der Nebenwirkungen bei Erwachsenen nicht aufgeführt, darunter Rhinitis/Erkältungssymptome (17,0 % vs. 9,5 %), Husten ( 11,4 % vs. 8,3 %), Konjunktivitis (5,1 % vs. 1,8 %) und Asthma (4,5 % vs. 4,1 %).
Nebenwirkungen
Die folgenden Reaktionen wurden selten (
Herz-Kreislauf: Flush, Bluthochdruck, Tachykardie.
Dermatologisch: Kontaktdermatitis, Ekzem, Haar- und Follikelinfektion, Furunkulose, Hautrisse.
Verdauungs: Verstopfung, Gastroenteritis, Glossitis, ulzerative Stomatitis, Erbrechen, erhöhter SGPT, aphthöse Stomatitis, Durchfall, Zahnschmerzen.
Stoffwechsel und Ernährung: gesteigerter Appetit.
Bewegungsapparat: Myalgie, Kiefergelenkluxation, rheumatoide Arthritis.
Neurologisch: Hyperkinesie, Hypästhesie, Schwindel.
Psychisch: Angst, Depersonalisation, Depression, Nervosität, Schlafstörungen, abnormales Denken. Atemwege: Bronchospasmus, Husten, Brennen im Hals, Laryngitis, Bronchitis, trockener Hals, nächtliche Dyspnoe, Nasopharyngitis, verstopfte Nase, pharyngolaryngeale Schmerzen, Sinusitis, trockene Nase, Hypersekretion der Nasennebenhöhlen, postnasaler Tropf.
Besondere Sinne: Konjunktivitis, Augenanomalie, Augenschmerzen, tränende Augen, Geschmacksverlust.
Urogenital: Albuminurie, Amenorrhoe, Brustschmerzen, Hämaturie, erhöhte Harnfrequenz.
Ganzer Körper: allergische Reaktion, Rückenschmerzen, Herpes simplex, Virusinfektion, Unwohlsein, Gliederschmerzen, Bauchschmerzen, Fieber.
Vasomotorische Rhinitis
Informationen zu Nebenwirkungen von Astelin Nasenspray stammen aus zwei placebokontrollierten klinischen Studien, an denen 216 Patienten ab 12 Jahren mit vasomotorischer Rhinitis teilnahmen, die Astelin Nasenspray in einer Dosis von 2 Sprühstößen pro Nasenloch zweimal täglich für bis zu 28 Tage erhielten. Die Inzidenz von Behandlungsabbrüchen aufgrund von Nebenwirkungen bei Patienten, die Astelin Nasenspray und Vehikel-Placebo erhielten, betrug 2,8 % bzw. 2,9 %.
Die folgenden Nebenwirkungen wurden mit einer Häufigkeit von ≥ 2 % in der Behandlungsgruppe mit Astelin Nasenspray und häufiger als unter Placebo berichtet.
Selten beobachtete Reaktionen (
In kontrollierten Studien mit nasalen und oralen Azelastinhydrochlorid-Formulierungen kam es selten zu erhöhten Lebertransaminasen.
Postmarketing-Erfahrung
Während der Anwendung nach der Zulassung von Astelin 10 ml Nasenspray wurden die folgenden Nebenwirkungen festgestellt. Da diese Reaktionen freiwillig aus einer Population unbekannter Größe gemeldet werden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder einen kausalen Zusammenhang mit der Arzneimittelexposition herzustellen. Zu den berichteten Nebenwirkungen gehören: Anaphylaxie, Reizung an der Applikationsstelle, Vorhofflimmern, Brustschmerzen, Verwirrtheit, Dyspnoe, Gesichtsödem, unwillkürliche Muskelkontraktionen, wunde Nase, Herzklopfen, Parästhesie, Parosmie, Pruritus, Hautausschlag, Störung oder Verlust des Geruchssinns und/ oder Geschmack, Verträglichkeit, Harnverhalt, Sehstörungen und Xerophthalmie.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Depressiva des zentralen Nervensystems
Die gleichzeitige Anwendung von Astelin Nasenspray mit Alkohol oder anderen das zentrale Nervensystem dämpfenden Mitteln sollte vermieden werden, da es zu einer Verringerung der Aufmerksamkeit und einer Beeinträchtigung der Leistung des zentralen Nervensystems kommen kann [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
WARNUNGEN
Eingeschlossen als Teil der VORSICHTSMASSNAHMEN Sektion.
VORSICHTSMASSNAHMEN
Somnolenz bei Aktivitäten, die geistige Wachsamkeit erfordern
In klinischen Studien wurde bei einigen Patienten, die Astelin 10 ml Nasenspray einnahmen, über das Auftreten von Somnolenz berichtet [siehe NEBENWIRKUNGEN ]. Die Patienten sollten davor gewarnt werden, gefährliche Berufe auszuüben, die eine vollständige geistige Wachsamkeit und motorische Koordination erfordern, wie z. B. das Bedienen von Maschinen oder das Führen eines Kraftfahrzeugs nach der Verabreichung von Astelin 10 ml Nasenspray. Die gleichzeitige Anwendung von Astelin 10 ml Nasenspray mit Alkohol oder anderen das zentrale Nervensystem dämpfenden Mitteln sollte vermieden werden, da eine zusätzliche Verringerung der Aufmerksamkeit und eine zusätzliche Beeinträchtigung der Leistung des zentralen Nervensystems auftreten können [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Informationen zur Patientenberatung
Sehen Von der FDA zugelassene Patientenkennzeichnung (PATIENTENINFORMATIONEN und Gebrauchsanweisung).
Aktivitäten, die geistige Wachsamkeit erfordern
Bei einigen Patienten, die Astelin 10 ml Nasenspray einnahmen, wurde über Somnolenz berichtet. Warnen Sie die Patienten davor, gefährliche Berufe auszuüben, die eine vollständige geistige Wachheit und motorische Koordination erfordern, wie z. B. Autofahren oder Bedienen von Maschinen nach der Verabreichung von Astelin Nasenspray [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Gleichzeitiger Konsum von Alkohol und anderen das zentrale Nervensystem dämpfenden Mitteln
Weisen Sie die Patienten an, die gleichzeitige Anwendung von Astelin Nasenspray mit Alkohol oder anderen das zentrale Nervensystem dämpfenden Mitteln zu vermeiden, da eine zusätzliche Verringerung der Aufmerksamkeit und eine zusätzliche Beeinträchtigung der Leistung des zentralen Nervensystems auftreten können [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Häufige Nebenwirkungen
Informieren Sie die Patienten darüber, dass die Behandlung mit Astelin 10 ml Nasenspray zu Nebenwirkungen führen kann, darunter bitterer Geschmack, Kopfschmerzen, Schläfrigkeit, Dysästhesie, Rhinitis, Nasenbrennen, Pharyngitis, Epistaxis, Sinusitis, paroxysmales Niesen, Übelkeit, Mundtrockenheit, Müdigkeit, Schwindel, und Gewichtszunahme [vgl NEBENWIRKUNGEN ].
Grundierung
Weisen Sie die Patienten an, die Pumpe vor dem ersten Gebrauch und wenn Astelin Nasenspray 3 oder mehr Tage lang nicht verwendet wurde, vorzufüllen [siehe DOSIERUNG UND ANWENDUNG ].
Sprühnebel von den Augen fernhalten
Weisen Sie die Patienten an, Astelin 10 ml Nasenspray nicht in die Augen zu sprühen.
Außerhalb der Reichweite von Kindern aufbewahren
Weisen Sie die Patienten an, Astelin 10 ml Nasenspray außerhalb der Reichweite von Kindern aufzubewahren. Wenn ein Kind versehentlich Astelin 10 ml Nasenspray einnimmt, suchen Sie sofort einen Arzt auf oder rufen Sie eine Giftnotrufzentrale an.
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
In 2-Jahres-Karzinogenitätsstudien an Ratten und Mäusen zeigte Azelastinhydrochlorid bei oralen Dosen von bis zu 30 mg/kg bzw. 25 mg/kg keine Hinweise auf Karzinogenität. Diese Dosen waren etwa das 150- bis 60-fache der maximal empfohlenen intranasalen Tagesdosis beim Menschen [MRHDID] auf mg/m²-Basis.
Azelastinhydrochlorid zeigte im Ames-Test, DNA-Reparaturtest, Maus-Lymphom-Vorwärtsmutationstest, Maus-Mikrokerntest oder Chromosomenaberrationstest im Knochenmark von Ratten keine genotoxischen Wirkungen.
Reproduktions- und Fertilitätsstudien an Ratten zeigten bei oralen Dosen von bis zu 30 mg/kg (etwa das 150-fache der MRHDID bei Erwachsenen auf mg/m²-Basis) keine Auswirkungen auf die männliche oder weibliche Fertilität. Bei 68,6 mg/kg (ungefähr das 340-fache der MRHDID auf mg/m²-Basis) war die Dauer der Östruszyklen verlängert und die Kopulationsaktivität und die Anzahl der Schwangerschaften verringert. Die Anzahl der Corpora lutea und Implantationen war verringert; der Präimplantationsverlust war jedoch nicht erhöht.
Verwendung in bestimmten Bevölkerungsgruppen
Schwangerschaft
Schwangerschaftskategorie C
Es gibt keine angemessenen und gut kontrollierten klinischen Studien bei Schwangeren. Es wurde gezeigt, dass Azelastinhydrochlorid bei Mäusen, Ratten und Kaninchen Entwicklungstoxizität verursacht. Astelin 10 ml Nasenspray sollte während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.
Teratogene Wirkungen
Bei Mäusen verursachte Azelastinhydrochlorid bei etwa dem 170-fachen der maximal empfohlenen intranasalen Tagesdosis beim Menschen (MRHDID) embryofötalen Tod, Missbildungen (Gaumenspalte, kurzer oder fehlender Schwanz, verschmolzene, fehlende oder verzweigte Rippen), verzögerte Ossifikation und verringertes fötales Gewicht. bei Erwachsenen (auf mg/m²-Basis bei einer maternalen oralen Dosis von 68,6 mg/kg/Tag, die auch maternale Toxizität verursachte, wie durch verringertes Körpergewicht belegt). Bei etwa 7-facher MRHDID bei Erwachsenen (auf mg/m²-Basis bei einer maternalen oralen Dosis von 3 mg/kg/Tag) traten bei Mäusen weder fetale noch maternale Wirkungen auf.
Bei Ratten verursachte Azelastinhydrochlorid Fehlbildungen (Oligo- und Brachydaktylie), verzögerte Ossifikation und Skelettveränderungen, ohne maternale Toxizität, bei etwa dem 150-Fachen der MRHDID bei Erwachsenen (auf mg/m²-Basis bei einer maternalen oralen Dosis von 30 mg /kg/Tag). Azelastinhydrochlorid verursachte den embryofötalen Tod und verringertes fötales Gewicht und schwere maternale Toxizität bei einer ungefähr 340-fachen MRHDID (auf mg/m²-Basis bei einer oralen Dosis von 68,6 mg/kg/Tag der Mutter). Bei etwa dem 15-fachen der MRHDID (auf mg/m²-Basis bei einer mütterlichen oralen Dosis von 2 mg/kg/Tag) traten weder fetale noch mütterliche Wirkungen auf.
Bei Kaninchen verursachte Azelastinhydrochlorid bei einer etwa 300-fachen MRHDID bei Erwachsenen (auf mg/m²-Basis bei einer maternalen oralen Dosis von 30 mg/kg/Tag) Aborte, verzögerte Ossifikation und vermindertes fetales Gewicht sowie schwere maternale Toxizität. Bei etwa dem Dreifachen der MRHDID (auf mg/m²-Basis bei einer mütterlichen oralen Dosis von 0,3 mg/kg/Tag) traten weder fetale noch mütterliche Wirkungen auf.
Stillende Mutter
Es ist nicht bekannt, ob Azelastinhydrochlorid in die Muttermilch übergeht. Da viele Arzneimittel in die Muttermilch übergehen, ist Vorsicht geboten, wenn Astelin 10 ml Nasenspray einer stillenden Frau verabreicht wird.
Pädiatrische Verwendung
Die Sicherheit und Wirksamkeit von Astelin Nasenspray zur Behandlung von Symptomen saisonaler allergischer Rhinitis wurde für Patienten ab 5 Jahren nachgewiesen [siehe NEBENWIRKUNGEN und Klinische Studien ]. Die Sicherheit und Wirksamkeit von Astelin Nasenspray zur Behandlung von vasomotorischer Rhinitis wurde für Patienten ab 12 Jahren nachgewiesen [siehe NEBENWIRKUNGEN und Klinische Studien ]. Die Sicherheit und Wirksamkeit von Astelin Nasenspray bei pädiatrischen Patienten unter 5 Jahren mit saisonaler allergischer Rhinitis und bei pädiatrischen Patienten unter 12 Jahren mit vasomotorischer Rhinitis ist nicht erwiesen.
Geriatrische Verwendung
Klinische Studien mit Astelin 10 ml Nasenspray schlossen keine ausreichende Anzahl von Patienten ab 65 Jahren ein, um festzustellen, ob sie anders ansprechen als jüngere Patienten. Andere berichtete klinische Erfahrungen haben keine Unterschiede im Ansprechen zwischen älteren und jüngeren Patienten festgestellt. Im Allgemeinen sollte die Dosisauswahl für einen älteren Patienten vorsichtig sein und normalerweise am unteren Ende des Dosierungsbereichs beginnen, um die größere Häufigkeit einer verminderten Leber-, Nieren- oder Herzfunktion und einer Begleiterkrankung oder einer anderen medikamentösen Therapie widerzuspiegeln.
ÜBERDOSIS
Es wurden keine Überdosierungen mit Astelin Nasenspray berichtet. Es ist unwahrscheinlich, dass eine akute Überdosierung dieser Darreichungsform durch Erwachsene zu klinisch signifikanten Nebenwirkungen außer erhöhter Schläfrigkeit führt, da eine Flasche Astelin Nasenspray 30 mg Azelastinhydrochlorid enthält. Klinische Studien mit Erwachsenen mit Einzeldosen der oralen Darreichungsform von Azelastinhydrochlorid (bis zu 16 mg) haben nicht zu einer erhöhten Inzidenz schwerwiegender Nebenwirkungen geführt. Im Falle einer Überdosierung sollten allgemeine unterstützende Maßnahmen ergriffen werden. Es ist kein Gegenmittel für Astelin 10 ml Nasenspray bekannt. Die orale Einnahme von Antihistaminika kann bei Kleinkindern schwerwiegende Nebenwirkungen hervorrufen. Dementsprechend ist Astelin Nasenspray für Kinder unzugänglich aufzubewahren.
KONTRAINDIKATIONEN
Keiner.
KLINISCHE PHARMAKOLOGIE
Wirkmechanismus
Azelastinhydrochlorid, ein Phthalazinon-Derivat, zeigt Histamin-H1-Rezeptor-antagonistische Aktivität in isolierten Geweben, Tiermodellen und Menschen. Astelin Nasenspray wird als racemisches Gemisch verabreicht, wobei in In-vitro-Studien kein Unterschied in der pharmakologischen Aktivität zwischen den Enantiomeren festgestellt wurde. Der Hauptmetabolit, Desmethylazelastin, besitzt ebenfalls H1-Rezeptor-antagonistische Aktivität.
Pharmakodynamik
Herzelektrophysiologie
In einer placebokontrollierten Studie (95 Patienten mit allergischer Rhinitis) gab es keinen Hinweis auf eine Wirkung von Astelin 10 ml Nasenspray (2 Sprühstöße pro Nasenloch zweimal täglich über 56 Tage) auf die kardiale Repolarisation, dargestellt durch das korrigierte QT-Intervall (QTc). des Elektrokardiogramms. Nach oraler Mehrfachgabe von Azelastin 4 mg oder 8 mg zweimal täglich betrug die mittlere QTc-Änderung 7,2 ms bzw. 3,6 ms.
Es wurden Wechselwirkungsstudien durchgeführt, in denen die kardiale Repolarisationswirkung von gleichzeitig verabreichtem oralem Azelastinhydrochlorid und Erythromycin oder Ketoconazol untersucht wurde. Basierend auf der Analyse serieller Elektrokardiogramme hatten diese Medikamente keine Wirkung auf QTc. Bei einer Dosis, die etwa dem Achtfachen der maximal empfohlenen Dosis entspricht, verlängert Azelastinhydrochlorid das QTc-Intervall nicht in klinisch relevantem Ausmaß.
Pharmakokinetik
Absorption
Nach intranasaler Verabreichung beträgt die systemische Bioverfügbarkeit von Azelastinhydrochlorid etwa 40 %. Maximale Plasmakonzentrationen (Cmax) werden in 23 Stunden erreicht.
Die intranasale Verabreichung von Azelastinhydrochlorid in Dosen von mehr als zwei Sprühstößen pro Nasenloch zweimal täglich über 29 Tage führte zu einem überproportionalen Anstieg der Cmax und der Fläche unter der Kurve (AUC) für Azelastin.
Verteilung
Basierend auf der intravenösen und oralen Verabreichung beträgt das Verteilungsvolumen im Steady State 14,5 l/kg. In-vitro-Studien mit menschlichem Plasma zeigen, dass die Plasmaproteinbindung von Azelastin und seinem Metaboliten Desmethylazelastin etwa 88 % bzw. 97 % beträgt.
Stoffwechsel
Azelastin wird durch das Cytochrom-P450-Enzymsystem oxidativ zum aktiven Hauptmetaboliten Desmethylazelastin metabolisiert. Die spezifischen P450-Isoformen, die für die Biotransformation von Azelastin verantwortlich sind, wurden nicht identifiziert. Nach intranasaler Gabe von Azelastinhydrochlorid bis zum Steady-State liegen die Plasmakonzentrationen von Desmethylazelastin zwischen 20 und 50 % der Azelastinkonzentrationen. Begrenzte Daten weisen darauf hin, dass das Metabolitenprofil ähnlich ist, wenn Azelastinhydrochlorid intranasal oder oral verabreicht wird.
Beseitigung
Basierend auf der intravenösen und oralen Verabreichung betragen die Eliminationshalbwertszeit und die Plasmaclearance 22 Stunden bzw. 0,5 l/h/kg. Ungefähr 75 % einer oralen Dosis von radioaktiv markiertem Azelastinhydrochlorid wurden mit dem Stuhl ausgeschieden, weniger als 10 % als unverändertes Azelastin.
Besondere Populationen
Leberfunktionsstörung: Nach oraler Gabe wurden die pharmakokinetischen Parameter nicht durch Leberfunktionsstörungen beeinflusst.
Nierenfunktionsstörung: Basierend auf Studien mit oraler Einzeldosis führte eine Niereninsuffizienz (Kreatinin-Clearance
Das Alter: Nach oraler Verabreichung wurden die pharmakokinetischen Parameter nicht durch das Alter beeinflusst.
Geschlecht: Nach oraler Verabreichung wurden die pharmakokinetischen Parameter nicht durch das Geschlecht beeinflusst.
Wettrennen: Der Einfluss der Rasse wurde nicht bewertet.
Arzneimittelwechselwirkungen
Erythromycin: Bei gleichzeitiger Verabreichung von oral verabreichtem Azelastin (4 mg zweimal täglich) und Erythromycin (500 mg dreimal täglich über 7 Tage) wurde keine signifikante pharmakokinetische Wechselwirkung beobachtet. In dieser Studie führte die gleichzeitige Verabreichung von oral verabreichtem Azelastin mit Erythromycin zu einer Cmax von 5,36 ± 2,6 ng/ml und einer AUC von 49,7 ± 24 ng·h/ml für Azelastin, wohingegen die alleinige Verabreichung von Azelastin zu einer Cmax von 5,57 ± 2,7 führte ng/ml und AUC von 48,4 ± 24 ng•h/ml für Azelastin.
Cimetidin und Ranitidin: In einer Steady-State-Interaktionsstudie mit mehreren Dosen bei gesunden Probanden erhöhte Cimetidin (400 mg zweimal täglich) die oral verabreichten mittleren Azelastin-Konzentrationen (4 mg zweimal täglich) um etwa 65 %. Bei gleichzeitiger Anwendung von oral verabreichtem Azelastin (4 mg zweimal täglich) und Ranitidinhydrochlorid (150 mg zweimal täglich) wurde keine pharmakokinetische Wechselwirkung beobachtet. Die gleichzeitige orale Verabreichung von Azelastin mit Ranitidin führte zu einer Cmax von 8,89 ± 3,28 ng/ml und einer AUC von 88,22 ± 40,43 ng·h/ml für Azelastin, während Azelastin bei alleiniger Verabreichung zu einer Cmax von 7,83 ± 4,06 ng/ml und einer AUC führte von 80,09 ± 43,55 ng·h/ml für Azelastin.
Theophyllin: Bei gleichzeitiger oraler Gabe von 4 mg Azelastinhydrochlorid zweimal täglich und Theophyllin 300 mg oder 400 mg zweimal täglich wurde keine signifikante pharmakokinetische Wechselwirkung beobachtet.
Klinische Studien
Saisonale allergische Rhinitis
Zwei Sprühstöße pro Nasenloch zweimal täglich
Die Wirksamkeit und Sicherheit von Astelin Nasenspray wurden in drei placebokontrollierten klinischen Studien mit Astelin Nasenspray bewertet, an denen 322 Patienten mit saisonaler allergischer Rhinitis teilnahmen, die bis zu 4 Wochen lang zweimal täglich zwei Sprühstöße pro Nasenloch erhielten. Diese Studien umfassten 55 pädiatrische Patienten im Alter von 12 bis 16 Jahren. Die Bewertung der Wirksamkeit basierte auf dem reflektierenden 12-Stunden-Total Symptom Complex (TSC) und Major Symptom Complex (MSC). Der MSC wurde als Durchschnitt der einzelnen Symptome von Nasenschnupfen, Niesen, laufender Nase/Schnupfen, juckender Nase und tränenden Augen berechnet, wie sie von Patienten auf einer kategorialen Skala von 0 bis 5 bewertet wurden. Astelin Nasenspray mit zwei Sprühstößen pro Nasenloch zweimal täglich zeigte eine stärkere Abnahme des MSC als Placebo (Tabelle 3).
In Dosisfindungsstudien führte die Verabreichung von Astelin 10 ml Nasenspray mit zwei Sprühstößen pro Nasenloch zweimal täglich zu einer statistisch signifikanten Abnahme der Symptome im Vergleich zu einem Placebo mit Kochsalzlösung innerhalb von 3 Stunden nach der ersten Dosisgabe und hielt über das 12-stündige Dosierungsintervall an.
Zweimal täglich ein Sprühstoß pro Nasenloch
Die Wirksamkeit und Sicherheit von Astelin 10 ml Nasenspray wurden in zwei placebokontrollierten klinischen Studien mit Astelin Nasenspray bewertet, an denen 275 Patienten mit saisonaler allergischer Rhinitis teilnahmen, die bis zu 2 Wochen lang zweimal täglich einen Sprühstoß pro Nasenloch erhielten. Die Bewertung der Wirksamkeit basierte auf dem reflektierenden 12-Stunden-Total Nasal Symptom Score [rTNSS]. rTNSS wird als Summe der Patientenbewertungen von vier individuellen Nasensymptomen (laufende Nase, Niesen, juckende Nase und verstopfte Nase) berechnet, wie sie von den Patienten auf einer kategorialen Skala von 0–3 bewertet werden. Der primäre Wirksamkeitsendpunkt war die Veränderung des rTNSS vom Ausgangswert bis zu Tag 14. Die mittlere Veränderung des rTNSS gegenüber dem Ausgangswert war bei Patienten, die Astelin 10 ml Nasenspray mit einem Sprühstoß pro Nasenloch zweimal täglich erhielten, größer als bei Patienten, die Placebo erhielten (Tabelle 4).
Zweiwöchige Studien zum Vergleich der Wirksamkeit (und Sicherheit) von Astelin 10 ml Nasenspray mit zwei Sprühstößen pro Nasenloch zweimal täglich mit einem Sprühstoß pro Nasenloch zweimal täglich wurden nicht durchgeführt.
Vasomotorische Rhinitis
Die Wirksamkeit und Sicherheit von Astelin 10 ml Nasenspray wurden in zwei placebokontrollierten klinischen Studien mit Astelin Nasenspray bewertet, an denen 216 Patienten mit vasomotorischer Rhinitis teilnahmen, die bis zu 4 Wochen lang zweimal täglich zwei Sprühstöße pro Nasenloch erhielten. Diese Patienten hatten seit mindestens einem Jahr eine vasomotorische Rhinitis, negative Hauttests auf Aeroallergene im Innen- und Außenbereich, negative Nasenabstriche auf Eosinophile und negative Nebenhöhlen-Röntgenaufnahmen. Astelin Nasenspray zeigte im Vergleich zu Placebo eine signifikant stärkere Abnahme eines Symptomkomplexes, der aus Rhinorrhoe, postnasalem Tropf, verstopfter Nase und Niesen bestand.
INFORMATIONEN ZUM PATIENTEN
Astelin [AS-ta-LIN] (Azelastinhydrochlorid) Nasenspray
Wichtig: Nur zur Anwendung in der Nase.
Was ist Astelin Nasenspray?
Es ist nicht bekannt, ob Astelin 10 ml Nasenspray bei Kindern mit saisonaler allergischer Rhinitis unter 5 Jahren oder bei Kindern mit vasomotorischer Rhinitis unter 12 Jahren sicher und wirksam ist.
Was sollte ich meinem Arzt vor der Anwendung von Astelin Nasenspray mitteilen?
Informieren Sie vor der Anwendung von Astelin 10 ml Nasenspray Ihren Arzt, wenn Sie:
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen, einschließlich verschreibungspflichtiger und rezeptfreier Arzneimittel, Vitamine und Kräuterergänzungen. Astelin Nasenspray und andere Arzneimittel können sich gegenseitig beeinflussen und Nebenwirkungen verursachen.
Wie sollte ich Astelin 10 ml Nasenspray verwenden?
Was sollte ich bei der Anwendung von Astelin 10ml Nasenspray vermeiden?
Astelin Nasenspray kann Schläfrigkeit verursachen:
Welche Nebenwirkungen kann Astelin Nasenspray haben?
Zu den häufigsten Nebenwirkungen von Astelin 10 ml Nasenspray gehören:
Informieren Sie Ihren Arzt, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Astelin 10 ml Nasenspray. Weitere Informationen erhalten Sie von Ihrem Arzt oder Apotheker.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1800-FDA-1088 melden.
Wie ist Astelin Nasenspray aufzubewahren?
Bewahren Sie Astelin 10 ml Nasenspray und alle Arzneimittel außerhalb der Reichweite von Kindern auf.
Allgemeine Informationen zur sicheren und wirksamen Anwendung von Astelin Nasenspray.
Arzneimittel werden manchmal für Erkrankungen verschrieben, die nicht in einer Packungsbeilage aufgeführt sind. Verwenden Sie Astelin Nasenspray nicht für einen Zustand, für den es nicht verschrieben wurde. Geben Sie Astelin Nasenspray nicht an andere Personen, selbst wenn sie die gleichen Symptome wie Sie haben. Es kann ihnen schaden.
Diese Packungsbeilage fasst die wichtigsten Informationen zu Astelin 10 ml Nasenspray zusammen. Wenn Sie weitere Informationen wünschen, wenden Sie sich an Ihren Arzt. Sie können Ihren Apotheker oder Gesundheitsdienstleister nach Informationen über Astelin 10 ml Nasenspray fragen, das für Angehörige der Gesundheitsberufe bestimmt ist.
Weitere Informationen erhalten Sie telefonisch unter 1-866-210-5954.
Was sind die Inhaltsstoffe von Astelin 10ml Nasenspray?
Wirkstoff: Azelastinhydrochlorid
Inaktive Inhaltsstoffe: Benzalkoniumchlorid, Dinatriumedetat, Hypromellose, Zitronensäure, dibasisches Natriumphosphat, Natriumchlorid und gereinigtes Wasser.
Gebrauchsanweisung
Astelin [AS-ta-LIN] (Azelastinhydrochlorid) Nasenspray
Wichtig: Nur zur Anwendung in der Nase.
Für die richtige Dosis des Arzneimittels:
Abbildung A zeigt die Teile Ihrer Astelin Nasenspraypumpe
Abbildung A 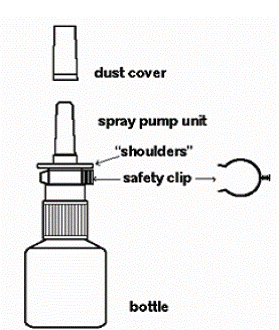
Bevor Sie Astelin Nasenspray zum ersten Mal verwenden, müssen Sie die Flasche entlüften. Vorbereitung Ihres Astelin 10ml Nasensprays
Entfernen Sie die blaue Staubabdeckung über der Spitze der Pumpe und den blauen Sicherheitsclip direkt unter den „Schultern“ der Pumpe (siehe Abbildung B ).
Abbildung B 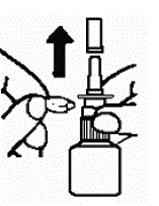
Halten Sie die Flasche aufrecht mit 2 Fingern auf den Schultern der Sprühpumpeneinheit und
Jetzt ist Ihre Pumpe vorbereitet und einsatzbereit.
Abbildung C 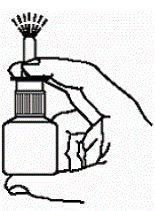
Verwenden Sie Ihr Astelin Nasenspray
Schritt 1. Schnäuzen Sie sich die Nase, um Ihre Nasenlöcher zu reinigen.
Schritt 2. Halten Sie Ihren Kopf nach unten in Richtung Ihrer Zehen geneigt.
Schritt 3. Platzieren Sie die Sprühspitze etwa ¼ Zoll bis ½ Zoll in 1 Nasenloch. Halten Sie die Flasche aufrecht und richten Sie die Sprühspitze auf Ihren Nasenrücken (siehe Abbildung D ).
Abbildung D 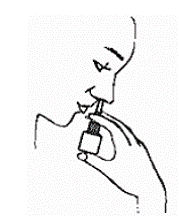
Schritt 4. Schließen Sie Ihr anderes Nasenloch mit einem Finger. Drücken Sie die Pumpe 1 Mal und schnüffeln Sie gleichzeitig sanft, wobei Sie Ihren Kopf nach vorne und unten geneigt halten (Siehe Abbildung E ).
Abbildung E 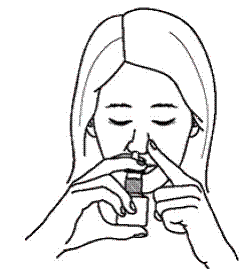
Schritt 5. Wiederholen Sie Schritt 3 und Schritt 4 in dein anderes Nasenloch.
Schritt 6 . Wenn Ihr Arzt Ihnen sagt, dass Sie 2 Sprühstöße in jedes Nasenloch geben sollen, wiederholen Sie dies Schritte 2 bis 4 oben für den zweiten Sprühstoß in jedes Nasenloch.
Schritt 7. Atmen Sie sanft ein und Neige deinen Kopf nicht nach hinten nach der Anwendung von Astelin Nasenspray. Dies hilft zu verhindern, dass das Arzneimittel in Ihren Rachen gelangt.
Schritt 8. Wischen Sie nach der Anwendung Ihres Astelin Nasensprays die Sprühspitze mit einem sauberen Tuch oder Lappen ab. Setzen Sie den Sicherheitsclip und die Staubschutzhülle wieder auf die Flasche.
Reinigen der Sprühspitze Ihres Astelin Nasensprays
Abbildung F 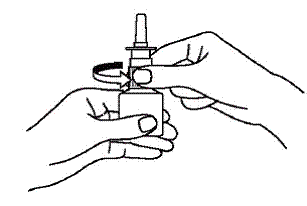
Abbildung G 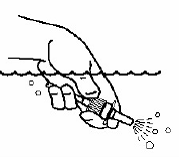
Diese Patienteninformation und Gebrauchsanweisung wurde von der US Food and Drug Administration genehmigt.