Herz-Kreislaufprobleme Behandlung : Coumadin 1mg, 2mg, 5mg Warfarin Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Coumadin und wie wird es angewendet?
Coumadin ist ein verschreibungspflichtiges Arzneimittel zur Behandlung von Blutgerinnseln und zur Verringerung der Wahrscheinlichkeit, dass sich Blutgerinnsel in Ihrem Körper bilden. Blutgerinnsel können einen Schlaganfall, Herzinfarkt oder andere schwerwiegende Erkrankungen verursachen, wenn sie sich in den Beinen oder der Lunge bilden.
Welche Nebenwirkungen hat Coumadin?
Coumadin kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Dies sind nicht alle Nebenwirkungen von Coumadin. Weitere Informationen erhalten Sie von Ihrem Arzt oder Apotheker. Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
WARNUNG
BLUTUNGSRISIKO
BEZEICHNUNG
COUMADIN (Warfarin-Natrium) Tabletten und COUMADIN (Warfarin-Natrium) zur Injektion enthalten Warfarin-Natrium, ein Antikoagulans, das durch Hemmung von Vitamin-K⌈-abhängigen Gerinnungsfaktoren wirkt. Der chemische Name von Warfarin-Natrium lautet 3-(α-Acetonylbenzyl)-4-hydroxycumarin-Natriumsalz, das eine racemische Mischung der R- und S-Enantiomere ist. Kristallines Warfarin-Natrium ist ein Isopropanol-Clathrat. Seine empirische Formel ist C19H15NaO4 und seine Strukturformel wird wie folgt dargestellt:
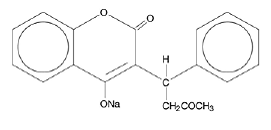
Kristallines Warfarin-Natrium liegt als weißes, geruchloses, kristallines Pulver vor, das sich durch Licht verfärbt. Es ist sehr gut löslich in Wasser, frei löslich in Alkohol und sehr schwach löslich in Chloroform und Äther.
COUMADIN Tabletten zum Einnehmen enthalten außerdem:
COUMADIN 1 mg zur Injektion zur intravenösen Anwendung wird als steriles, lyophilisiertes Pulver geliefert, das nach Rekonstitution mit 2,7 ml sterilem Wasser zur Injektion enthält:
INDIKATIONEN
COUMADIN® ist angezeigt für:
Nutzungsbeschränkungen
COUMADIN 2 mg hat keine direkte Wirkung auf einen etablierten Thrombus, noch kehrt es ischämische Gewebeschäden um. Sobald jedoch ein Thrombus aufgetreten ist, besteht das Ziel der Behandlung mit Antikoagulanzien darin, eine weitere Ausdehnung des gebildeten Gerinnsels zu verhindern und sekundäre thromboembolische Komplikationen zu verhindern, die zu schwerwiegenden und möglicherweise tödlichen Folgen führen können.
DOSIERUNG UND ANWENDUNG
Individuelle Dosierung
Die Dosierung und Verabreichung von COUMADIN 2 mg muss für jeden Patienten entsprechend der INR-Reaktion des Patienten auf das Medikament individuell angepasst werden. Passen Sie die Dosis basierend auf der INR des Patienten und der zu behandelnden Erkrankung an. Konsultieren Sie die neuesten evidenzbasierten Leitlinien für die klinische Praxis bezüglich der Dauer und Intensität der Antikoagulation für die indizierten Erkrankungen.
Empfohlene Ziel-INR-Bereiche und -Dauern für einzelne Indikationen
Ein INR von mehr als 4,0 scheint bei den meisten Patienten keinen zusätzlichen therapeutischen Nutzen zu bringen und ist mit einem höheren Blutungsrisiko verbunden.
Venöse Thromboembolie (einschließlich tiefer Venenthrombose [TVT] und PE)
Passen Sie die Warfarin-Dosis so an, dass ein INR-Zielwert von 2,5 (INR-Bereich 2,0-3,0) für alle Behandlungsdauern beibehalten wird.
Die Behandlungsdauer richtet sich nach der Indikation wie folgt:
Vorhofflimmern
Bei Patienten mit nicht-valvulärem Vorhofflimmern mit Warfarin antikoagulieren, um eine INR von 2,5 (Bereich 2,0–3,0) anzustreben.
Mechanische und bioprothetische Herzklappen
Post-Myokardinfarkt
Wiederkehrende systemische Embolie und andere Indikationen
Die orale Antikoagulationstherapie mit Warfarin wurde in klinischen Studien bei Patienten mit Herzklappenerkrankungen im Zusammenhang mit Vorhofflimmern, Patienten mit Mitralstenose und Patienten mit rezidivierender systemischer Embolie unbekannter Ätiologie nicht vollständig untersucht. Bei diesen Patienten kann jedoch ein moderates Dosierungsschema (INR 2,0-3,0) angewendet werden.
Anfangs- und Erhaltungsdosierung
Die geeignete Anfangsdosis von COUMADIN 2 mg ist für verschiedene Patienten sehr unterschiedlich. Nicht alle Faktoren, die für die Variabilität der Warfarin-Dosis verantwortlich sind, sind bekannt, und die Anfangsdosis wird beeinflusst durch:
Wählen Sie die Anfangsdosis basierend auf der erwarteten Erhaltungsdosis unter Berücksichtigung der oben genannten Faktoren. Modifizieren Sie diese Dosis unter Berücksichtigung patientenspezifischer klinischer Faktoren. Erwägen Sie niedrigere Anfangs- und Erhaltungsdosen für ältere und/oder geschwächte Patienten und bei asiatischen Patienten [siehe Verwendung in bestimmten Bevölkerungsgruppen und KLINISCHE PHARMAKOLOGIE ]. Die routinemäßige Anwendung von Aufsättigungsdosen wird nicht empfohlen, da diese Praxis hämorrhagische und andere Komplikationen verstärken kann und keinen schnelleren Schutz vor Gerinnselbildung bietet.
Individualisieren Sie die Therapiedauer für jeden Patienten. Im Allgemeinen sollte die Antikoagulanzientherapie fortgesetzt werden, bis die Gefahr einer Thrombose und Embolie vorüber ist [siehe Empfohlene Ziel-INR-Bereiche und -Dauern für einzelne Indikationen ].
Dosierungsempfehlungen ohne Berücksichtigung des Genotyps
Wenn die CYP2C9- und VKORC1-Genotypen des Patienten nicht bekannt sind, beträgt die Anfangsdosis von COUMADIN 1 mg normalerweise 2 bis 5 mg einmal täglich. Bestimmen Sie den Dosierungsbedarf jedes Patienten durch genaue Überwachung der INR-Reaktion und Berücksichtigung der behandelten Indikation. Typische Erhaltungsdosen sind 2 bis 10 mg einmal täglich.
Dosierungsempfehlungen unter Berücksichtigung des Genotyps
Tabelle 1 zeigt drei Bereiche erwarteter COUMADIN-Erhaltungsdosen, die in Untergruppen von Patienten mit unterschiedlichen Kombinationen von CYP2C9- und VKORC1-Genvarianten beobachtet wurden [siehe KLINISCHE PHARMAKOLOGIE ]. Wenn der CYP2C9- und/oder VKORC1-Genotyp des Patienten bekannt ist, berücksichtigen Sie diese Bereiche bei der Wahl der Anfangsdosis. Patienten mit CYP2C9 *1/*3, *2/*2, *2/*3 und *3/*3 benötigen möglicherweise eine längere Zeit (> 2 bis 4 Wochen), um die maximale INR-Wirkung für ein bestimmtes Dosierungsschema zu erreichen Patienten ohne diese CYP-Varianten.
Überwachung zur Erzielung einer optimalen Antikoagulation
COUMADIN hat eine enge therapeutische Breite (Index) und seine Wirkung kann durch Faktoren wie andere Arzneimittel und diätetisches Vitamin K beeinflusst werden. Daher muss die Antikoagulation während der COUMADIN-Therapie sorgfältig überwacht werden. Bestimmen Sie die INR täglich nach Verabreichung der Anfangsdosis, bis sich die INR-Ergebnisse im therapeutischen Bereich stabilisieren. Halten Sie nach der Stabilisierung die Dosierung innerhalb des therapeutischen Bereichs, indem Sie regelmäßige INRs durchführen. Die Häufigkeit der Durchführung von INR sollte auf der klinischen Situation basieren, aber allgemein akzeptable Intervalle für INR-Bestimmungen sind 1 bis 4 Wochen. Führen Sie zusätzliche INR-Tests durch, wenn andere Warfarin-Produkte mit COUMADIN ausgetauscht werden, sowie wenn andere Medikamente begonnen, abgesetzt oder unregelmäßig eingenommen werden. Heparin, eine häufige Begleitmedikation, erhöht die INR [siehe Umstellung von anderen Antikoagulanzien und WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Die Bestimmung der Blutgerinnungs- und Blutungszeiten im Vollblut sind keine wirksamen Maßnahmen zur Überwachung der Therapie mit COUMADIN 5 mg.
Nierenfunktionsstörung
Bei Patienten mit Nierenversagen ist keine Dosisanpassung erforderlich. Überwachen Sie die INR häufiger bei Patienten mit eingeschränkter Nierenfunktion, um die INR innerhalb des therapeutischen Bereichs zu halten [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und Verwendung in bestimmten Bevölkerungsgruppen ].
Verpasste Dosis
Die gerinnungshemmende Wirkung von COUMADIN hält über 24 Stunden an. Wenn ein Patient eine Dosis COUMADIN zur vorgesehenen Tageszeit versäumt, sollte der Patient die Dosis so schnell wie möglich noch am selben Tag einnehmen. Der Patient sollte die Dosis am nächsten Tag nicht verdoppeln, um eine vergessene Dosis auszugleichen.
Intravenöser Verabreichungsweg
Die intravenöse Dosis von COUMADIN 1 mg entspricht der oralen Dosis. Nach der Rekonstitution COUMADIN zur Injektion als langsame Bolusinjektion in eine periphere Vene über 1 bis 2 Minuten verabreichen.
COUMADIN 2 mg zur Injektion wird nicht zur intramuskulären Verabreichung empfohlen.
Rekonstituieren Sie die Durchstechflasche mit 2,7 ml sterilem Wasser für Injektionszwecke. Die resultierende Ausbeute beträgt 2,5 ml einer 2 mg pro ml Lösung (insgesamt 5 mg). Parenterale Arzneimittel sollten vor der Verabreichung visuell auf Partikel und Verfärbungen untersucht werden, sofern Lösung und Behältnis dies zulassen. Nicht verwenden, wenn Partikel oder Verfärbungen festgestellt werden.
Nach Rekonstitution ist COUMADIN zur Injektion 4 Stunden bei Raumtemperatur stabil. Sie enthält kein antimikrobielles Konservierungsmittel und daher muss darauf geachtet werden, dass die Sterilität der zubereiteten Lösung gewährleistet ist. Die Durchstechflasche ist nur zum einmaligen Gebrauch bestimmt, verwerfen Sie nicht verwendete Lösung.
Behandlung während Zahnmedizin und Chirurgie
Einige zahnärztliche oder chirurgische Eingriffe können eine Unterbrechung oder Dosisänderung der COUMADIN-Therapie erforderlich machen. Berücksichtigen Sie die Vorteile und Risiken, wenn Sie COUMADIN 2 mg auch nur für kurze Zeit absetzen. Bestimmen Sie die INR unmittelbar vor jedem zahnärztlichen oder chirurgischen Eingriff. Bei Patienten, die sich minimal-invasiven Eingriffen unterziehen und vor, während oder unmittelbar nach diesen Eingriffen antikoaguliert werden müssen, kann eine Anpassung der COUMADIN-Dosierung, um die INR am unteren Ende des therapeutischen Bereichs zu halten, eine sichere Fortsetzung der Antikoagulation ermöglichen.
Umstellung von anderen Antikoagulanzien
Heparin
Da die volle gerinnungshemmende Wirkung von COUMADIN 2 mg erst nach mehreren Tagen erreicht wird, wird Heparin für die anfängliche schnelle Antikoagulation bevorzugt. Während der Initialtherapie mit COUMADIN ist die Interferenz mit der Heparin-Antikoagulation von minimaler klinischer Bedeutung. Die Umstellung auf COUMADIN kann gleichzeitig mit einer Heparintherapie beginnen oder um 3 bis 6 Tage verzögert werden. Um eine therapeutische Antikoagulation zu gewährleisten, setzen Sie die Heparintherapie in voller Dosis fort und überlappen Sie die COUMADIN-Therapie mit Heparin für 4 bis 5 Tage und bis COUMADIN 2 mg die gewünschte therapeutische Reaktion gemäß INR erzielt hat, zu diesem Zeitpunkt kann Heparin abgesetzt werden.
Da Heparin die INR beeinflussen kann, sollte bei Patienten, die sowohl Heparin als auch COUMADIN 1 mg erhalten, die INR mindestens überwacht werden:
COUMADIN 1 mg kann die aktivierte partielle Thromboplastinzeit (aPTT) auch ohne Heparin verlängern. Ein starker Anstieg (> 50 Sekunden) der aPTT mit einer INR im gewünschten Bereich wurde als Hinweis auf ein erhöhtes Risiko einer postoperativen Blutung identifiziert.
Andere Antikoagulanzien
Anweisungen zur Umwandlung in COUMADIN sind der Kennzeichnung anderer Antikoagulantien zu entnehmen.
WIE GELIEFERT
Darreichungsformen und Stärken
Tablets
COUMADIN Tabletten mit einfacher Bruchkerbe
Zur Injektion
Zur Injektion: 5 mg, lyophilisiertes Pulver in einer Einzeldosis-Durchstechflasche.
Lagerung und Handhabung
Tablets
COUMADIN-Tabletten sind einfach eingekerbt, wobei eine Seite numerisch mit 1, 2, 2-1/2, 3, 4, 5, 6, 7-1/2 oder 10 überlagert und mit „COUMADIN“ und der gegenüberliegenden Seite bedruckt ist schmucklos. COUMADIN ist in Flaschen und Einzeldosis-Blisterpackungen für Krankenhäuser mit den folgenden Stärken und Farben erhältlich:
Vor Licht und Feuchtigkeit schützen. Bei kontrollierter Raumtemperatur (59°-86°F, 15°-30°C) lagern. In einem dichten, lichtbeständigen Behälter gemäß USP abgeben.
Bewahren Sie die Krankenhaus-Blisterpackungen zur Abgabe von Einzeldosen im Karton auf, bis der Inhalt aufgebraucht ist.
Injektion
COUMADIN für Injektionszwecke ergeben 5 mg Warfarin nach Rekonstitution mit 2,7 ml sterilem Wasser für Injektionszwecke (maximale Ausbeute beträgt 2,5 ml einer 2 mg/ml Lösung). Der Nettoinhalt der Durchstechflasche beträgt 5,4 mg lyophilisiertes Pulver.
5-mg-Durchstechflasche (Schachtel mit 6) - NDC 0590-0324-35
Vor Licht schützen. Bewahren Sie die Durchstechflasche bis zur Verwendung in der Schachtel auf. Bei kontrollierter Raumtemperatur (59°-86°F, 15°-30°C) lagern.
Nach der Rekonstitution bei kontrollierter Raumtemperatur (59°-86°F, 15°-30°C) lagern und innerhalb von 4 Stunden verwenden.
Nicht kühlen. Verwerfen Sie nicht verwendete Lösung.
Besondere Behandlung
Verfahren zur ordnungsgemäßen Handhabung und Entsorgung potenziell gefährlicher Arzneimittel sollten in Betracht gezogen werden.
Leitlinien zu diesem Thema wurden veröffentlicht [ siehe REFERENZEN ].
Schwangeres Apotheken- und Klinikpersonal sollte den Kontakt mit zerkleinerten oder zerbrochenen Tabletten vermeiden [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
VERWEISE
OSHA Gefährliche Drogen. OSHA. http://www.osha.gov/SLTC/hazardousdrugs/index.html.
Vertrieb durch: Bristol-Myers Squibb Company, Princeton, New Jersey 08543 USA. Überarbeitet: Juni 2017
NEBENWIRKUNGEN
Die folgenden schwerwiegenden Nebenwirkungen von COUMADIN 2 mg werden in anderen Abschnitten der Kennzeichnung ausführlicher erörtert:
Andere Nebenwirkungen von COUMADIN 1 mg umfassen:
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Arzneimittel können über pharmakodynamische oder pharmakokinetische Mechanismen mit COUMADIN 5 mg interagieren. Pharmakodynamische Mechanismen für Arzneimittelwechselwirkungen mit COUMADIN 2 mg sind Synergismus (gestörte Hämostase, verminderte Gerinnungsfaktorsynthese), kompetitiver Antagonismus (Vitamin K) und Veränderung des physiologischen Regelkreises für den Vitamin-K-Stoffwechsel (erbliche Resistenz). Pharmakokinetische Mechanismen für Arzneimittelwechselwirkungen mit COUMADIN sind hauptsächlich Enzyminduktion, Enzymhemmung und reduzierte Plasmaproteinbindung. Es ist wichtig zu beachten, dass einige Medikamente durch mehr als einen Mechanismus interagieren können. Eine häufigere INR-Überwachung sollte durchgeführt werden, wenn andere Arzneimittel begonnen oder abgesetzt werden, einschließlich pflanzlicher Arzneimittel, oder wenn die Dosierung anderer Arzneimittel geändert wird, einschließlich Arzneimitteln, die zur kurzfristigen Anwendung bestimmt sind (z. B. Antibiotika, Antimykotika, Kortikosteroide) [siehe KASTENWARNUNG ].
Konsultieren Sie die Kennzeichnung aller gleichzeitig angewendeten Arzneimittel, um weitere Informationen über Wechselwirkungen mit COUMADIN oder Nebenwirkungen im Zusammenhang mit Blutungen zu erhalten.
CYP450-Wechselwirkungen
Zu den CYP450-Isoenzymen, die am Metabolismus von Warfarin beteiligt sind, gehören CYP2C9, 2C19, 2C8, 2C18, 1A2 und 3A4. Das wirksamere S-Enantiomer von Warfarin wird von CYP2C9 metabolisiert, während das R-Enantiomer von CYP1A2 und 3A4 metabolisiert wird.
Beispiele für Inhibitoren und Induktoren von CYP2C9, 1A2 und 3A4 sind unten in Tabelle 2 aufgeführt; Diese Liste sollte jedoch nicht als vollständig betrachtet werden. Konsultieren Sie die Kennzeichnung aller gleichzeitig angewendeten Arzneimittel, um weitere Informationen über das Wechselwirkungspotenzial von CYP450 zu erhalten. Das Hemmungs- und Induktionspotential von CYP450 sollte beim Beginnen, Beenden oder Ändern der Dosis von Begleitmedikationen berücksichtigt werden. INR engmaschig überwachen, wenn ein gleichzeitig verabreichtes Medikament ein Inhibitor oder Induktor von CYP2C9, 1A2 und/oder 3A4 ist.
Medikamente, die das Blutungsrisiko erhöhen
Beispiele für Arzneimittel, von denen bekannt ist, dass sie das Blutungsrisiko erhöhen, sind in Tabelle 3 aufgeführt. Da das Blutungsrisiko erhöht ist, wenn diese Arzneimittel gleichzeitig mit Warfarin angewendet werden, sollten Patienten, die solche Arzneimittel zusammen mit Warfarin erhalten, engmaschig überwacht werden.
Antibiotika und Antimykotika
Es gibt Berichte über INR-Veränderungen bei Patienten, die Warfarin und Antibiotika oder Antimykotika einnehmen, aber klinische pharmakokinetische Studien haben keine konsistenten Wirkungen dieser Wirkstoffe auf die Plasmakonzentrationen von Warfarin gezeigt.
Bei Patienten, die Warfarin einnehmen, ist die INR beim Beginn oder Absetzen von Antibiotika oder Antimykotika genau zu überwachen.
Botanische (pflanzliche) Produkte und Lebensmittel
Eine häufigere INR-Überwachung sollte durchgeführt werden, wenn mit pflanzlichen Mitteln begonnen oder aufgehört wird.
Es gibt nur wenige adäquate, gut kontrollierte Studien, die das Potenzial für metabolische und/oder pharmakologische Wechselwirkungen zwischen pflanzlichen Stoffen und COUMADIN 2 mg bewerten. Aufgrund fehlender Herstellungsstandardisierung bei botanischen Arzneipräparaten kann die Wirkstoffmenge variieren. Dies könnte die Fähigkeit, potenzielle Wechselwirkungen und Wirkungen auf die Antikoagulation zu beurteilen, weiter beeinträchtigen.
Einige Pflanzenstoffe können bei alleiniger Einnahme Blutungen verursachen (z. B. Knoblauch und Ginkgo biloba) und können gerinnungshemmende, gerinnungshemmende und/oder fibrinolytische Eigenschaften haben. Es ist zu erwarten, dass diese Wirkungen zu den gerinnungshemmenden Wirkungen von COUMADIN hinzukommen. Umgekehrt können einige Pflanzenstoffe die Wirkung von COUMADIN verringern (z. B. Co-Enzym Q10, Johanniskraut, Ginseng). Einige Pflanzenstoffe und Lebensmittel können durch CYP450-Wechselwirkungen mit COUMADIN 2 mg interagieren (z. B. Echinacea, Grapefruitsaft, Ginkgo, Gelbwurzel, Johanniskraut).
Die Menge an Vitamin K in der Nahrung kann die Therapie mit COUMADIN beeinflussen. Empfehlen Sie Patienten, die COUMADIN 1 mg einnehmen, sich normal und ausgewogen zu ernähren und eine konstante Menge an Vitamin K beizubehalten. Patienten, die COUMADIN 5 mg einnehmen, sollten drastische Änderungen ihrer Ernährungsgewohnheiten vermeiden, wie z. B. den Verzehr großer Mengen von grünem Blattgemüse.
WARNUNGEN
Eingeschlossen als Teil der "VORSICHTSMASSNAHMEN" Abschnitt
VORSICHTSMASSNAHMEN
Blutung
COUMADIN kann schwere oder tödliche Blutungen verursachen. Blutungen treten eher innerhalb des ersten Monats auf. Zu den Risikofaktoren für Blutungen gehören eine hohe Intensität der Antikoagulation (INR > 4,0), ein Alter von mindestens 65 Jahren, stark schwankende INR-Werte in der Vorgeschichte, gastrointestinale Blutungen in der Vorgeschichte, Bluthochdruck, zerebrovaskuläre Erkrankungen, Anämie, Malignität, Trauma, Nierenfunktionsstörung und bestimmte genetische Faktoren Faktoren [vgl KLINISCHE PHARMAKOLOGIE ], bestimmte Begleitmedikamente [vgl WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ] und lange Dauer der Warfarin-Therapie.
Führen Sie bei allen behandelten Patienten eine regelmäßige Überwachung der INR durch. Personen mit hohem Blutungsrisiko können von einer häufigeren INR-Überwachung, einer sorgfältigen Dosisanpassung an die gewünschte INR und einer dem klinischen Zustand angemessenen kürzesten Therapiedauer profitieren. Die Aufrechterhaltung der INR im therapeutischen Bereich beseitigt jedoch nicht das Blutungsrisiko.
Medikamente, Ernährungsumstellungen und andere Faktoren beeinflussen die mit COUMADIN 1 mg erzielten INR-Werte. Führen Sie eine häufigere INR-Überwachung durch, wenn Sie mit anderen Arzneimitteln beginnen oder aufhören, einschließlich pflanzlicher Arzneimittel, oder wenn Sie die Dosierung anderer Arzneimittel ändern [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Informieren Sie die Patienten über Präventionsmaßnahmen, um das Blutungsrisiko zu minimieren und Anzeichen und Symptome von Blutungen zu melden [siehe INFORMATIONEN ZUM PATIENTEN ].
Gewebenekrose
Nekrose und/oder Gangrän der Haut und anderer Gewebe sind ein seltenes, aber ernstes Risiko (
Eine sorgfältige klinische Untersuchung ist erforderlich, um festzustellen, ob die Nekrose durch eine Grunderkrankung verursacht wird. Obwohl verschiedene Behandlungen versucht wurden, wurde keine Behandlung für Nekrose als einheitlich wirksam angesehen. Beenden Sie die Therapie mit COUMADIN 5 mg, wenn eine Nekrose auftritt. Erwägen Sie alternative Medikamente, wenn eine fortgesetzte Antikoagulationstherapie erforderlich ist.
Kalziphylaxie
Bei Patienten mit und ohne terminaler Niereninsuffizienz wurde über tödliche und schwere Kalziphylaxie oder Calcium-urämische Arteriolopathie berichtet. Wenn bei diesen Patienten eine Kalziphylaxie diagnostiziert wird, ist COUMADIN 5 mg abzusetzen und die Kalziphylaxie entsprechend zu behandeln. Erwägen Sie eine alternative Antikoagulationstherapie.
Akute Nierenschädigung
Bei Patienten mit veränderter glomerulärer Integrität oder mit einer Nierenerkrankung in der Vorgeschichte kann es unter COUMADIN 2 mg zu einer akuten Nierenschädigung kommen, möglicherweise im Zusammenhang mit Episoden übermäßiger Antikoagulation und Hämaturie [siehe Verwendung in bestimmten Bevölkerungsgruppen ]. Bei Patienten mit eingeschränkter Nierenfunktion wird eine häufigere Überwachung der Antikoagulation empfohlen.
Systemische Atheroembolien und Cholesterin-Mikroembolien
Eine Antikoagulationstherapie mit COUMADIN kann die Freisetzung von atheromatösen Plaque-Emboli verstärken. Systemische Atheroembolien und Cholesterinmikroembolien können je nach Embolisationsort eine Vielzahl von Anzeichen und Symptomen aufweisen. Die am häufigsten betroffenen viszeralen Organe sind die Nieren, gefolgt von Bauchspeicheldrüse, Milz und Leber. Einige Fälle sind bis zur Nekrose oder zum Tod fortgeschritten. Ein ausgeprägtes Syndrom, das aus Mikroembolien an den Füßen resultiert, ist als „Purple-Toes-Syndrom“ bekannt. Beenden Sie die COUMADIN-Therapie, wenn solche Phänomene beobachtet werden. Erwägen Sie alternative Medikamente, wenn eine fortgesetzte Antikoagulationstherapie erforderlich ist.
Extremitätenischämie, Nekrose und Gangrän bei Patienten mit HIT und HITTS
Wenden Sie COUMADIN nicht als Initialtherapie bei Patienten mit Heparin-induzierter Thrombozytopenie (HIT) und mit Heparin-induzierter Thrombozytopenie mit Thrombose-Syndrom (HITTS) an. Fälle von Extremitätenischämie, Nekrose und Gangrän sind bei Patienten mit HIT und HITTS aufgetreten, wenn die Heparinbehandlung abgesetzt und eine Warfarintherapie begonnen oder fortgesetzt wurde. Bei einigen Patienten waren die Folgen Amputation des betroffenen Bereichs und/oder Tod. Eine Behandlung mit COUMADIN kann in Erwägung gezogen werden, nachdem sich die Thrombozytenzahl normalisiert hat.
Anwendung bei Schwangeren mit mechanischen Herzklappen
COUMADIN kann den Fötus schädigen, wenn es einer schwangeren Frau verabreicht wird. Obwohl COUMADIN während der Schwangerschaft kontraindiziert ist, kann der potenzielle Nutzen der Anwendung von COUMADIN 1 mg die Risiken für schwangere Frauen mit mechanischen Herzklappen mit hohem Thromboembolierisiko überwiegen. In diesen individuellen Situationen sollte die Entscheidung, die Behandlung mit COUMADIN 2 mg einzuleiten oder fortzusetzen, mit dem Patienten überprüft werden, wobei die spezifischen Risiken und Vorteile in Bezug auf die individuelle medizinische Situation des einzelnen Patienten sowie die aktuellsten medizinischen Richtlinien zu berücksichtigen sind. Die COUMADIN-Exposition während der Schwangerschaft verursacht ein bekanntes Muster schwerer angeborener Missbildungen (Warfarin-Embryopathie und Fetotoxizität), tödliche fötale Blutungen und ein erhöhtes Risiko für spontane Fehlgeburten und fötale Sterblichkeit. Wenn dieses Arzneimittel während der Schwangerschaft angewendet wird oder wenn die Patientin während der Einnahme dieses Arzneimittels schwanger wird, sollte die Patientin über die potenzielle Gefahr für einen Fötus informiert werden [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
Andere klinische Einstellungen mit erhöhten Risiken
In den folgenden klinischen Situationen können die Risiken einer COUMADIN-Therapie erhöht sein:
Endogene Faktoren, die INR beeinflussen
Die folgenden Faktoren können für eine erhöhte INR-Reaktion verantwortlich sein: Durchfall, Lebererkrankungen, schlechter Ernährungszustand, Steatorrhoe oder Vitamin-K-Mangel.
Die folgenden Faktoren können für eine verringerte INR-Reaktion verantwortlich sein: erhöhte Vitamin-K-Aufnahme oder erbliche Warfarin-Resistenz.
Informationen zur Patientenberatung
Weisen Sie den Patienten an, die von der FDA zugelassene Patientenkennzeichnung ( Leitfaden für Medikamente ).
Anweisungen für Patienten
Empfehlen Sie den Patienten:
Blutungsrisiken
Patienten beraten
Begleitmedikationen und Botanicals (Kräuter)
Empfehlen Sie den Patienten:
Schwangerschaft und Stillzeit
Empfehlen Sie den Patienten:
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Karzinogenitäts-, Mutagenitäts- oder Fertilitätsstudien wurden mit Warfarin nicht durchgeführt.
Verwendung in bestimmten Bevölkerungsgruppen
Schwangerschaft
Zusammenfassung der Risiken
COUMADIN 1 mg ist bei schwangeren Frauen kontraindiziert, außer bei schwangeren Frauen mit mechanischen Herzklappen, die ein hohes Risiko für Thromboembolien haben und für die der Nutzen von COUMADIN 5 mg die Risiken überwiegen kann [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ]. COUMADIN 1 mg kann den Fötus schädigen. Die Exposition gegenüber Warfarin während des ersten Schwangerschaftstrimesters verursachte bei etwa 5 % der exponierten Nachkommen ein Muster angeborener Missbildungen. Da diese Daten nicht in angemessenen und gut kontrollierten Studien erhoben wurden, ist diese Inzidenz schwerer Geburtsfehler keine angemessene Grundlage für einen Vergleich mit den geschätzten Inzidenzen in der Kontrollgruppe oder der US-Allgemeinbevölkerung und spiegelt möglicherweise nicht die in der Praxis beobachteten Inzidenzen wider. Berücksichtigen Sie den Nutzen und die Risiken von COUMADIN und mögliche Risiken für den Fötus, wenn Sie einer schwangeren Frau COUMADIN verschreiben.
Unerwünschte Folgen in der Schwangerschaft treten unabhängig vom Gesundheitszustand der Mutter oder der Einnahme von Medikamenten auf. Das geschätzte Hintergrundrisiko schwerer Geburtsfehler und Fehlgeburten für die angegebene Population ist unbekannt. In der US-Allgemeinbevölkerung liegt das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten bei klinisch erkannten Schwangerschaften bei 2 % bis 4 % bzw. 15 % bis 20 %.
Klinische Überlegungen
Fetale/neonatale Nebenwirkungen
Beim Menschen passiert Warfarin die Plazentaschranke, und die Konzentrationen im fötalen Plasma nähern sich den mütterlichen Werten. Die Exposition gegenüber Warfarin während des ersten Schwangerschaftstrimesters verursachte bei etwa 5 % der exponierten Nachkommen ein Muster angeborener Missbildungen. Die Warfarin-Embryopathie ist gekennzeichnet durch nasale Hypoplasie mit oder ohne getüpfelte Epiphysenfugen (Chondrodysplasia punctata) und Wachstumsverzögerung (einschließlich niedrigem Geburtsgewicht). Es wurde auch über Anomalien des Zentralnervensystems und der Augen berichtet, einschließlich Dysplasie der dorsalen Mittellinie, gekennzeichnet durch Agenesie des Corpus callosum, Dandy-Walker-Fehlbildung, Mittellinienatrophie des Kleinhirns und Dysplasie der ventralen Mittellinie, gekennzeichnet durch Optikusatrophie. Mentale Retardierung, Erblindung, Schizenzephalie, Mikrozephalie, Hydrozephalus und andere unerwünschte Schwangerschaftsergebnisse wurden nach Warfarin-Exposition während des zweiten und dritten Schwangerschaftstrimesters berichtet [siehe KONTRAINDIKATIONEN ].
Stillzeit
Zusammenfassung der Risiken
Warfarin war in der Muttermilch von Müttern, die mit Warfarin behandelt wurden, aus einer begrenzten veröffentlichten Studie nicht vorhanden. Wegen der Möglichkeit schwerwiegender Nebenwirkungen, einschließlich Blutungen bei einem gestillten Säugling, sind die Entwicklungs- und Gesundheitsvorteile des Stillens zusammen mit dem klinischen Bedarf der Mutter an COUMADIN und möglichen Nebenwirkungen von COUMADIN 2 mg auf den gestillten Säugling oder der zugrunde liegenden Erkrankung der Mutter zu berücksichtigen bevor Sie einer stillenden Frau COUMADIN 5 mg verschreiben.
Klinische Überlegungen
Überwachen Sie stillende Säuglinge auf Blutergüsse oder Blutungen.
Daten
Menschliche Daten
Basierend auf veröffentlichten Daten von 15 stillenden Müttern wurde Warfarin nicht in der Muttermilch nachgewiesen. Unter den 15 voll ausgetragenen Neugeborenen hatten 6 gestillte Säuglinge dokumentierte Prothrombinzeiten innerhalb des erwarteten Bereichs. Für die anderen 9 gestillten Säuglinge wurden keine Prothrombinzeiten erhalten. Die Auswirkungen auf Frühgeborene wurden nicht untersucht.
Weibchen und Männchen mit reproduktivem Potenzial
Schwangerschaftstest
COUMADIN kann den Fötus schädigen [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
Überprüfen Sie den Schwangerschaftsstatus von Frauen im gebärfähigen Alter vor Beginn der COUMADIN-Therapie.
Empfängnisverhütung
Frauen
Raten Sie Frauen im gebärfähigen Alter, während der Behandlung und für mindestens 1 Monat nach der letzten Dosis von COUMADIN eine wirksame Verhütungsmethode anzuwenden.
Pädiatrische Verwendung
Angemessene und gut kontrollierte Studien mit COUMADIN wurden in keiner pädiatrischen Population durchgeführt, und die optimale Dosierung, Sicherheit und Wirksamkeit bei pädiatrischen Patienten ist nicht bekannt. Die pädiatrische Anwendung von COUMADIN basiert auf Daten und Empfehlungen für Erwachsene sowie auf begrenzt verfügbaren pädiatrischen Daten aus Beobachtungsstudien und Patientenregistern. Pädiatrische Patienten, denen COUMADIN 1 mg verabreicht wurde, sollten alle Aktivitäten oder Sportarten vermeiden, die zu traumatischen Verletzungen führen können.
Das sich entwickelnde hämostatische System bei Säuglingen und Kindern führt zu einer veränderten Physiologie der Thrombose und Reaktion auf Antikoagulanzien. Die Dosierung von Warfarin in der pädiatrischen Population variiert je nach Alter des Patienten, wobei Säuglinge im Allgemeinen die höchste und Jugendliche die niedrigste Milligramm-pro-Kilogramm-Dosis benötigen, um die Ziel-INRs aufrechtzuerhalten. Aufgrund des sich ändernden Warfarin-Bedarfs aufgrund des Alters, der Begleitmedikation, der Ernährung und des bestehenden Gesundheitszustands kann es bei pädiatrischen Patienten schwierig sein, INR-Zielbereiche zu erreichen und aufrechtzuerhalten, und häufigere INR-Bestimmungen werden empfohlen.
Die Blutungsraten variierten je nach Patientenpopulation und klinischem Versorgungszentrum in pädiatrischen Beobachtungsstudien und Patientenregistern.
Säuglinge und Kinder, die Vitamin-K-Ergänzungsnahrung, einschließlich Säuglingsanfangsnahrung, erhalten, können gegen eine Warfarin-Therapie resistent sein, während mit Muttermilch gefütterte Säuglinge empfindlich auf eine Warfarin-Therapie reagieren können.
Geriatrische Verwendung
Von der Gesamtzahl der Patienten, die Warfarin-Natrium in kontrollierten klinischen Studien erhielten, für die Daten zur Analyse verfügbar waren, waren 1885 Patienten (24,4 %) 65 Jahre und älter, während 185 Patienten (2,4 %) 75 Jahre und älter waren. Insgesamt wurden keine Unterschiede in der Wirksamkeit oder Sicherheit zwischen diesen Patienten und jüngeren Patienten beobachtet, aber eine größere Empfindlichkeit einiger älterer Personen kann nicht ausgeschlossen werden.
Patienten, die 60 Jahre oder älter sind, scheinen eine stärker als erwartete INR-Antwort auf die gerinnungshemmende Wirkung von Warfarin zu zeigen [siehe KLINISCHE PHARMAKOLOGIE ]. COUMADIN ist bei allen unbeaufsichtigten Patienten mit Senilität kontraindiziert. Seien Sie vorsichtig bei der Verabreichung von COUMADIN an ältere Patienten in jeder Situation oder mit jedem körperlichen Zustand, in dem ein zusätzliches Blutungsrisiko besteht. Erwägen Sie niedrigere Anfangs- und Erhaltungsdosen von COUMADIN bei älteren Patienten [siehe DOSIERUNG UND ANWENDUNG ].
Nierenfunktionsstörung
Die renale Clearance gilt als untergeordnete Determinante der gerinnungshemmenden Reaktion auf Warfarin. Bei Patienten mit eingeschränkter Nierenfunktion ist keine Dosisanpassung erforderlich. Weisen Sie Patienten mit eingeschränkter Nierenfunktion, die Warfarin einnehmen, an, ihre INR häufiger zu überwachen [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Leberfunktionsstörung
Eine eingeschränkte Leberfunktion kann die Reaktion auf Warfarin durch eine gestörte Synthese von Gerinnungsfaktoren und eine verminderte Metabolisierung von Warfarin verstärken. Bei der Anwendung von COUMADIN bei diesen Patienten ist Vorsicht geboten.
ÜBERDOSIS
Anzeichen und Symptome
Blutungen (z. B. Auftreten von Blut im Stuhl oder Urin, Hämaturie, übermäßige Menstruationsblutung, Meläna, Petechien, übermäßige Blutergüsse oder anhaltende Blutergüsse aufgrund oberflächlicher Verletzungen, unerklärlicher Abfall des Hämoglobins) sind eine Manifestation einer übermäßigen Antikoagulation.
Behandlung
Die Behandlung einer übermäßigen Antikoagulation richtet sich nach der Höhe der INR, dem Vorhandensein oder Nichtvorhandensein von Blutungen und den klinischen Umständen. Eine Aufhebung der Antikoagulation mit COUMADIN 2 mg kann durch Absetzen der Therapie mit COUMADIN 1 mg und, falls erforderlich, durch orale oder parenterale Verabreichung von Vitamin K1 erreicht werden.
Die Anwendung von Vitamin K1 reduziert das Ansprechen auf eine nachfolgende COUMADIN-Therapie und die Patienten können nach der schnellen Umkehrung einer verlängerten INR in einen thrombotischen Zustand vor der Behandlung zurückkehren. Die Wiederaufnahme der Verabreichung von COUMADIN 2 mg kehrt die Wirkung von Vitamin K um, und durch sorgfältige Dosisanpassung kann wieder eine therapeutische INR erreicht werden. Wenn eine schnelle erneute Antikoagulation angezeigt ist, kann Heparin für die Initialtherapie vorzuziehen sein.
Prothrombinkomplexkonzentrat (PCC), gefrorenes Frischplasma oder eine Behandlung mit aktiviertem Faktor VII können in Betracht gezogen werden, wenn die Notwendigkeit einer Aufhebung der Wirkung von COUMADIN 2 mg dringend ist. Mit der Verwendung von Blutprodukten ist ein Risiko für Hepatitis und andere Viruserkrankungen verbunden; PCC und aktivierter Faktor VII sind ebenfalls mit einem erhöhten Thromboserisiko verbunden. Daher sollten diese Präparate nur bei außergewöhnlichen oder lebensbedrohlichen Blutungsepisoden infolge einer Überdosierung von COUMADIN 2 mg angewendet werden.
KONTRAINDIKATIONEN
COUMADIN 1mg ist kontraindiziert bei:
COUMADIN 2 mg ist bei schwangeren Frauen kontraindiziert, außer bei schwangeren Frauen mit mechanischen Herzklappen, die ein hohes Risiko für Thromboembolien haben [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und Verwendung in bestimmten Bevölkerungsgruppen ]. COUMADIN 2 mg kann den Fötus schädigen, wenn es einer schwangeren Frau verabreicht wird. Die COUMADIN-Exposition während der Schwangerschaft verursacht ein bekanntes Muster schwerer angeborener Missbildungen (Warfarin-Embryopathie und Fetotoxizität), tödliche fötale Blutungen und ein erhöhtes Risiko für spontane Fehlgeburten und fötale Sterblichkeit. Wenn COUMADIN während der Schwangerschaft angewendet wird oder wenn die Patientin während der Einnahme dieses Arzneimittels schwanger wird, sollte die Patientin über die potenzielle Gefahr für einen Fötus informiert werden [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
COUMADIN ist kontraindiziert bei Patienten mit:
KLINISCHE PHARMAKOLOGIE
Wirkmechanismus
Warfarin wirkt durch Hemmung der Synthese von Vitamin-K-abhängigen Gerinnungsfaktoren, zu denen die Faktoren II, VII, IX und X sowie die gerinnungshemmenden Proteine C und S gehören. Vitamin K ist ein wesentlicher Cofaktor für die postribosomale Synthese des Vitamins K- abhängige Gerinnungsfaktoren. Vitamin K fördert die Biosynthese von γ-Carboxyglutaminsäureresten in den Proteinen, die für die biologische Aktivität essentiell sind. Es wird angenommen, dass Warfarin die Gerinnungsfaktorsynthese durch Hemmung der C1-Untereinheit des Vitamin-K-Epoxid-Reduktase (VKORC1)-Enzymkomplexes stört, wodurch die Regeneration von Vitamin-K1-Epoxid reduziert wird [siehe Pharmakogenomik ].
Pharmakodynamik
Eine gerinnungshemmende Wirkung tritt im Allgemeinen innerhalb von 24 Stunden nach der Gabe von Warfarin ein. Die maximale gerinnungshemmende Wirkung kann jedoch um 72 bis 96 Stunden verzögert sein. Die Wirkungsdauer einer Einzeldosis von racemischem Warfarin beträgt 2 bis 5 Tage. Die Wirkungen von COUMADIN 1 mg können stärker ausgeprägt sein, wenn sich die Wirkungen der täglichen Erhaltungsdosen überschneiden. Dies steht im Einklang mit den Halbwertszeiten der betroffenen Vitamin-K-abhängigen Gerinnungsfaktoren und Antikoagulationsproteine: Faktor II – 60 Stunden, VII – 4 bis 6 Stunden, IX – 24 Stunden, X – 48 bis 72 Stunden und Proteine C und S ungefähr 8 Stunden bzw. 30 Stunden.
Pharmakokinetik
COUMADIN ist ein racemisches Gemisch der R- und S-Enantiomere von Warfarin. Das S-Enantiomer zeigt beim Menschen eine 2- bis 5-mal höhere gerinnungshemmende Aktivität als das R-Enantiomer, hat aber im Allgemeinen eine schnellere Clearance.
Absorption
Warfarin wird nach oraler Verabreichung im Wesentlichen vollständig resorbiert, wobei die Spitzenkonzentration im Allgemeinen innerhalb der ersten 4 Stunden erreicht wird.
Verteilung
Warfarin verteilt sich in einem relativ kleinen scheinbaren Verteilungsvolumen von etwa 0,14 l/kg. Nach schneller intravenöser oder oraler Gabe einer wässrigen Lösung ist eine Verteilungsphase von 6 bis 12 Stunden zu unterscheiden. Ungefähr 99 % des Arzneimittels sind an Plasmaproteine gebunden.
Stoffwechsel
Die Elimination von Warfarin erfolgt fast ausschließlich durch Metabolisierung. Warfarin wird stereoselektiv durch mikrosomale Cytochrom P-450 (CYP450)-Enzyme der Leber zu inaktiven hydroxylierten Metaboliten (vorwiegender Weg) und durch Reduktasen zu reduzierten Metaboliten (Warfarinalkohole) mit minimaler gerinnungshemmender Aktivität metabolisiert. Zu den identifizierten Metaboliten von Warfarin gehören Dehydrowarfarin, zwei diastereoisomere Alkohole und 4'-, 6-, 7-, 8- und 10-Hydroxywarfarin. Zu den CYP450-Isozymen, die am Metabolismus von Warfarin beteiligt sind, gehören CYP2C9, 2C19, 2C8, 2C18, 1A2 und 3A4. CYP2C9, ein polymorphes Enzym, ist wahrscheinlich die Hauptform des menschlichen Leber-CYP450, das die gerinnungshemmende Aktivität von Warfarin in vivo moduliert. Patienten mit einer oder mehreren Varianten von CYP2C9-Allelen haben eine verringerte S-Warfarin-Clearance [siehe Pharmakogenomik ].
Ausscheidung
Die terminale Halbwertszeit von Warfarin nach einer Einzeldosis beträgt etwa 1 Woche; Die effektive Halbwertszeit reicht jedoch von 20 bis 60 Stunden, mit einem Mittelwert von etwa 40 Stunden. Die Clearance von R-Warfarin ist im Allgemeinen halb so groß wie die von S-Warfarin, daher ist die Halbwertszeit von Rwarfarin länger als die von S-Warfarin, da die Verteilungsvolumina ähnlich sind. Die Halbwertszeit von R-Warfarin reicht von 37 bis 89 Stunden, während die von S-Warfarin von 21 bis 43 Stunden reicht. Studien mit radioaktiv markierten Arzneimitteln haben gezeigt, dass bis zu 92 % der oral verabreichten Dosis im Urin wiedergefunden werden. Sehr wenig Warfarin wird unverändert im Urin ausgeschieden. Die Ausscheidung über den Urin erfolgt in Form von Metaboliten.
Geriatrische Patienten
Patienten, die 60 Jahre oder älter sind, scheinen eine stärker als erwartete INR-Reaktion auf die gerinnungshemmende Wirkung von Warfarin zu zeigen. Die Ursache für die erhöhte Empfindlichkeit gegenüber den gerinnungshemmenden Wirkungen von Warfarin in dieser Altersgruppe ist unbekannt, kann aber auf eine Kombination aus pharmakokinetischen und pharmakodynamischen Faktoren zurückzuführen sein. Begrenzte Informationen deuten darauf hin, dass es keinen Unterschied in der Clearance von S-Warfarin gibt; bei älteren Patienten kann es jedoch im Vergleich zu jüngeren zu einer leichten Abnahme der Clearance von R-Warfarin kommen. Daher ist mit zunehmendem Alter des Patienten normalerweise eine niedrigere Warfarin-Dosis erforderlich, um ein therapeutisches Antikoagulationsniveau zu erreichen [siehe DOSIERUNG UND ANWENDUNG ].
Asiatische Patienten
Asiatische Patienten benötigen möglicherweise niedrigere Anfangs- und Erhaltungsdosen von Warfarin. Eine nicht kontrollierte Studie mit 151 chinesischen ambulanten Patienten, die für verschiedene Indikationen auf Warfarin stabilisiert wurden, ergab einen mittleren täglichen Warfarinbedarf von 3,3 ± 1,4 mg, um einen INR von 2 bis 2,5 zu erreichen. Das Patientenalter war die wichtigste Determinante des Warfarinbedarfs bei diesen Patienten, wobei der Warfarinbedarf mit zunehmendem Alter progressiv abnahm.
Pharmakogenomik
CYP2C9- und VKORC1-Polymorphismen
Das S-Enantiomer von Warfarin wird hauptsächlich durch CYP2C9, ein polymorphes Enzym, zu 7-Hydroxywarfarin metabolisiert. Die Allele-Varianten CYP2C9*2 und CYP2C9*3 führen zu einer verminderten enzymatischen 7-Hydroxylierung von S-Warfarin in vitro durch CYP2C9. Die Häufigkeit dieser Allele bei Kaukasiern beträgt etwa 11 % bzw. 7 % für CYP2C9*2 und CYP2C9*3.
Andere CYP2C9-Allele, die mit einer reduzierten enzymatischen Aktivität assoziiert sind, treten mit geringerer Häufigkeit auf, darunter *5-, *6- und *11-Allele in Populationen afrikanischer Abstammung und *5-, *9- und *11-Allele bei Kaukasiern.
Warfarin reduziert die Regeneration von Vitamin K aus Vitamin-K-Epoxid im Vitamin-K-Zyklus durch Hemmung von VKOR, einem Multiprotein-Enzymkomplex. Bestimmte Einzelnukleotid-Polymorphismen im VKORC1-Gen (z. B. .1639G>A) wurden mit unterschiedlichen Warfarin-Dosisanforderungen in Verbindung gebracht.
Die VKORC1- und CYP2C9-Genvarianten erklären im Allgemeinen den größten Teil der bekannten Variabilität der Warfarin-Dosisanforderungen.
CYP2C9- und VKORC1-Genotypinformationen können, sofern verfügbar, bei der Auswahl der Anfangsdosis von Warfarin hilfreich sein [siehe DOSIERUNG UND ANWENDUNG ].
Klinische Studien
Vorhofflimmern
In fünf prospektiven, randomisierten, kontrollierten klinischen Studien mit 3711 Patienten mit nicht-rheumatischem Vorhofflimmern reduzierte Warfarin signifikant das Risiko einer systemischen Thromboembolie einschließlich Schlaganfall (siehe Tabelle 4). Die Risikoreduktion lag in allen zwischen 60 % und 86 %, mit Ausnahme einer Studie (CAFA: 45 %), die aufgrund veröffentlichter positiver Ergebnisse aus zwei dieser Studien vorzeitig beendet wurde. Die Inzidenz schwerer Blutungen lag in diesen Studien zwischen 0,6 % und 2,7 % (siehe Tabelle 4).
Studien an Patienten mit Vorhofflimmern und Mitralstenose deuten auf einen Nutzen der Antikoagulation mit COUMADIN hin [siehe DOSIERUNG UND ANWENDUNG ].
Mechanische und bioprothetische Herzklappen
In einer prospektiven, randomisierten, offenen, positiv kontrollierten Studie an 254 Patienten mit mechanischen Herzklappenprothesen wurde festgestellt, dass das thromboemboliefreie Intervall bei Patienten, die mit Warfarin allein behandelt wurden, signifikant länger war als bei Patienten, die mit Dipyridamol/Aspirin behandelt wurden (S
In einer prospektiven, unverblindeten klinischen Studie, in der mäßige (INR 2,65) und hochintensive (INR 9,0) Warfarin-Therapien bei 258 Patienten mit mechanischen Herzklappenprothesen verglichen wurden, traten Thromboembolien mit ähnlicher Häufigkeit in beiden Gruppen auf (4,0 und 3,7 Ereignisse pro 100). Patientenjahre). Größere Blutungen traten häufiger in der Gruppe mit hoher Intensität auf. Die Ergebnisse dieser Studie sind in Tabelle 6 dargestellt.
In einer randomisierten Studie mit 210 Patienten, in der zwei Intensitäten der Warfarin-Therapie (INR 2,0–2,25 vs. INR 2,5–4,0) über einen Zeitraum von drei Monaten nach dem Gewebeherzklappenersatz verglichen wurden, traten Thromboembolien in beiden Gruppen mit ähnlicher Häufigkeit auf (schwere embolische Ereignisse 2,0 % vs. 1,9 % und kleinere embolische Ereignisse 10,8 % vs. 10,2 %). Größere Blutungen traten bei 4,6 % der Patienten in der INR-Gruppe mit höherer Intensität auf, verglichen mit Null in der INR-Gruppe mit niedrigerer Intensität.
Herzinfarkt
WARIS (The Warfarin Re-Infarction Study) war eine doppelblinde, randomisierte Studie mit 1214 Patienten, die 2 bis 4 Wochen nach dem Infarkt mit Warfarin auf einen INR-Zielwert von 2,8 bis 4,8 behandelt wurden. Der primäre Endpunkt war eine Kombination aus Gesamtmortalität und rezidivierendem Infarkt. Als sekundärer Endpunkt wurden zerebrovaskuläre Ereignisse bewertet. Die mittlere Nachbeobachtungszeit der Patienten betrug 37 Monate. Die Ergebnisse für jeden Endpunkt separat, einschließlich einer Analyse des vaskulären Todes, sind in Tabelle 7 aufgeführt.
WARIS II (The Warfarin, Aspirin, Re-Infarction Study) war eine unverblindete, randomisierte Studie mit 3630 Patienten, die wegen eines akuten Myokardinfarkts ins Krankenhaus eingeliefert wurden und mit Warfarin auf einen INR-Zielwert von 2,8 bis 4,2, Aspirin 160 mg pro Tag oder Warfarin auf a behandelt wurden Ziel INR 2,0 bis 2,5 plus 75 mg Aspirin pro Tag vor der Entlassung aus dem Krankenhaus. Der primäre Endpunkt war eine Kombination aus Tod, nicht tödlichem Reinfarkt oder thromboembolischem Schlaganfall. Die mittlere Beobachtungsdauer betrug etwa 4 Jahre. Die Ergebnisse für WARIS II sind in Tabelle 8 aufgeführt.
In den beiden Gruppen, die Warfarin erhielten, traten ungefähr viermal so viele Episoden schwerer Blutungen auf wie in der Gruppe, die nur Aspirin erhielt. Episoden schwerer Blutungen waren bei Patienten, die Aspirin plus Warfarin erhielten, nicht häufiger als bei Patienten, die Warfarin allein erhielten, aber die Inzidenz kleinerer Blutungsepisoden war in der Gruppe mit kombinierter Therapie höher.
INFORMATIONEN ZUM PATIENTEN
COUMADIN® (COU-ma-din) (Warfarin-Natrium)
Was sind die wichtigsten Informationen, die ich über COUMADIN 5mg wissen sollte?
COUMADIN kann Blutungen verursachen, die schwerwiegend sein und manchmal zum Tod führen können. Dies liegt daran, dass COUMADIN ein blutverdünnendes Arzneimittel ist, das die Wahrscheinlichkeit der Bildung von Blutgerinnseln in Ihrem Körper verringert.
Informieren Sie Ihren Arzt, wenn Sie eines dieser Arzneimittel einnehmen. Fragen Sie Ihren Arzt, wenn Sie sich nicht sicher sind, ob Ihr Arzneimittel zu den oben aufgeführten gehört.
Viele andere Arzneimittel können mit COUMADIN 1 mg interagieren und die von Ihnen benötigte Dosis beeinflussen oder die Nebenwirkungen von COUMADIN 1 mg verstärken. Ändern oder setzen Sie keines Ihrer Arzneimittel ab und beginnen Sie nicht mit neuen Arzneimitteln, bevor Sie mit Ihrem Arzt gesprochen haben.
Nehmen Sie während der Einnahme von COUMADIN keine anderen Arzneimittel ein, die Warfarin-Natrium enthalten.
Siehe „Was sind die möglichen Nebenwirkungen von COUMADIN 1 mg?“ für weitere Informationen zu Nebenwirkungen.
Was ist COUMADIN?
COUMADIN ist ein verschreibungspflichtiges Arzneimittel zur Behandlung von Blutgerinnseln und zur Verringerung der Wahrscheinlichkeit, dass sich Blutgerinnsel in Ihrem Körper bilden. Blutgerinnsel können einen Schlaganfall, Herzinfarkt oder andere schwerwiegende Erkrankungen verursachen, wenn sie sich in den Beinen oder der Lunge bilden.
Wer sollte COUMADIN nicht einnehmen?
Nehmen Sie COUMADIN 5 mg nicht ein, wenn:
Vor der Einnahme von COUMADIN
Informieren Sie Ihren Arzt über alle Ihre Erkrankungen, auch wenn Sie:
Informieren Sie alle Ihre Gesundheitsdienstleister und Zahnärzte, dass Sie COUMADIN einnehmen. Sie sollten mit dem Arzt sprechen, der Ihnen COUMADIN 1 mg verschrieben hat, bevor Sie es haben irgendein Chirurgie oder Zahnbehandlung. Möglicherweise muss Ihr COUMADIN für kurze Zeit abgesetzt oder Ihre Dosis angepasst werden.
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen, einschließlich verschreibungspflichtiger und rezeptfreier Arzneimittel, Vitamine und Kräuterergänzungen. Einige Ihrer anderen Arzneimittel können die Wirkungsweise von COUMADIN beeinflussen. Bestimmte Arzneimittel können Ihr Blutungsrisiko erhöhen. Sehen „Was sind die wichtigsten Informationen, die ich über COUMADIN wissen sollte?“
Wie sollte ich COUMADIN 1 mg einnehmen?
Was sollte ich während der Einnahme von COUMADIN 5 mg vermeiden?
Welche Nebenwirkungen kann COUMADIN haben?
COUMADIN kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Dies sind nicht alle Nebenwirkungen von COUMADIN. Weitere Informationen erhalten Sie von Ihrem Arzt oder Apotheker. Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1..800-FDA-1088 melden.
Wie ist COUMADIN 5mg aufzubewahren?
Bewahren Sie COUMADIN 1mg und alle Arzneimittel außerhalb der Reichweite von Kindern auf.
Allgemeine Informationen zur sicheren und wirksamen Anwendung von COUMADIN.
Medikamente werden manchmal für andere als die in einem Medikationsleitfaden aufgeführten Zwecke verschrieben. Verwenden Sie COUMADIN 5mg nicht für einen Zustand, für den es nicht verschrieben wurde. Geben Sie COUMADIN 2 mg nicht an andere Personen weiter, selbst wenn diese die gleichen Symptome wie Sie haben. Es kann ihnen schaden.
Sie können Ihren Arzt oder Apotheker um Informationen über COUMADIN bitten, die für Angehörige der Gesundheitsberufe bestimmt sind.
Was sind die Inhaltsstoffe von COUMADIN 1 mg Tabletten?
Wirkstoff: Warfarin-Natrium
Inaktive Zutaten : Lactose, Stärke und Magnesiumstearat, zusätzlich:
1 mg: D&C Red Nr. 6 Bariumsee
2 mg: FD&C Blau Nr. 2 Aluminiumlack und FD&C Rot Nr. 40 Aluminiumlack
2,5 mg: D&C Gelb Nr. 10 Aluminiumlack und FD&C Blau Nr. 1 Aluminiumlack
3 mg: FD&C Gelb Nr. 6 Aluminiumlack, FD&C Blau Nr. 2 Aluminiumlack und FD&C Rot Nr. 40 Aluminiumlack
4 mg: FD&C Blau Nr. 1 Aluminiumlack
5 mg: FD&C Yellow Nr. 6 Aluminiumlack
mg: FD&C Yellow Nr. 6 Aluminiumlack und FD&C Blue Nr. 1 Aluminiumlack
7,5 mg: D&C Gelb Nr. 10 Aluminiumlack und FD&C Gelb Nr. 6 Aluminiumlack
Dieser Medikationsleitfaden wurde von der US Food and Drug Administration genehmigt.