Mellaril 10mg, 25mg, 50mg, 100mg Thioridazine Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Mellaril Topper und wie wird es angewendet?
Mellaril Topper ist ein verschreibungspflichtiges Arzneimittel zur Behandlung der Symptome von Schizophrenie und depressiven Störungen. Mellaril 25 mg Topper kann allein oder zusammen mit anderen Medikamenten verwendet werden.
Welche Nebenwirkungen kann Mellaril Topper haben?
Mellaril 100 mg Topper kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigsten Nebenwirkungen von Mellaril Topper gehören:
Teilen Sie dem Arzt mit, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Mellaril 10 mg Topper. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
WARNUNG
MELLARIL® (THIORIDAZIN HCl) HAT ZEIGEND, DASS DAS QTc-INTERVALL DOSISABHÄNGIG VERLÄNGERT WIRD, UND ARZNEIMITTEL MIT DIESEM POTENZIAL, EINSCHLIESSLICH MELLARIL (Thioridazin HCl) WURDEN MIT ARRHYTHMIEN VOM TORSADE-DE-POINTES-TYP UND PLÖTZLICHEM TOD IN VERBINDUNG GESTELLT. AUFGRUND SEINES POTENZIALS FÜR ERHEBLICHE, MÖGLICHERWEISE LEBENSBEDROHENDE, PROARHYTHMISCHE WIRKUNGEN SOLLTE MELLARIL (Thioridazin-hcl) DER VERWENDUNG BEI DER BEHANDLUNG SCHIZOPHRENER PATIENTEN VORBEHALTEN WERDEN, DIE KEINE AKZEPTABLE REAKTION AUF ANGEMESSENE BEHANDLUNGSKURSE MIT ANDEREN ANTIPSYCHOTIKEN ZEIGEN, ENTWEDER WEIL VON UNZUREICHENDER WIRKSAMKEIT ODER DER UNFÄHIGKEIT, EINE WIRKSAME DOSIS ZU ERREICHEN, AUFGRUND VON UNTOLERIERBAREN NEBENWIRKUNGEN DIESER ARZNEIMITTEL. (SEHEN WARNHINWEISE, KONTRAINDIKATIONEN, UND INDIKATIONEN ).
BEZEICHNUNG
Mellaril® (Thioridazin-HCl) ist 2-Methylmercapto-10-[2-(N-methyl-2-piperidyl)ethyl]phenothiazin.
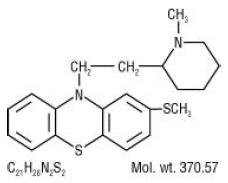
10 mg, 15 mg, 25 mg, 50 mg, 100 mg, 150 mg und 200 mg Tabletten
Wirkstoff: Thioridazin-HCl, USP
10-mg-Tabletten
Inaktive Zutaten: Akazie, Calciumsulfatdihydrat, Carnaubawachs, D&C Yellow #10, FD&C Blue #1, FD&C Yellow #6, Gelatine, Lactose, Methylparaben, Povidon, Propylparaben, Natriumbenzoat, Stärke, Stearinsäure, Saccharose, synthetisches schwarzes Eisenoxid, Talk , Titandioxid und andere Inhaltsstoffe.
15-mg-Tabletten
Inaktive Zutaten: Akazie, Calciumsulfatdihydrat, Carnaubawachs, D&C Red #7, Gelatine, Laktose, Methylparaben, Povidon, Propylparaben, Stärke, Stearinsäure, Saccharose, synthetisches schwarzes Eisenoxid, Talk, Titandioxid und andere Inhaltsstoffe.
25-mg-Tabletten
Inaktive Zutaten: Akazie, Calciumsulfatdihydrat, Carnaubawachs, Gelatine, Lactose, Methylparaben, Povidon, Propylparaben, Natriumbenzoat, Stärke, Stearinsäure, Saccharose, synthetisches schwarzes Eisenoxid, synthetisches Eisenoxid, Talk, Titandioxid und andere Inhaltsstoffe.
50-mg-Tabletten
Inaktive Zutaten: Akazie, Calciumsulfatdihydrat, Carnaubawachs, Gelatine, Lactose, Natriumbenzoat, Stärke, Stearinsäure, Saccharose, synthetisches schwarzes Eisenoxid, Talk, Titandioxid und andere Inhaltsstoffe.
100-mg-Tabletten
Inaktive Zutaten: Akazie, Calciumsulfatdihydrat, Carnaubawachs, D&C Yellow #10, FD&C Blue #1, FD&C Blue #2, FD&C Yellow #6, Lactose, Methylparaben, Povidon, Propylparaben, Natriumbenzoat, Sorbit, Stärke, Stearinsäure, Saccharose, synthetisch schwarzes Eisenoxid, Talk, Titandioxid und andere Inhaltsstoffe.
150-mg-Tabletten
Inaktive Zutaten: Akazie, Calciumsulfatdihydrat, Carnaubawachs, D&C Yellow #10, FD&C Green #3, FD&C Yellow #6, Lactose, Methylparaben, Povidon, Propylparaben, Natriumbenzoat, Stärke, Stearinsäure, Saccharose, synthetisches schwarzes Eisenoxid, Talk, Titan Dioxid und andere Zutaten.
200-mg-Tabletten
Inaktive Zutaten: Akazie, Ammoniumcalciumalginat, Calciumsulfatdihydrat, Carnaubawachs, kolloidales Siliciumdioxid, D&C Red #7, Laktose, Magnesiumstearat, Methylparaben, Povidon, Propylparaben, Natriumbenzoat, Stärke, Stearinsäure, Saccharose, synthetisches schwarzes Eisenoxid, Talkum, Titandioxid und andere Inhaltsstoffe.
30 mg/ml und 100 mg/ml Lösung zum Einnehmen (Konzentrat)
Wirkstoff: Thioridazin-HCl, USP
30 mg/ml Lösung zum Einnehmen (Konzentrat)
Inaktive Zutaten: Alkohol, 3,0 %, Aroma, Methylparaben, Propylparaben, gereinigtes Wasser und Sorbitlösung. Kann Natriumhydroxid oder Salzsäure enthalten, um den pH-Wert einzustellen.
100 mg/ml Lösung zum Einnehmen (Konzentrat)
Inaktive Zutaten: Alkohol, 4,2 %, Aroma, Glycerin, Methylparaben, Propylparaben, gereinigtes Wasser, Sorbitlösung und Saccharose. Kann Natriumhydroxid oder Salzsäure enthalten, um den pH-Wert einzustellen.
5 mg/ml und 20 mg/ml Suspension zum Einnehmen
Wirkstoff: jeder ml enthält Thioridazin, USP, entsprechend 5 mg bzw. 20 mg Thioridazin-HCl, USP.
5 mg/ml Suspension zum Einnehmen
Inaktive Zutaten: Carbomer 934, Aroma, Polysorbat 80, gereinigtes Wasser, Natriumhydroxid und Saccharose.
20 mg/ml Suspension zum Einnehmen
Inaktive Zutaten: Carbomer 934, D&C Yellow Nr. 10, FD&C Yellow Nr. 6, Aroma, Polysorbat 80, gereinigtes Wasser, Natriumhydroxid und Saccharose.
INDIKATIONEN
Mellaril® (Thioridazin-HCl) ist für die Behandlung schizophrener Patienten indiziert, die nicht ausreichend auf eine Behandlung mit anderen Antipsychotika ansprechen. Aufgrund des Risikos erheblicher, möglicherweise lebensbedrohlicher, proarrhythmischer Wirkungen bei der Behandlung mit Mellaril (Thioridazin-hcl) sollte Mellaril (Thioridazin-hcl) nur bei Patienten angewendet werden, die auch auf eine Behandlung mit geeigneten Behandlungszyklen anderer Antipsychotika nicht ausreichend angesprochen haben wegen unzureichender Wirksamkeit bzw
die Unfähigkeit, eine wirksame Dosis aufgrund von nicht tolerierbaren Nebenwirkungen dieser Arzneimittel zu erreichen. Daher wird vor Beginn der Behandlung mit Mellaril (Thioridazin-HCl) dringend empfohlen, dass ein Patient mindestens 2 Studien mit jeweils einem anderen Antipsychotikum in angemessener Dosis und über eine angemessene Dauer erhält (siehe Abschnitt 4.1). WARNUNGEN und KONTRAINDIKATIONEN ).
Der verschreibende Arzt sollte sich jedoch darüber im Klaren sein, dass Mellaril (Thioridazin hcl) nicht systematisch in kontrollierten Studien bei therapierefraktären schizophrenen Patienten untersucht wurde und seine Wirksamkeit bei solchen Patienten unbekannt ist.
DOSIERUNG UND ANWENDUNG
Da Mellaril (Thioridazin-HCl) mit einer dosisabhängigen Verlängerung des QTc-Intervalls verbunden ist, was ein potenziell lebensbedrohliches Ereignis darstellt, sollte seine Anwendung schizophrenen Patienten vorbehalten bleiben, die nicht angemessen auf eine Behandlung mit anderen Antipsychotika ansprechen. Die Dosierung muss individuell angepasst werden und die kleinste wirksame Dosierung sollte für jeden Patienten bestimmt werden (vgl INDIKATIONEN und WARNUNGEN ).
Erwachsene
Die übliche Anfangsdosis für erwachsene Schizophrenie-Patienten beträgt 50-100 mg dreimal täglich, mit einer allmählichen Erhöhung auf maximal 800 mg täglich, falls erforderlich. Sobald eine wirksame Kontrolle der Symptome erreicht ist, kann die Dosis schrittweise reduziert werden, um die minimale Erhaltungsdosis zu bestimmen. Die tägliche Gesamtdosis liegt zwischen 200 und 800 mg, aufgeteilt in zwei bis vier Dosen.
Pädiatrische Patienten
Für pädiatrische Patienten mit Schizophrenie, die auf andere Arzneimittel nicht ansprechen, beträgt die empfohlene Anfangsdosis 0,5 mg/kg/Tag, verteilt auf mehrere Dosen. Die Dosierung kann schrittweise erhöht werden, bis eine optimale therapeutische Wirkung erzielt oder die Höchstdosis von 3 mg/kg/Tag erreicht ist.
WIE GELIEFERT
Mellaril® (Thioridazin HCl) Tabletten
10mg
Hellgrüne, überzogene Tabletten; Auf der einen Seite Aufdruck „S“, auf der anderen Seite Aufdruck „78-2“ in Schwarz.
100er Flasche .................................................. NDC 0078-0002-05 1000er Flasche .......................................... NDC 0078-0002-09 Einheitsdosispackung mit 100 ............ NDC 0078-0002-06
15mg
Rosa, überzogene Tabletten; „S“-Aufdruck auf einer Seite, „78-8“-Aufdruck auf der anderen Seite, in Schwarz.
100er Flasche .................................................. NDC 0078-0008-05
25mg
Hellbraune, überzogene Tabletten; „S“ auf der einen Seite, „MELLARIL (thioridazine hcl) 25“ auf der anderen Seite in Schwarz.
100er Flasche .................................................. NDC 0078-0003-05 1000er Flasche .......................................... NDC 0078-0003-09 Einzeldosispackung mit 100 ............ NDC 0078-0003-06
50mg
Weiße, überzogene Tabletten; „S“ auf einer Seite bedruckt, „MELLARIL (Thioridazin hcl) 50'' auf der anderen Seite bedruckt, in Schwarz.
100er Flasche .................................................. NDC 0078-0004-05 1000er Flasche .......................................... NDC 0078-0004-09 Einheitsdosispackung mit 100 ............ NDC 0078-0004-06
100mg
Hellgrüne, überzogene Tabletten; „^4&“ auf der einen Seite, „MELLARIL (thioridazine hcl) 100'' auf der anderen Seite in Schwarz.
100er Flasche .................................................. NDC 0078-0005-05 1000er Flasche .......................................... NDC 0078-0005-09 Einheitsdosispackung mit 100 ............ NDC 0078-0005-06
150mg
Gelbe, überzogene Tabletten; „S“ auf der einen Seite, „MELLARIL (thioridazine hcl) 150“ auf der anderen Seite in Schwarz.
100er Flasche .................................................. NDC 0078-0006-05
200mg
Rosafarbene, überzogene Tabletten mit dem Aufdruck „^4&“ auf einer Seite und dem Aufdruck „MELLARIL (thioridazine hcl) 200“ auf der anderen Seite in Schwarz.
100er Flasche .................................................. NDC 0078-0007-05 Einheitsdosispackung mit 100 ............ NDC 0078-0007-06
Speichern und abgeben
Unter 30 °C (86 °F); dichter Behälter.
Mellaril® (Thioridazin-HCl) Lösung zum Einnehmen (Konzentrat)
30 mg/ml
Eine klare, strohgelbe Flüssigkeit mit kirschartigem Geruch. Jeder ml enthält 30 mg Thioridazinhydrochlorid, USP, Alkohol, 3,0 Vol.-%. Unmittelbarer Behälter: Braunglasflaschen mit 4 fl. oz. (118 ml) wie folgt: 4 fl. Unze. oz. Flaschen, in Kartons mit 12 Flaschen, mit einem begleitenden Tropfer, graduiert, um 10 mg, 25 mg und 50 mg Thioridazinhydrochlorid, USP ( NDC 0078-0001-31).
100 mg/ml
Eine klare, hellgelbe Flüssigkeit mit erdbeerartigem Geruch. Jeder ml enthält 100 mg Thioridazinhydrochlorid, USP, Alkohol, 4,2 Vol.-%. Unmittelbarer Behälter: Braunglasflaschen mit 4 fl. oz. (118 ml), in Kartons mit 12 Flaschen, mit einem begleitenden Tropfer, der graduiert ist, um 100 mg, 150 mg und 200 mg Thioridazinhydrochlorid, USP ( NDC 0078-0009-31).
Speichern und abgeben
Unter 30 °C (86 °F); dichte, braune Glasflasche.
Die Lösung zum Einnehmen (Konzentrat) kann mit destilliertem Wasser, angesäuertem Leitungswasser oder geeigneten Säften verdünnt werden. Jede Dosis sollte unmittelbar vor der Verabreichung entsprechend verdünnt werden – die Herstellung und Aufbewahrung von Großverdünnungen wird nicht empfohlen.
Mellaril (Thioridazin hcl) -S® (Thioridazin) Suspension zum Einnehmen
5 mg/ml
Eine cremefarbene Suspension mit Buttergeschmack und Pfefferminzgeruch. Jeder ml enthält Thioridazin, USP, entsprechend 5 mg Thioridazinhydrochlorid, USP. Butterfruchtgeschmack in Pintflaschen (NDC 0078-0068-33).
20 mg/ml
Eine gelbe Suspension mit Buttergeschmack und Pfefferminzgeruch. Jeder ml enthält Thioridazin, USP, entsprechend 20 mg Thioridazinhydrochlorid, USP. Butterfruchtgeschmack in Pintflaschen (NDC 0078-0069-33).
Speichern und abgeben
Unter 25 °C (77 °F); dichte, braune Glasflasche.
Zusätzliche Informationen für Ärzte. Novartis Pharmaceuticals Corporation, East Hanover, New Jersey 07936. Überarbeitet: Juni 2000.
NEBENWIRKUNGEN
In den empfohlenen Dosierungsbereichen mit Mellaril® (Thioridazin-HCl) sind die meisten Nebenwirkungen leicht und vorübergehend.
Zentrales Nervensystem: Gelegentlich kann es zu Schläfrigkeit kommen, insbesondere wenn zu Beginn der Behandlung hohe Dosen verabreicht werden. Im Allgemeinen neigt dieser Effekt dazu, bei Fortführung der Therapie oder einer Verringerung der Dosierung abzuklingen. Pseudoparkinsonismus und andere extrapyramidale Symptome können auftreten, sind aber selten. Nächtliche Verwirrtheit, Hyperaktivität, Lethargie, psychotische Reaktionen, Unruhe und Kopfschmerzen wurden berichtet, sind aber äußerst selten.
Vegetatives Nervensystem: Mundtrockenheit, verschwommenes Sehen, Verstopfung, Übelkeit, Erbrechen, Durchfall, verstopfte Nase und Blässe wurden beobachtet.
Hormonsystem: Galaktorrhoe, Milchstau, Amenorrhoe, Hemmung der Ejakulation und periphere Ödeme wurden beschrieben.
Haut: Dermatitis und Hautausschläge vom Urtikaria-Typ wurden selten beobachtet. Lichtempfindlichkeit ist äußerst selten.
Herz-Kreislauf-System: Mellaril (Thioridazin hcl) bewirkt eine dosisabhängige Verlängerung des QTc-Intervalls, was mit der Fähigkeit verbunden ist, Arrhythmien vom Torsade-de-Pointes-Typ, eine potenziell tödliche polymorphe ventrikuläre Tachykardie und plötzlichen Herztod zu verursachen (vgl WARNUNGEN ). Sowohl Arrhythmien vom Torsade-de-Pointes-Typ als auch plötzlicher Herztod wurden im Zusammenhang mit Mellaril (Thioridazin-HCl) berichtet. Ein kausaler Zusammenhang zwischen diesen Ereignissen und der Therapie mit Mellaril (Thioridazin-HCl) wurde nicht hergestellt, aber angesichts der Fähigkeit von Mellaril (Thioridazin-HCl), das QTc-Intervall zu verlängern, ist ein solcher Zusammenhang möglich. Andere EKG-Veränderungen wurden berichtet (siehe Phenothiazin-Derivate: Kardiovaskuläre Wirkungen ).

Sonstiges: Nach Verabreichung von Mellaril (Thioridazin-HCl) wurden seltene Fälle berichtet, die als Parotisschwellung beschrieben wurden.
Berichte nach der Einführung
Dies sind freiwillige Meldungen von unerwünschten Ereignissen, die zeitlich mit Mellaril (Thioridazin-HCl) in Zusammenhang stehen und seit der Markteinführung eingegangen sind, und es besteht möglicherweise kein kausaler Zusammenhang zwischen der Anwendung von Mellaril (Thioridazin-HCl) und diesen Ereignissen: Priapismus.
Phenothiazin-Derivate
Es sollte beachtet werden, dass Wirksamkeit, Indikationen und unerwünschte Wirkungen bei den verschiedenen Phenothiazinen unterschiedlich sind. Es wurde berichtet, dass das Alter die Toleranz gegenüber Phenothiazinen senkt. Die häufigsten neurologischen Nebenwirkungen bei diesen Patienten sind Parkinsonismus und Akathisie. Es scheint ein erhöhtes Risiko für Agranulozytose und Leukopenie in der geriatrischen Bevölkerung zu geben. Der Arzt sollte sich darüber im Klaren sein, dass Folgendes mit einem oder mehreren Phenothiazinen aufgetreten ist und bei jeder Anwendung eines dieser Arzneimittel berücksichtigt werden sollte:
Autonome Reaktionen: Miosis, Obstipation, Anorexie, paralytischer Ileus.
Hautreaktionen: Erythem, exfoliative Dermatitis, Kontaktdermatitis.
Blutkrankheiten: Agranulozytose, Leukopenie, Eosinophilie, Thrombozytopenie, Anämie, aplastische Anämie, Panzytopenie.
Allergische Reaktionen: Fieber, Kehlkopfödem, angioneurotisches Ödem, Asthma.
Hepatotoxizität: Gelbsucht, Gallenstauung.
Kardiovaskuläre Wirkungen: Bei Patienten, die Phenothiazine erhielten, wurden Veränderungen im Endbereich des Elektrokardiogramms beobachtet, die eine Verlängerung des QT-Intervalls, eine Senkung und Inversion der T-Welle sowie das Auftreten einer Welle, die vorläufig als Bifid-T-Welle oder U-Welle identifiziert wurde, umfassen Mellaril (Thioridazin-HCl). Bisher scheinen diese auf eine veränderte Repolarisation zurückzuführen zu sein, die nicht mit einer Myokardschädigung zusammenhängt und reversibel ist. Nichtsdestotrotz wurde eine signifikante Verlängerung des QT-Intervalls mit schweren ventrikulären Arrhythmien und plötzlichem Herztod in Verbindung gebracht (vgl WARNUNGEN ). Es wurde über Hypotonie berichtet, die selten zu einem Herzstillstand führte.
Extrapyramidale Symptome: Akathisie, Agitiertheit, motorische Unruhe, dystonische Reaktionen, Trismus, Torticollis, Opisthotonus, Augenkrisen, Tremor, Muskelstarre, Akinesie.
Spätdyskinesie: Die chronische Anwendung von Neuroleptika kann mit der Entwicklung einer tardiven Dyskinesie einhergehen. Die hervorstechenden Merkmale dieses Syndroms sind in beschrieben WARNUNGEN Abschnitt und danach.
Das Syndrom ist gekennzeichnet durch unwillkürliche choreoathetoide Bewegungen, die auf unterschiedliche Weise Zunge, Gesicht, Mund, Lippen oder Kiefer betreffen (z. B. Vorstehen der Zunge, Aufblähen der Wangen, Verziehen des Mundes, Kaubewegungen), Rumpf und Extremitäten. Die Schwere des Syndroms und der Grad der verursachten Beeinträchtigung sind sehr unterschiedlich.
Das Syndrom kann entweder während der Behandlung, nach Dosisreduktion oder nach Absetzen der Behandlung klinisch erkennbar werden. Bewegungen können an Intensität verlieren und ganz verschwinden, wenn eine weitere Behandlung mit Neuroleptika ausgesetzt wird. Es wird allgemein angenommen, dass eine Reversibilität eher nach kurzer als nach langfristiger Neuroleptika-Exposition eintritt. Daher ist die Früherkennung von tardiven Dyskinesien wichtig. Um die Wahrscheinlichkeit zu erhöhen, dass das Syndrom zum frühestmöglichen Zeitpunkt erkannt wird, sollte die Dosis des Neuroleptikums regelmäßig reduziert werden (falls klinisch möglich) und der Patient auf Anzeichen der Erkrankung beobachtet werden. Dieses Manöver ist kritisch, da Neuroleptika die Anzeichen des Syndroms maskieren können.
Malignes neuroleptisches Syndrom (NMS): Die chronische Anwendung von Neuroleptika kann mit der Entwicklung eines malignen neuroleptischen Syndroms in Verbindung gebracht werden. Die hervorstechenden Merkmale dieses Syndroms sind in beschrieben WARNUNGEN Abschnitt und danach. Klinische Manifestationen von NMS sind Hyperpyrexie, Muskelrigidität, veränderter Geisteszustand und Anzeichen einer autonomen Instabilität (unregelmäßiger Puls oder Blutdruck, Tachykardie, Diaphorese und Herzrhythmusstörungen).
Endokrine Störungen: Menstruationsstörungen, veränderte Libido, Gynäkomastie, Laktation, Gewichtszunahme, Ödeme. Es wurden falsch positive Schwangerschaftstests gemeldet.
Harnstörungen: Retention, Inkontinenz.
Andere: Hyperpyrexie. Es wurde über Verhaltenseffekte berichtet, die auf eine paradoxe Reaktion hindeuten. Dazu gehören Aufregung, bizarre Träume, Verschlimmerung von Psychosen und toxische Verwirrtheitszustände. In jüngerer Zeit wurde ein besonderes Haut-Augen-Syndrom als Nebenwirkung nach Langzeitbehandlung mit Phenothiazinen erkannt. Diese Reaktion ist gekennzeichnet durch eine fortschreitende Pigmentierung von Bereichen der Haut oder der Bindehaut und/oder begleitet von einer Verfärbung der freigelegten Sklera und Hornhaut. Es wurde auch über Trübungen der vorderen Linse und Hornhaut berichtet, die als unregelmäßig oder sternförmig beschrieben wurden. Systemisches Lupus-erythematodes-ähnliches Syndrom.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Reduzierte Cytochrom-P450-2D6-Isozymaktivität, Arzneimittel, die dieses Isozym hemmen (z. B. Fluoxetin und Paroxetin) und bestimmte andere Arzneimittel (z. B. Fluvoxamin, Propranolol und Pindolol) scheinen den Metabolismus von Thioridazin merklich zu hemmen. Es ist zu erwarten, dass die daraus resultierenden erhöhten Thioridazinspiegel die mit Mellaril (Thioridazin hcl) verbundene Verlängerung des QTc-Intervalls verstärken und das Risiko schwerer, möglicherweise tödlicher Herzrhythmusstörungen, wie Arrhythmien vom Torsade-de-Pointes-Typ, erhöhen können. Ein solches erhöhtes Risiko kann sich auch aus der additiven Wirkung der gleichzeitigen Verabreichung von Mellaril (Thioridazin-HCl) mit anderen Wirkstoffen ergeben, die das QTc-Intervall verlängern. Daher ist Mellaril (Thioridazin hcl) mit diesen Arzneimitteln kontraindiziert sowie bei Patienten, die etwa 7 % der Normalbevölkerung ausmachen und von denen bekannt ist, dass sie einen genetischen Defekt haben, der zu einer verminderten Aktivität von P450 2D6 führt (siehe WARNUNGEN und KONTRAINDIKATIONEN ).
Medikamente, die Cytochrom P450 2D6 hemmen
In einer Studie mit 19 gesunden männlichen Probanden, die 6 langsame und 13 schnelle Hydroxylatoren von Debrisoquin umfasste, führte eine orale Einzeldosis von 25 mg Thioridazin zu einer 2,4-fach höheren Cmax und einer 4,5-fach höheren AUC für Thioridazin im Vergleich zu den langsamen Hydroxylatoren schnelle Hydroxylatoren. Es wird angenommen, dass die Geschwindigkeit der Debrisoquin-Hydroxylierung vom Grad der Cytochrom-P450-2D6-Isozymaktivität abhängt. Somit legt diese Studie nahe, dass Arzneimittel, die P450 2D6 hemmen, oder das Vorhandensein von reduzierten Aktivitätsspiegeln dieses Isozyms erhöhte Plasmaspiegel von Thioridazin erzeugen. Daher sind die gleichzeitige Anwendung von Arzneimitteln, die P450 2D6 hemmen, mit Mellaril (Thioridazin-hcl) und die Anwendung von Mellaril (Thioridazin-hcl) bei Patienten mit bekannter verminderter Aktivität von P450 2D6 kontraindiziert.
Arzneimittel, die die Clearance von Mellaril® (Thioridazin hcl) durch andere Mechanismen reduzieren
Fluvoxamin: Die Wirkung von Fluvoxamin (25 mg zweimal täglich für eine Woche) auf die Steady-State-Konzentration von Thioridazin wurde bei 10 stationären männlichen Patienten mit Schizophrenie untersucht. Die Konzentrationen von Thioridazin und seinen beiden aktiven Metaboliten, Mesoridazin und Sulforidazin, stiegen nach gleichzeitiger Gabe von Fluvoxamin um das Dreifache an. Fluvoxamin und Mellaril (Thioridazin-HCl) sollten nicht gleichzeitig verabreicht werden.
Propranolol: Es wurde berichtet, dass die gleichzeitige Verabreichung von Propranolol (100–800 mg täglich) zu einem Anstieg der Plasmaspiegel von Thioridazin (ca. 50 %–400 %) und seinen Metaboliten (ca. 80 %–300 %) führt. Propranolol und Mellaril (Thioridazin-HCl) sollten nicht gleichzeitig verabreicht werden.
Pindolol: Die gleichzeitige Verabreichung von Pindolol und Thioridazin führte zu moderaten, dosisabhängigen Anstiegen der Serumspiegel von Thioridazin und zwei seiner Metaboliten sowie zu höheren Pindololspiegeln im Serum als erwartet. Pindolol und Mellaril (Thioridazin-HCl) sollten nicht gleichzeitig verabreicht werden.
Medikamente, die das QTc-Intervall verlängern
Es liegen keine Studien zur gleichzeitigen Anwendung von Mellaril (Thioridazin-hcl) und anderen Arzneimitteln vor, die das QTc-Intervall verlängern. Es wird jedoch erwartet, dass eine solche gleichzeitige Verabreichung zu einer zusätzlichen Verlängerung des QTc-Intervalls führen würde, und daher ist eine solche Anwendung kontraindiziert.
WARNUNGEN
Potenzial für proarrhythmische Effekte
AUFGRUND DES POTENZIALS FÜR ERHEBLICHE, MÖGLICHERWEISE LEBENSBEDROHENDE, PROARHYTHMISCHE WIRKUNGEN BEI DER BEHANDLUNG MIT MELLARIL® (THIORIDAZIN-HCl) SOLLTE MELLARIL (Thioridazin-HCl) DER VERWENDUNG IN DER BEHANDLUNG VON SCHIZOPHRENISCHEN PATIENTEN VORBEHALTEN WERDEN, DIE AUF ANGEMESSENE BEHANDLUNGEN KEINE AKZEPTABLE REAKTION ZEIGEN BEHANDLUNG MIT ANDEREN ANTIPSYCHOTIKEN, ENTWEDER AUFGRUND UNZUREICHENDER WIRKSAMKEIT ODER DER UNMÖGLICHKEIT, EINE WIRKSAME DOSIS ZU ERREICHEN, AUFGRUND UNTRAGBARER NEBENWIRKUNGEN DIESER ARZNEIMITTEL. DESHALB WIRD ES DRINGEND EMPFOHLEN, VOR BEGINN DER BEHANDLUNG MIT MELLARIL (Thioridazin-hcl) EINEM PATIENTEN MINDESTENS ZWEI VERSUCHE MIT EINEM UNTERSCHIEDLICHEN ANTIPSYCHOTIKARZNEIMITTEL IN EINER ANGEMESSENEN DOSIS UND FÜR EINE ANGEMESSENE DAUER ZU GEBEN. MELLARIL (Thioridazin hcl) WURDE NICHT SYSTEMATISCH IN KONTROLLIERTEN STUDIEN ZUR BEHANDLUNG VON PATIENTEN MIT REFRAKTÄRER SCHIZOPHRENIE UNTERSUCHT UND SEINE WIRKSAMKEIT BEI SOLCHEN PATIENTEN IST NICHT BEKANNT.
Eine Crossover-Studie an neun gesunden Männern, in der Einzeldosen von 10 mg und 50 mg Thioridazin mit Placebo verglichen wurden, zeigte eine dosisabhängige Verlängerung des QTc-Intervalls. Die mittlere maximale Verlängerung des QTc-Intervalls nach der 50-mg-Dosis betrug etwa 23 ms; Bei der klinischen Behandlung von nicht gescreenten Patienten kann eine längere Verlängerung beobachtet werden.
Eine Verlängerung des QTc-Intervalls wurde mit der Fähigkeit in Verbindung gebracht, Arrhythmien vom Torsade-de-Pointes-Typ, eine potenziell tödliche polymorphe ventrikuläre Tachykardie und plötzlichen Tod zu verursachen. Es gibt mehrere veröffentlichte Fallberichte über Torsade de Pointes und plötzlichen Tod im Zusammenhang mit der Behandlung mit Thioridazin. Ein kausaler Zusammenhang zwischen diesen Ereignissen und der Therapie mit Mellaril (Thioridazin-HCl) wurde nicht hergestellt, aber angesichts der Fähigkeit von Mellaril (Thioridazin-HCl), das QTc-Intervall zu verlängern, ist ein solcher Zusammenhang möglich.
Bestimmte Umstände können das Risiko für Torsade de Pointes und/oder plötzlichen Herztod in Verbindung mit der Anwendung von Arzneimitteln erhöhen, die das QTc-Intervall verlängern, einschließlich 1) Bradykardie, 2) Hypokaliämie, 3) gleichzeitige Anwendung anderer Arzneimittel, die das QTc-Intervall verlängern, 4) Vorhandensein einer angeborenen Verlängerung des QT-Intervalls und 5) für Thioridazin insbesondere seine Anwendung bei Patienten mit reduzierter Aktivität von P450 2D6 oder seine gleichzeitige Verabreichung mit Arzneimitteln, die P450 2D6 hemmen oder durch einen anderen Mechanismus die Clearance beeinträchtigen können von Thioridazin (vgl KONTRAINDIKATIONEN und VORSICHTSMASSNAHMEN ).
Es wird empfohlen, dass bei Patienten, die für eine Behandlung mit Mellaril (Thioridazin-HCl) in Betracht gezogen werden, ein Basis-EKG durchgeführt und die Serumkaliumspiegel gemessen werden. Das Serumkalium sollte vor Beginn der Behandlung normalisiert werden, und Patienten mit einem QTc-Intervall von mehr als 450 ms sollten keine Behandlung mit Mellaril (Thioridazin-HCl) erhalten. Es kann auch nützlich sein, EKGs und Serumkalium während der Behandlung mit Mellaril (Thioridazin-HCl) regelmäßig zu überwachen, insbesondere während einer Phase der Dosisanpassung. Mellaril (Thioridazin hcl) sollte bei Patienten abgesetzt werden, bei denen ein QTc-Intervall von über 500 ms festgestellt wird.
Patienten, die Mellaril (Thioridazin-HCl) einnehmen und bei denen Symptome auftreten, die mit dem Auftreten von Torsade de Pointes verbunden sein können (z. B. Schwindel, Herzklopfen oder Synkope), können eine weitere kardiale Untersuchung rechtfertigen; insbesondere sollte eine Holter-Überwachung in Erwägung gezogen werden.
Tardive Dyskinesie
Spätdyskinesie, ein Syndrom bestehend aus potenziell irreversiblen, unwillkürlichen, dyskinetischen Bewegungen, kann sich bei Patienten entwickeln, die mit Neuroleptika (Antipsychotika) behandelt werden. Obwohl die Prävalenz des Syndroms bei älteren Menschen, insbesondere bei älteren Frauen, am höchsten zu sein scheint, ist es unmöglich, sich auf Prävalenzschätzungen zu verlassen, um zu Beginn einer neuroleptischen Behandlung vorherzusagen, welche Patienten wahrscheinlich das Syndrom entwickeln werden. Ob sich neuroleptische Arzneimittel in ihrem Potenzial unterscheiden, tardive Dyskinesie zu verursachen, ist nicht bekannt.
Es wird angenommen, dass sowohl das Risiko, das Syndrom zu entwickeln, als auch die Wahrscheinlichkeit, dass es irreversibel wird, zunimmt, wenn die Dauer der Behandlung und die dem Patienten verabreichte kumulative Gesamtdosis von Neuroleptika zunehmen. Das Syndrom kann sich jedoch, wenn auch viel seltener, nach relativ kurzen Behandlungszeiten bei niedrigen Dosen entwickeln.
Es gibt keine bekannte Behandlung für etablierte Fälle von tardiver Dyskinesie, obwohl das Syndrom teilweise oder vollständig zurückgehen kann, wenn die neuroleptische Behandlung abgesetzt wird. Die neuroleptische Behandlung selbst kann jedoch die Anzeichen und Symptome des Syndroms unterdrücken (oder teilweise unterdrücken) und dadurch möglicherweise den zugrunde liegenden Krankheitsprozess maskieren. Die Auswirkung der symptomatischen Unterdrückung auf den Langzeitverlauf des Syndroms ist unbekannt.
Angesichts dieser Überlegungen sollten Neuroleptika so verschrieben werden, dass das Auftreten von tardiven Dyskinesien am wahrscheinlichsten minimiert wird. Eine chronische neuroleptische Behandlung sollte im Allgemeinen Patienten vorbehalten bleiben, die an einer chronischen Krankheit leiden, die 1) bekanntermaßen auf Neuroleptika anspricht und 2) für die alternative, ebenso wirksame, aber potenziell weniger schädliche Behandlungen nicht verfügbar oder angemessen sind. Bei Patienten, die eine chronische Behandlung benötigen, sollte die niedrigste Dosis und die kürzeste Behandlungsdauer angestrebt werden, die ein zufriedenstellendes klinisches Ansprechen bewirken. Die Notwendigkeit einer Fortsetzung der Behandlung sollte regelmäßig überprüft werden.
Wenn bei einem Patienten unter Neuroleptika Anzeichen und Symptome einer tardiven Dyskinesie auftreten, sollte ein Absetzen des Arzneimittels in Erwägung gezogen werden. Einige Patienten benötigen jedoch möglicherweise trotz des Vorhandenseins des Syndroms eine Behandlung.
(Weitere Informationen zur Beschreibung der tardiven Dyskinesie und ihrer klinischen Erkennung finden Sie in den Abschnitten Patienteninformationen und NEBENWIRKUNGEN. )
In Bezug auf Phenothiazine im Allgemeinen wurde vermutet, dass Menschen, die eine Überempfindlichkeitsreaktion (z. B. Blutdyskrasie, Gelbsucht) auf eines davon gezeigt haben, möglicherweise eher dazu neigen, eine Reaktion auf andere zu zeigen. Es sollte beachtet werden, dass Phenothiazine in der Lage sind, das zentrale Nervensystem dämpfende Mittel (z. B. Anästhetika, Opiate, Alkohol usw.) sowie Atropin- und Phosphorinsektizide zu potenzieren. Bei der Behandlung weniger schwerer Erkrankungen sollten Ärzte Nutzen und Risiko sorgfältig abwägen.
Bisherige Reproduktionsstudien an Tieren und klinische Erfahrungen haben keine teratogene Wirkung von Mellaril (Thioridazin-hcl) gezeigt. Da es jedoch wünschenswert ist, die Verabreichung aller Arzneimittel während der Schwangerschaft auf ein Minimum zu beschränken, sollte Mellaril (Thioridazin hcl) nur gegeben werden, wenn der Nutzen der Behandlung die möglichen Risiken für Mutter und Fötus überwiegt.
Malignes neuroleptisches Syndrom (NMS)
In Verbindung mit Antipsychotika wurde über einen potenziell tödlichen Symptomkomplex berichtet, der manchmal als malignes neuroleptisches Syndrom (NMS) bezeichnet wird. Klinische Manifestationen von NMS sind Hyperpyrexie, Muskelrigidität, veränderter Geisteszustand und Anzeichen einer autonomen Instabilität (unregelmäßiger Puls oder Blutdruck, Tachykardie, Diaphorese und Herzrhythmusstörungen).
Die diagnostische Beurteilung von Patienten mit diesem Syndrom ist kompliziert. Um zu einer Diagnose zu gelangen, ist es wichtig, Fälle zu identifizieren, bei denen das klinische Erscheinungsbild sowohl eine schwere medizinische Erkrankung (z. B. Lungenentzündung, systemische Infektion usw.) als auch unbehandelte oder unzureichend behandelte extrapyramidale Zeichen und Symptome (EPS) umfasst. Weitere wichtige Erwägungen bei der Differentialdiagnose sind zentrale anticholinerge Toxizität, Hitzschlag, Drogenfieber und primäre Pathologie des Zentralnervensystems (ZNS).
Das Management von NMS sollte Folgendes umfassen: 1) sofortiges Absetzen von Antipsychotika und anderen Arzneimitteln, die für eine gleichzeitige Therapie nicht unbedingt erforderlich sind, 2) intensive symptomatische Behandlung und medizinische Überwachung und 3) Behandlung aller begleitenden schwerwiegenden medizinischen Probleme, für die spezifische Behandlungen verfügbar sind. Es gibt keine allgemeine Übereinstimmung über spezifische pharmakologische Behandlungsschemata für unkompliziertes NMS.
Wenn ein Patient nach Genesung von NMS eine antipsychotische medikamentöse Behandlung benötigt, sollte die mögliche Wiederaufnahme der medikamentösen Therapie sorgfältig erwogen werden. Der Patient sollte sorgfältig überwacht werden, da Rezidive von NMS berichtet wurden.
Depressiva des zentralen Nervensystems
Wie im Fall anderer Phenothiazine ist Mellaril (Thioridazin hcl) in der Lage, das zentrale Nervensystem dämpfende Mittel (z. B. Alkohol, Anästhetika, Barbiturate, Narkotika, Opiate, andere psychoaktive Arzneimittel usw.) sowie Atropin- und Phosphorinsektizide zu potenzieren. Schwere Atemdepression und Atemstillstand wurden berichtet, wenn ein Patient Phenothiazin und gleichzeitig eine hohe Dosis eines Barbiturats erhielt.
VORSICHTSMASSNAHMEN
Leukopenie und/oder Agranulozytose und Krampfanfälle wurden berichtet, sind aber selten. Mellaril® (Thioridazin-HCl) hat sich bei der Behandlung von Verhaltensstörungen bei Epilepsiepatienten als hilfreich erwiesen, aber auch eine antikonvulsive Medikation sollte beibehalten werden. Die pigmentäre Retinopathie, die hauptsächlich bei Patienten beobachtet wurde, die höhere Dosen als empfohlen einnahmen, ist gekennzeichnet durch eine Verringerung der Sehschärfe, eine bräunliche Färbung des Sehvermögens und eine Beeinträchtigung des Nachtsehens; Die Untersuchung des Fundus zeigt Pigmentablagerungen. Die Möglichkeit dieser Komplikation kann verringert werden, indem die empfohlenen Dosierungsgrenzen eingehalten werden.
Bei Aktivitäten, die eine vollständige geistige Wachheit erfordern (z. B. Autofahren), ist es ratsam, die Phenothiazine vorsichtig zu verabreichen und die Dosierung schrittweise zu steigern. Weibliche Patienten scheinen eine größere Neigung zu orthostatischer Hypotonie zu haben als männliche Patienten. Die Verabreichung von Epinephrin sollte bei der Behandlung von arzneimittelinduzierter Hypotonie vermieden werden, da Phenothiazine gelegentlich eine umgekehrte Epinephrinwirkung hervorrufen können. Sollte ein Vasokonstriktor erforderlich sein, sind Levarterenol und Phenylephrin am besten geeignet.
Neuroleptika erhöhen den Prolaktinspiegel; die Erhöhung bleibt während der chronischen Verabreichung bestehen. Gewebekulturexperimente weisen darauf hin, dass ungefähr ein Drittel der menschlichen Brustkrebserkrankungen in vitro Prolaktin-abhängig sind, ein Faktor von potenzieller Bedeutung, wenn die Verschreibung dieser Arzneimittel bei einer Patientin mit einem zuvor festgestellten Brustkrebs in Betracht gezogen wird. Obwohl über Störungen wie Galaktorrhoe, Amenorrhoe, Gynäkomastie und Impotenz berichtet wurde, ist die klinische Bedeutung erhöhter Prolaktinspiegel im Serum bei den meisten Patienten unbekannt. Bei Nagetieren wurde nach chronischer Verabreichung von Neuroleptika eine Zunahme von Mamma-Neoplasmen festgestellt. Weder klinische Studien noch bisher durchgeführte epidemiologische Studien haben jedoch einen Zusammenhang zwischen der chronischen Verabreichung dieser Medikamente und der Mamma-Tumorentstehung gezeigt; Die verfügbaren Beweise gelten als zu begrenzt, um zum jetzigen Zeitpunkt schlüssig zu sein.
Pädiatrische Verwendung
Sehen DOSIERUNG Sektion Pädiatrische Patienten .
ÜBERDOSIS
Viele der beobachteten Symptome sind Erweiterungen der unten beschriebenen Nebenwirkungen NEBENWIRKUNGEN. Mellaril® (Thioridazin-HCl) (Thioridazin-HCl) kann bei Überdosierung toxisch sein, wobei die kardiale Toxizität besonders besorgniserregend ist. Eine häufige EKG- und Vitalzeichenüberwachung von überdosierten Patienten wird empfohlen. Aufgrund des Risikos verzögerter Wirkungen kann eine mehrtägige Beobachtung erforderlich sein.
Anzeichen und Symptome
Auswirkungen und klinische Komplikationen einer akuten Überdosierung von Phenothiazinen können sein:
Herz-Kreislauf: Herzrhythmusstörungen, Hypotonie, Schock, EKG-Veränderungen, verlängerte QT- und PR-Intervalle, unspezifische ST- und T-Wellen-Veränderungen, Bradykardie, Sinustachykardie, atrioventrikulärer Block, ventrikuläre Tachykardie, Kammerflimmern, Torsade de Pointes, Myokarddepression.
Zentrales Nervensystem: Sedierung, extrapyramidale Wirkungen, Verwirrtheit, Erregung, Hypothermie, Hyperthermie, Ruhelosigkeit, Krampfanfälle, Areflexie, Koma.
Vegetatives Nervensystem: Mydriasis, Miosis, trockene Haut, trockener Mund, verstopfte Nase, Harnverhalt, verschwommenes Sehen.
Atmung: Atemdepression, Apnoe, Lungenödem.
Magen-Darm: Hypomotilität, Obstipation, Ileus.
Nieren: Oligurie, Urämie.
Toxische Dosis- und Blutkonzentrationsbereiche für die Phenothiazine wurden nicht fest etabliert. Es wurde vermutet, dass der toxische Blutkonzentrationsbereich für Thioridazin bei 1,0 mg/dL beginnt und 2-8 mg/dL der tödliche Konzentrationsbereich ist.
Behandlung
Ein Atemweg muss hergestellt und aufrechterhalten werden. Für ausreichende Sauerstoffversorgung und Belüftung ist zu sorgen.
Die kardiovaskuläre Überwachung sollte sofort beginnen und eine kontinuierliche elektrokardiographische Überwachung umfassen, um mögliche Arrhythmien zu erkennen. Die Behandlung kann eine oder mehrere der folgenden therapeutischen Interventionen umfassen: Korrektur von Elektrolytanomalien und Säure-Basen-Gleichgewicht, Lidocain, Phenytoin, Isoproterenol, ventrikuläre Stimulation und Defibrillation. Disopyramid, Procainamid und Chinidin können zusätzliche QT-verlängernde Wirkungen haben, wenn sie Patienten mit einer akuten Überdosierung von Mellaril verabreicht werden, und sollten vermieden werden (siehe WARNUNGEN und KONTRAINDIKATIONEN ). Bei der Verabreichung von Lidocain ist Vorsicht geboten, da es das Risiko für Krampfanfälle erhöhen kann.
Die Behandlung von Hypotonie kann intravenöse Flüssigkeiten und Vasopressoren erfordern. Phenylephrin, Levarterenol oder Metaraminol sind geeignete blutdruckerhöhende Mittel zur Behandlung von refraktärer Hypotonie. Die starken α-adrenergen Blockierungseigenschaften der Phenothiazine machen die Verwendung von Vasopressoren mit gemischten α- und β-adrenergen Agonisteneigenschaften unangemessen, einschließlich Epinephrin und Dopamin. Es kann zu einer paradoxen Vasodilatation kommen. Darüber hinaus ist zu erwarten, dass die α-adrenergen blockierenden Eigenschaften von Bretylium zu denen von Mellaril (Thioridazin-HCl) addiert werden könnten, was zu einer problematischen Hypotonie führt.
Bei der Behandlung einer Überdosierung sollte der Arzt immer die Möglichkeit einer Beteiligung mehrerer Arzneimittel in Betracht ziehen. Eine Magenspülung und wiederholte Gaben von Aktivkohle sollten in Erwägung gezogen werden. Die Induktion von Erbrechen ist einer Magenspülung wegen des Risikos einer Dystonie und der Möglichkeit einer Aspiration von Erbrochenem weniger vorzuziehen. Bei Patienten, bei denen eine rasche Verschlechterung zu erwarten ist, oder bei Patienten mit Bewusstseinsstörungen sollte kein Erbrechen ausgelöst werden.
Akute extrapyramidale Symptome können mit Diphenhydraminhydrochlorid oder Benztropinmesylat behandelt werden.
Vermeiden Sie die Verwendung von Barbituraten bei der Behandlung von Krampfanfällen, da sie die Phenothiazin-induzierte Atemdepression verstärken können.
Forcierte Diurese, Hämoperfusion, Hämodialyse und Manipulation des Urin-pH-Werts sind aufgrund ihres großen Verteilungsvolumens und ihrer starken Plasmaproteinbindung von unwahrscheinlichem Nutzen bei der Behandlung einer Phenothiazin-Überdosierung.
Aktuelle Informationen zur Behandlung einer Überdosierung sind häufig bei einem zertifizierten regionalen Giftinformationszentrum erhältlich. Die Telefonnummern zertifizierter regionaler Giftinformationszentren sind in der Physicians' Desk Reference®** aufgeführt.
KONTRAINDIKATIONEN
Die Anwendung von Mellaril® (Thioridazin-HCl) sollte in Kombination mit anderen Arzneimitteln, die bekanntermaßen das QTc-Intervall verlängern, und bei Patienten mit angeborenem Long-QT-Syndrom oder Herzrhythmusstörungen in der Vorgeschichte vermieden werden.
Arzneimittel mit verringerter Cytochrom-P450-2D6-Isozymaktivität, die dieses Isozym hemmen (z. B. Fluoxetin und Paroxetin) und bestimmte andere Arzneimittel (z. B. Fluvoxamin, Propranolol und Pindolol) scheinen den Metabolismus von Thioridazin merklich zu hemmen. Es ist zu erwarten, dass die daraus resultierenden erhöhten Thioridazinspiegel die mit Mellaril (Thioridazin hcl) verbundene Verlängerung des QTc-Intervalls verstärken und das Risiko schwerer, möglicherweise tödlicher Herzrhythmusstörungen, wie Arrhythmien vom Torsade-de-Pointes-Typ, erhöhen können. Ein solches erhöhtes Risiko kann sich auch aus der additiven Wirkung der gleichzeitigen Verabreichung von Mellaril (Thioridazin-HCl) mit anderen Wirkstoffen ergeben, die das QTc-Intervall verlängern. Daher ist Mellaril (Thioridazin hcl) mit diesen Arzneimitteln kontraindiziert sowie bei Patienten, die etwa 7 % der Normalbevölkerung ausmachen und von denen bekannt ist, dass sie einen genetischen Defekt haben, der zu einer verminderten Aktivität von P450 2D6 führt (siehe WARNUNGEN und VORSICHTSMASSNAHMEN ).
Wie andere Phenothiazine ist Mellaril (Thioridazin hcl) kontraindiziert bei schwerer Depression des Zentralnervensystems oder komatösen Zuständen jeglicher Ursache, einschließlich arzneimittelinduzierter Depression des Zentralnervensystems (siehe WARNUNGEN ). Es sollte auch beachtet werden, dass hypertensive oder hypotensive Herzerkrankungen extremen Ausmaßes eine Kontraindikation für die Verabreichung von Phenothiazin sind.
KLINISCHE PHARMAKOLOGIE
Die pharmakologische Grundaktivität von Mellaril® (Thioridazin-HCl) ähnelt der anderer Phenothiazine, ist jedoch mit einer minimalen extrapyramidalen Stimulation verbunden.
Es wurde jedoch gezeigt, dass Thioridazin das QTc-Intervall dosisabhängig verlängert. Dieser Effekt kann das Risiko schwerer, potenziell tödlicher ventrikulärer Arrhythmien, wie z. B. Arrhythmien vom Torsade-de-Pointes-Typ, erhöhen. Aufgrund dieses Risikos ist Mellaril (Thioridazin hcl) nur für schizophrene Patienten indiziert, die auf andere Antipsychotika nicht angesprochen haben oder diese nicht vertragen (siehe WARNUNGEN und KONTRAINDIKATIONEN ). Der verschreibende Arzt sollte sich jedoch darüber im Klaren sein, dass Mellaril (Thioridazin hcl) nicht systematisch in kontrollierten Studien bei therapierefraktären schizophrenen Patienten untersucht wurde und seine Wirksamkeit bei solchen Patienten unbekannt ist.
INFORMATIONEN ZUM PATIENTEN
Die Patienten sollten darüber informiert werden, dass Mellaril (Thioridazin-HCl) mit potenziell tödlichen Herzrhythmusstörungen in Verbindung gebracht wurde. Das Risiko solcher Ereignisse kann erhöht sein, wenn bestimmte Arzneimittel zusammen mit Mellaril (Thioridazin-HCl) verabreicht werden. Daher sollten Patienten den verschreibenden Arzt darüber informieren, dass sie eine Behandlung mit Mellaril (Thioridazin-HCl) erhalten, bevor sie neue Medikamente einnehmen.
Angesichts der Wahrscheinlichkeit, dass einige Patienten, die chronisch Neuroleptika ausgesetzt sind, tardive Dyskinesie entwickeln werden, wird empfohlen, dass alle Patienten, bei denen eine chronische Anwendung in Betracht gezogen wird, möglichst umfassend über dieses Risiko informiert werden. Die Entscheidung, Patienten und/oder ihre Erziehungsberechtigten zu informieren, muss natürlich die klinischen Umstände und die Kompetenz des Patienten, die bereitgestellten Informationen zu verstehen, berücksichtigen.