Ponstel 250mg, 500mg Mefenamic Acid Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
PONSTEL® (Mefenaminsäure) Kapseln, USP 250 mg
Herz-Kreislauf-Risiko
Magen-Darm-Risiko
BEZEICHNUNG
Ponstel® (Mefenaminsäure) gehört zur Gruppe der nichtsteroidalen Antiphlogistika (NSAIDs) der Fenamate. Jede elfenbeinfarbene Kapsel mit blauem Band enthält 250 mg Mefenaminsäure zur oralen Verabreichung. Mefenaminsäure ist ein weißes bis grauweißes, geruchloses, mikrokristallines Pulver mit einem Schmelzpunkt von 230°-231°C und einer Wasserlöslichkeit von 0,004 % bei pH 7,1. Der chemische Name lautet N-2,3-Xylylanthranilsäure. Das Molekulargewicht beträgt 241,29. Seine Summenformel ist C15H15NO2 und die Strukturformel von Mefenaminsäure ist:
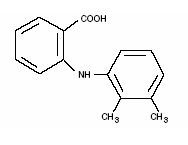
Jede Kapsel enthält auch Lactose, NF. Die Kapselhülle und/oder das Band enthält Citronensäure, USP; D&C gelb Nr. 10; FD&C blau Nr. 1; FD&C rot Nr. 3; FD&C gelb Nr. 6; Gelatine, NF; Glycerolmonooleat; Siliziumdioxid, NF; Natriumbenzoat, NF; Natriumlaurylsulfat, NF; Titandioxid, USP.
INDIKATIONEN
Wägen Sie die potenziellen Vorteile und Risiken von PONSTEL (Mefenaminsäure) und anderen Behandlungsoptionen sorgfältig ab, bevor Sie sich für die Anwendung von PONSTEL (Mefenaminsäure) entscheiden. Verwenden Sie die niedrigste wirksame Dosis für die kürzeste Dauer im Einklang mit den individuellen Behandlungszielen des Patienten (siehe WARNUNGEN ).
PONSTEL (Mefenaminsäure) ist angezeigt:
DOSIERUNG UND ANWENDUNG
Wägen Sie die potenziellen Vorteile und Risiken von PONSTEL (Mefenaminsäure) und anderen Behandlungsoptionen sorgfältig ab, bevor Sie sich für die Anwendung von PONSTEL (Mefenaminsäure) entscheiden. Verwenden Sie die niedrigste wirksame Dosis für die kürzeste Dauer im Einklang mit den individuellen Behandlungszielen des Patienten (siehe WARNUNGEN ).
Nachdem das Ansprechen auf die Initialtherapie mit PONSTEL (Mefenaminsäure) beobachtet wurde, sollten Dosis und Häufigkeit an die individuellen Bedürfnisse des Patienten angepasst werden.
Zur Linderung akuter Schmerzen bei Erwachsenen und Jugendlichen im Alter von 14 Jahren beträgt die empfohlene Dosis 500 mg als Anfangsdosis, gefolgt von 250 mg alle 6 Stunden nach Bedarf, normalerweise nicht länger als eine Woche.4
Für die Behandlung der primären Dysmenorrhoe beträgt die empfohlene Dosis 500 mg als Anfangsdosis, gefolgt von 250 mg alle 6 Stunden, oral gegeben, beginnend mit dem Einsetzen der Blutung und der damit verbundenen Symptome. Klinische Studien weisen darauf hin, dass eine wirksame Behandlung mit Beginn der Menstruation begonnen werden kann und nicht länger als 2 bis 3 Tage erforderlich sein sollte.5
WIE GELIEFERT
Ponstel (Mefenaminsäure) ist als 250 mg blau gebänderte, elfenbeinfarbene Kapseln mit dem Aufdruck „FHPC 400“ und „PONSTEL® (Mefenaminsäure)“ erhältlich.
NEBENWIRKUNGEN
Bei Patienten, die Ponstel (Mefenaminsäure) oder andere NSAIDs einnehmen, sind die am häufigsten berichteten Nebenwirkungen, die bei etwa 1-10 % der Patienten auftraten:
Gastrointestinale Erfahrungen einschließlich - Bauchschmerzen, Verstopfung, Durchfall, Dyspepsie, Blähungen, starke Blutungen/Perforationen, Sodbrennen, Übelkeit, Magen-Darm-Geschwüre (Magen/Zwölffingerdarm), Erbrechen, abnorme Nierenfunktion, Anämie, Schwindel, Ödeme, erhöhte Leberenzyme, Kopfschmerzen, erhöhte Blutungszeit, Pruritus, Hautausschläge, Tinnitus
Zusätzliche Nebenwirkungen, die gelegentlich berichtet und hier nach Körpersystemen aufgelistet werden, umfassen:
Körper als Ganzes - Fieber, Infektion, Sepsis
Herz-Kreislauf-System - Herzinsuffizienz, Bluthochdruck, Tachykardie, Synkope
Verdauungstrakt - Mundtrockenheit, Ösophagitis, Magen-/Magengeschwüre, Gastritis, Magen-Darm-Blutungen, Glossitis, Hämatemesis, Hepatitis, Gelbsucht
Hämisches und lymphatisches System - Ekchymose, Eosinophilie, Leukopenie, Meläna, Purpura, rektale Blutung, Stomatitis, Thrombozytopenie
Stoffwechsel und Ernährung - Gewichtsveränderungen
Nervöses System Angst, Asthenie, Verwirrtheit, Depression, Traumanomalien, Benommenheit; Schlaflosigkeit, Unwohlsein, Nervosität, Parästhesien, Somnolenz, Zittern, Schwindel
Atmungssystem - Asthma, Atemnot
Haut und Anhängsel - Alopezie, Lichtempfindlichkeit, Juckreiz, Schweiß
Besondere Sinne - verschwommene Sicht
Urogenitalsystem - Zystitis, Dysurie, Hämaturie, interstitielle Nephritis, Oligurie/Polyurie, Proteinurie, Nierenversagen
Andere Nebenwirkungen, die selten auftreten, sind:
Körper als Ganzes - Anaphylaktoide Reaktionen, Appetitveränderungen, Tod
Herz-Kreislauf-System - Arrhythmie, Hypotonie, Myokardinfarkt, Herzklopfen, Vaskulitis
Verdauungstrakt - Aufstoßen, Leberversagen, Pankreatitis
Hämisches und lymphatisches System - Agranulozytose, hämolytische Anämie, aplastische Anämie, Lymphadenopathie, Panzytopenie
Stoffwechsel und Ernährung - Hyperglykämie
Nervöses System - Krämpfe, Koma, Halluzinationen, Meningitis.
Atmung Atemdepression, Lungenentzündung
Haut und Anhängsel - Angioödem, toxische epidermale Nekrose, Erythema multiforme, exfoliative Dermatitis, Stevens-Johnson-Syndrom, Urtikaria
Besondere Sinne - Bindehautentzündung, Schwerhörigkeit
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Eine Reihe von Verbindungen sind Inhibitoren von CYP2C9. Wechselwirkungsstudien mit Mefenaminsäure und diesen Verbindungen wurden nicht durchgeführt. Bei gleichzeitiger Anwendung von Ponstel (Mefenaminsäure) mit diesen Arzneimitteln sollte die Möglichkeit einer veränderten Sicherheit und Wirksamkeit in Betracht gezogen werden.
ACE-Hemmer
Berichte deuten darauf hin, dass NSAIDs die blutdrucksenkende Wirkung von ACE-Hemmern verringern können. Diese Wechselwirkung sollte bei Patienten berücksichtigt werden, die NSAIDs gleichzeitig mit ACE-Hemmern einnehmen.
Aspirin
Wenn PONSTEL (Mefenaminsäure) zusammen mit Aspirin verabreicht wird, wird seine Proteinbindung reduziert, obwohl die Clearance von freiem PONSTEL (Mefenaminsäure) nicht verändert wird. Die klinische Bedeutung dieser Wechselwirkung ist nicht bekannt; jedoch wird, wie bei anderen NSAIDs, die gleichzeitige Verabreichung von Mefenamic Acid und Aspirin aufgrund des Potenzials verstärkter Nebenwirkungen im Allgemeinen nicht empfohlen.
Diuretika
Klinische Studien sowie Beobachtungen nach der Markteinführung haben gezeigt, dass PONSTEL (Mefenaminsäure) bei einigen Patienten die natriuretische Wirkung von Furosemid und Thiaziden verringern kann. Diese Reaktion wurde der Hemmung der renalen Prostaglandinsynthese zugeschrieben. Während einer gleichzeitigen Therapie mit NSAIDs sollte der Patient engmaschig auf Anzeichen einer Niereninsuffizienz überwacht werden (s VORSICHTSMASSNAHMEN, Auswirkungen auf die Nieren ) sowie zur Sicherstellung der diuretischen Wirksamkeit.
Lithium
NSAIDs haben zu einer Erhöhung der Plasma-Lithiumspiegel und einer Verringerung der renalen Lithium-Clearance geführt. Die mittlere minimale Lithiumkonzentration stieg um 15 % und die renale Clearance verringerte sich um etwa 20 %. Diese Wirkungen wurden der Hemmung der renalen Prostaglandinsynthese durch das NSAID zugeschrieben. Wenn NSAIDs und Lithium gleichzeitig verabreicht werden, sollten die Probanden daher sorgfältig auf Anzeichen einer Lithiumtoxizität beobachtet werden.
Methotrexat
Es wurde berichtet, dass NSAIDs die Akkumulation von Methotrexat in Nierenschnitten von Kaninchen kompetitiv hemmen. Dies kann darauf hindeuten, dass sie die Toxizität von Methotrexat verstärken könnten. Vorsicht ist geboten, wenn NSAIDs gleichzeitig mit Methotrexat verabreicht werden.
Warfarin
Die Wirkungen von Warfarin und NSAIDs auf gastrointestinale Blutungen sind synergistisch, so dass Benutzer beider Medikamente zusammen ein höheres Risiko für schwere gastrointestinale Blutungen haben als Benutzer eines der beiden Medikamente allein.
Antazida
In einer Einzeldosisstudie (n=6) erhöhte die Einnahme eines Antazidums, das 1,7 Gramm Magnesiumhydroxid mit 500 mg Mefenaminsäure enthielt, die Cmax und AUC von Mefenaminsäure um 125 % bzw. 36 %.1
Arzneimittel-/Labortest-Wechselwirkungen
Ponstel (Mefenaminsäure) kann die Prothrombinzeit verlängern.4 Daher ist bei Verabreichung des Arzneimittels an Patienten, die orale Antikoagulanzien erhalten, eine häufige Überwachung der Prothrombinzeit erforderlich.
Nach Verabreichung von Mefenaminsäure kann es im Diazo-Tablettentest zu einer falsch-positiven Reaktion auf Gallenflüssigkeit im Urin kommen. Bei Verdacht auf Biliurie sollten andere diagnostische Verfahren wie der Harrison-Spot-Test durchgeführt werden.
VERWEISE
4. Glazko AJ: Experimentelle Beobachtungen von Flufenaminsäure, Mefenaminsäure und Meclofenaminsäure. Teil III. Stoffwechseldisposition, in Fenamate in der Medizin. A Symposium, London, 1966. Annals of Physical Medicine, Supplement, S. 23-36, 1967.
WARNUNGEN
Kardiovaskuläre Wirkungen
Kardiovaskuläre thrombotische Ereignisse
Klinische Studien mit mehreren COX-2-selektiven und nicht-selektiven NSAIDs mit einer Dauer von bis zu drei Jahren haben ein erhöhtes Risiko für schwerwiegende kardiovaskuläre (CV) thrombotische Ereignisse, Myokardinfarkt und Schlaganfall gezeigt, die tödlich sein können. Alle NSAIDs, sowohl COX-2-selektive als auch nicht-selektive, können ein ähnliches Risiko aufweisen. Patienten mit bekannter kardiovaskulärer Erkrankung oder Risikofaktoren für eine kardiovaskuläre Erkrankung können einem höheren Risiko ausgesetzt sein. Um das potenzielle Risiko eines unerwünschten kardiovaskulären Ereignisses bei Patienten, die mit einem NSAID behandelt werden, zu minimieren, sollte die niedrigste wirksame Dosis für die kürzestmögliche Dauer angewendet werden. Ärzte und Patienten sollten auf die Entwicklung solcher Ereignisse achten, auch wenn zuvor keine kardiovaskulären Symptome aufgetreten sind. Die Patienten sollten über die Anzeichen und/oder Symptome schwerwiegender kardiovaskulärer Ereignisse und die zu ergreifenden Maßnahmen bei deren Auftreten informiert werden.
Es gibt keine konsistenten Beweise dafür, dass die gleichzeitige Anwendung von Aspirin das erhöhte Risiko schwerer kardiovaskulärer thrombotischer Ereignisse im Zusammenhang mit der Anwendung von NSAR mindert. Die gleichzeitige Anwendung von Aspirin und einem NSAID erhöht das Risiko schwerwiegender gastrointestinaler Ereignisse (vgl GI-WARNUNGEN ).
Zwei große, kontrollierte klinische Studien mit einem COX-2-selektiven NSAID zur Behandlung von Schmerzen in den ersten 10–14 Tagen nach einer CABG-Operation ergaben eine erhöhte Inzidenz von Myokardinfarkt und Schlaganfall (vgl KONTRAINDIKATIONEN ).
Hypertonie
NSAIDs, einschließlich PONSTEL (Mefenaminsäure), können zum Auftreten von neuem Bluthochdruck oder zur Verschlechterung eines vorbestehenden Bluthochdrucks führen, die beide zu einer erhöhten Inzidenz von kardiovaskulären Ereignissen beitragen können. Patienten, die Thiazide oder Schleifendiuretika einnehmen, können bei der Einnahme von NSAR auf diese Therapien beeinträchtigt sein. NSAR, einschließlich PONSTEL (Mefenaminsäure), sollten bei Patienten mit Bluthochdruck mit Vorsicht angewendet werden. Der Blutdruck (BP) sollte zu Beginn der NSAID-Behandlung und während des gesamten Therapieverlaufs engmaschig überwacht werden.
Herzinsuffizienz und Ödeme
Bei einigen Patienten, die NSAIDs einnahmen, wurden Flüssigkeitsretention und Ödeme beobachtet. PONSTEL (Mefenaminsäure) sollte bei Patienten mit Flüssigkeitsretention oder Herzinsuffizienz mit Vorsicht angewendet werden.
Auswirkungen auf den Gastrointestinaltrakt – Risiko von Ulzerationen, Blutungen und Perforationen
NSAIDs, einschließlich PONSTEL (Mefenaminsäure), können schwerwiegende Nebenwirkungen im Magen-Darm-Trakt (GI) verursachen, darunter Entzündungen, Blutungen, Geschwüre und Perforationen des Magens, Dünndarms oder Dickdarms, die tödlich sein können. Diese schwerwiegenden unerwünschten Ereignisse können jederzeit mit oder ohne Warnsymptome bei Patienten auftreten, die mit NSAIDs behandelt werden. Nur jeder fünfte Patient, der unter NSAID-Therapie ein schwerwiegendes unerwünschtes Ereignis im oberen Gastrointestinaltrakt entwickelt, ist symptomatisch. Geschwüre im oberen Gastrointestinaltrakt, starke Blutungen oder Perforationen, die durch NSAIDs verursacht werden, treten bei etwa 1 % der Patienten auf, die 3–6 Monate lang behandelt wurden, und bei etwa 2–4 % der Patienten, die ein Jahr lang behandelt wurden. Diese Trends setzen sich bei längerer Anwendungsdauer fort und erhöhen die Wahrscheinlichkeit, irgendwann im Verlauf der Therapie ein schwerwiegendes gastrointestinales Ereignis zu entwickeln. Allerdings ist auch eine Kurzzeittherapie nicht ohne Risiko.
NSAIDs sollten bei Patienten mit Ulkuserkrankungen oder gastrointestinalen Blutungen in der Vorgeschichte mit äußerster Vorsicht verschrieben werden. Patienten mit Magengeschwüren und/oder gastrointestinalen Blutungen in der Vorgeschichte, die NSAIDs anwenden, haben ein mehr als 10-fach erhöhtes Risiko für die Entwicklung einer gastrointestinalen Blutung im Vergleich zu Patienten mit keinem dieser Risikofaktoren. Andere Faktoren, die das Risiko für gastrointestinale Blutungen bei mit NSAR behandelten Patienten erhöhen, sind die gleichzeitige Anwendung von oralen Kortikosteroiden oder Antikoagulanzien, eine längere Dauer der NSAID-Therapie, Rauchen, Alkoholkonsum, höheres Alter und ein schlechter allgemeiner Gesundheitszustand. Die meisten Spontanberichte über tödliche gastrointestinale Ereignisse stammen von älteren oder geschwächten Patienten, weshalb bei der Behandlung dieser Patientengruppe besondere Vorsicht geboten ist.
Um das potenzielle Risiko eines unerwünschten gastrointestinalen Ereignisses bei Patienten, die mit einem NSAID behandelt werden, zu minimieren, sollte die niedrigste wirksame Dosis für die kürzestmögliche Dauer angewendet werden. Patienten und Ärzte sollten während der NSAID-Therapie auf Anzeichen und Symptome von gastrointestinalen Ulzerationen und Blutungen achten und unverzüglich eine zusätzliche Untersuchung und Behandlung einleiten, wenn der Verdacht auf ein schwerwiegendes gastrointestinales unerwünschtes Ereignis besteht. Dies sollte das Absetzen des NSAID einschließen, bis ein schwerwiegendes gastrointestinales unerwünschtes Ereignis ausgeschlossen ist. Bei Hochrisikopatienten sollten alternative Therapien ohne NSAIDs in Betracht gezogen werden.
Auswirkungen auf die Nieren
Die langfristige Verabreichung von NSAIDs hat zu Nierenpapillennekrose und anderen Nierenschäden geführt. Nierentoxizität wurde auch bei Patienten beobachtet, bei denen renale Prostaglandine eine kompensatorische Rolle bei der Aufrechterhaltung der Nierendurchblutung spielen. Bei diesen Patienten kann die Verabreichung eines nichtsteroidalen Antirheumatikums eine dosisabhängige Verringerung der Prostaglandinbildung und sekundär des renalen Blutflusses verursachen, was eine offenkundige Nierendekompensation auslösen kann. Patienten mit dem größten Risiko für diese Reaktion sind Patienten mit eingeschränkter Nierenfunktion, Herzinsuffizienz, Leberfunktionsstörungen, Patienten, die Diuretika und ACE-Hemmer einnehmen, sowie ältere Menschen. Auf das Absetzen der NSAID-Therapie folgt normalerweise die Wiederherstellung des Zustands vor der Behandlung.
Fortgeschrittene Nierenerkrankung
Es liegen keine Informationen zu kontrollierten Studien zur Anwendung von PONSTEL (Mefenaminsäure) bei Patienten mit fortgeschrittener Nierenerkrankung vor. Daher wird die Behandlung mit PONSTEL (Mefenaminsäure) bei diesen Patienten mit fortgeschrittener Nierenerkrankung nicht empfohlen (siehe KONTRAINDIKATIONEN ).
Anaphylaktoide Reaktionen
Wie bei anderen NSAIDs können bei Patienten ohne bekannte vorherige Exposition gegenüber PONSTEL (Mefenaminsäure) anaphylaktoide Reaktionen auftreten. PONSTEL (Mefenaminsäure) sollte Patienten mit der Aspirin-Triade nicht verabreicht werden. Dieser Symptomkomplex tritt typischerweise bei Asthmatikern auf, die eine Rhinitis mit oder ohne Nasenpolypen erleiden oder die nach der Einnahme von Aspirin oder anderen NSAIDs einen schweren, möglicherweise tödlichen Bronchospasmus zeigen (siehe KONTRAINDIKATIONEN und VORSICHTSMASSNAHMEN - Vorbestehendes Asthma ). In Fällen, in denen eine anaphylaktoide Reaktion auftritt, sollte Notfallhilfe in Anspruch genommen werden.
Hautreaktionen
NSAIDs, einschließlich PONSTEL (Mefenaminsäure), können schwerwiegende Nebenwirkungen der Haut wie exfoliative Dermatitis, Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN) verursachen, die tödlich sein können. Diese schwerwiegenden Ereignisse können ohne Vorwarnung eintreten. Die Patienten sollten über die Anzeichen und Symptome schwerwiegender Hautmanifestationen informiert werden und die Anwendung des Arzneimittels sollte beim ersten Auftreten von Hautausschlag oder anderen Anzeichen einer Überempfindlichkeit abgebrochen werden.
Schwangerschaft
In der späten Schwangerschaft sollte PONSTEL (Mefenaminsäure) wie andere NSAIDs vermieden werden, da es einen vorzeitigen Verschluss des Ductus arteriosus verursachen kann.
VORSICHTSMASSNAHMEN
Allgemein
Von PONSTEL (Mefenaminsäure) kann nicht erwartet werden, dass es Kortikosteroide ersetzt oder eine Kortikosteroidinsuffizienz behandelt. Ein abruptes Absetzen von Kortikosteroiden kann zu einer Exazerbation der Erkrankung führen. Bei Patienten unter längerer Kortikosteroidtherapie sollte die Therapie langsam ausgeschlichen werden, wenn die Entscheidung getroffen wird, Kortikosteroide abzusetzen.
Die pharmakologische Aktivität von PONSTEL (Mefenaminsäure) bei der Senkung von Fieber und Entzündungen kann die Nützlichkeit dieser diagnostischen Zeichen bei der Erkennung von Komplikationen bei vermutlich nicht infektiösen, schmerzhaften Zuständen verringern.
Hepatische Wirkungen
Bei bis zu 15 % der Patienten, die NSAIDs, einschließlich PONSTEL (Mefenaminsäure), einnehmen, können grenzwertige Erhöhungen eines oder mehrerer Leberwerte auftreten. Diese Laboranomalien können fortschreiten, unverändert bleiben oder bei fortgesetzter Therapie vorübergehend sein. Bemerkenswerte Erhöhungen von ALT oder AST (etwa das Drei- oder Mehrfache der Obergrenze des Normalwerts) wurden bei etwa 1 % der Patienten in klinischen Studien mit NSAIDs berichtet. Darüber hinaus wurden seltene Fälle von schweren Leberreaktionen, einschließlich Gelbsucht und tödlich verlaufender fulminanter Hepatitis, Lebernekrose und Leberversagen, einige davon mit tödlichem Ausgang, berichtet.
Ein Patient mit Symptomen und/oder Anzeichen, die auf eine Leberfunktionsstörung hindeuten, oder bei dem ein abnormaler Lebertest aufgetreten ist, sollte während der Therapie mit PONSTEL (Mefenaminsäure) auf Hinweise auf die Entwicklung einer schwereren Leberreaktion untersucht werden. Wenn sich klinische Anzeichen und Symptome entwickeln, die einer Lebererkrankung entsprechen, oder wenn systemische Manifestationen auftreten (z. B. Eosinophilie, Hautausschlag usw.), sollte PONSTEL (Mefenaminsäure) abgesetzt werden.
Hämatologische Wirkungen
Anämie wird manchmal bei Patienten beobachtet, die NSAIDs, einschließlich PONSTEL (Mefenaminsäure) erhalten. Dies kann auf Flüssigkeitsretention, gastrointestinalen Blutverlust oder eine unvollständig beschriebene Wirkung auf die Erythropoese zurückzuführen sein. Patienten unter Langzeitbehandlung mit NSAIDs, einschließlich PONSTEL (Mefenaminsäure), sollten ihren Hämoglobin- oder Hämatokritwert überprüfen lassen, wenn sie Anzeichen oder Symptome einer Anämie aufweisen. NSAIDs hemmen die Blutplättchenaggregation und verlängern nachweislich die Blutungszeit bei einigen Patienten. Im Gegensatz zu Aspirin ist ihre Wirkung auf die Thrombozytenfunktion quantitativ geringer, von kürzerer Dauer und reversibel. Patienten, die PONSTEL (Mefenaminsäure) erhalten und die durch Veränderungen der Thrombozytenfunktion beeinträchtigt werden können, wie z. B. Patienten mit Gerinnungsstörungen oder Patienten, die Antikoagulanzien erhalten, sollten sorgfältig überwacht werden.
Vorbestehendes Asthma
Patienten mit Asthma können Aspirin-empfindliches Asthma haben. Die Anwendung von Aspirin bei Patienten mit Aspirin-empfindlichem Asthma wurde mit schwerem Bronchospasmus in Verbindung gebracht, der tödlich sein kann. Da bei solchen Aspirin-empfindlichen Patienten über Kreuzreaktivität, einschließlich Bronchospasmus, zwischen Aspirin und anderen nichtsteroidalen entzündungshemmenden Arzneimitteln berichtet wurde, sollte PONSTEL (Mefenaminsäure) Patienten mit dieser Form der Aspirin-Sensitivität nicht verabreicht werden und sollte mit Vorsicht angewendet werden Patienten mit vorbestehendem Asthma.
Informationen für Patienten
Die Patienten sollten vor Beginn der Therapie mit einem NSAID und in regelmäßigen Abständen während der laufenden Therapie über die folgenden Informationen informiert werden. Die Patienten sollten auch ermutigt werden, das NSAID zu lesen Leitfaden für Medikamente die jedem abgegebenen Rezept beiliegt.
Labortests
Da schwerwiegende Geschwüre und Blutungen im Magen-Darm-Trakt ohne Warnsymptome auftreten können, sollte der Arzt auf Anzeichen oder Symptome einer Magen-Darm-Blutung achten. Patienten unter Langzeitbehandlung mit NSAIDs sollten ihr großes Blutbild und ihr chemisches Profil regelmäßig überprüfen lassen. Wenn sich klinische Anzeichen und Symptome entwickeln, die mit einer Leber- oder Nierenerkrankung einhergehen, systemische Manifestationen auftreten (z. B. Eosinophilie, Hautausschlag usw.) oder wenn abnormale Leberwerte bestehen bleiben oder sich verschlechtern, sollte Ponstel (Mefenaminsäure) abgesetzt werden.
Schwangerschaft
Teratogene Wirkungen
Schwangerschaftskategorie C
An Ratten und Kaninchen durchgeführte Reproduktionsstudien haben keine Hinweise auf Entwicklungsstörungen ergeben. Reproduktionsstudien an Tieren sind jedoch nicht immer prädiktiv für die Reaktion des Menschen. Es liegen keine adäquaten oder gut kontrollierten Studien bei Schwangeren vor. Postel sollte in der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt.
Nicht teratogene Wirkungen
Aufgrund der bekannten Wirkungen nichtsteroidaler Antirheumatika auf das fetale Herz-Kreislauf-System (Verschluss des Ductus arteriosus) sollte die Anwendung während der Schwangerschaft (insbesondere in der Spätschwangerschaft) vermieden werden.
Arbeit und Lieferung
In Rattenstudien mit NSAIDs, wie auch mit anderen Arzneimitteln, von denen bekannt ist, dass sie die Prostaglandinsynthese hemmen, trat eine erhöhte Inzidenz von Dystokie, verzögerter Geburt und verringerter Überlebensrate der Jungtiere auf. Die Auswirkungen von Ponstel (Mefenaminsäure) auf Wehen und Geburt bei Schwangeren sind nicht bekannt.
Stillende Mutter
Spuren von Ponstel (Mefenaminsäure) können in der Muttermilch vorhanden sein und auf den gestillten Säugling übertragen werden.7 Aufgrund der Möglichkeit schwerwiegender Nebenwirkungen bei gestillten Säuglingen durch PONSTEL (Mefenaminsäure) sollte eine Entscheidung getroffen werden, ob das Stillen beendet werden soll oder das Medikament abzusetzen, unter Berücksichtigung der Bedeutung des Medikaments für die Mutter.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten unter 14 Jahren wurden nicht nachgewiesen.
Geriatrische Verwendung
Klinische Studien mit Ponstel (Mefenaminsäure) schlossen keine ausreichende Anzahl von Probanden ab 65 Jahren ein, um festzustellen, ob sie anders reagieren als jüngere Probanden. Wie bei allen NSAIDs ist bei der Behandlung älterer Menschen (65 Jahre und älter) Vorsicht geboten.
Es ist bekannt, dass dieses Medikament im Wesentlichen über die Nieren ausgeschieden wird, und das Risiko toxischer Reaktionen auf dieses Medikament kann bei Patienten mit eingeschränkter Nierenfunktion größer sein. Da ältere Patienten eher eine eingeschränkte Nierenfunktion haben, sollte die Dosis sorgfältig ausgewählt werden und es kann sinnvoll sein, die Nierenfunktion zu überwachen (siehe KLINISCHE PHARMAKOLOGIE und NEBENWIRKUNGEN).
VERWEISE
7. Buchanan RA, et al. Die Ausscheidung von Mefenaminsäure aus der Muttermilch. Curr Ther Res. 10:592, 1968.
ÜBERDOSIS
Die Symptome nach einer akuten NSAID-Überdosierung beschränken sich in der Regel auf Lethargie, Benommenheit, Übelkeit, Erbrechen und epigastrische Schmerzen, die im Allgemeinen mit unterstützenden Maßnahmen reversibel sind. Gastrointestinale Hypertonie, akutes Nierenversagen, Atemdepression und Koma können auftreten, sind aber selten. Anaphylaktoide Reaktionen wurden bei therapeutischer Einnahme von NSAIDs berichtet und können nach einer Überdosierung auftreten.
Die Patienten sollten nach einer NSAID-Überdosierung symptomatisch und unterstützend behandelt werden. Es gibt keine spezifischen Gegenmittel. Erbrechen und/oder Aktivkohle (60 bis 100 g bei Erwachsenen, 1 bis 2 g/kg bei Kindern) und/oder osmotische Abführmittel können bei Patienten indiziert sein, die innerhalb von 4 Stunden nach der Einnahme mit Symptomen oder nach einer starken Überdosierung (5 bis 10 mal die übliche Dosis). Forcierte Diurese, Alkalisierung des Urins, Hämodialyse oder Hämoperfusion sind aufgrund der hohen Proteinbindung möglicherweise nicht sinnvoll.
KONTRAINDIKATIONEN
PONSTEL (Mefenaminsäure) ist bei Patienten mit bekannter Überempfindlichkeit gegen Mefenaminsäure kontraindiziert.
PONSTEL (Mefenaminsäure) sollte nicht an Patienten verabreicht werden, bei denen Asthma, Urtikaria oder allergische Reaktionen nach der Einnahme von Aspirin oder anderen NSAIDs aufgetreten sind. Bei solchen Patienten wurde über schwere, selten tödliche, anaphylaktische Reaktionen auf NSAIDs berichtet (s WARNHINWEISE – Anaphylaktoide Reaktionen und VORSICHTSMASSNAHMEN – Vorbestehendes Asthma ).
PONSTEL (Mefenaminsäure) ist kontraindiziert für die Behandlung von perioperativen Schmerzen im Rahmen einer Koronararterien-Bypass-Operation (CABG) (siehe WARNUNGEN ).
Ponstel (Mefenaminsäure) ist kontraindiziert bei Patienten mit akuter aktiver Ulzeration oder chronischer Entzündung des oberen oder unteren Gastrointestinaltrakts.
Ponstel (Mefenaminsäure) sollte bei Patienten mit vorbestehender Nierenerkrankung nicht angewendet werden.
KLINISCHE PHARMAKOLOGIE
Pharmakodynamik
Ponstel (Mefenaminsäure) ist ein nicht-steroidales entzündungshemmendes Medikament (NSAID), das in Tiermodellen entzündungshemmende, analgetische und antipyretische Aktivitäten zeigt. Der Wirkungsmechanismus von Ponstel (Mefenaminsäure) ist ebenso wie der anderer NSAIDs nicht vollständig geklärt, kann aber mit der Hemmung der Prostaglandin-Synthetase zusammenhängen.
Pharmakokinetik
Absorption
Mefenaminsäure wird nach oraler Verabreichung schnell resorbiert. In zwei Studien mit einer oralen Einzeldosis von 500 mg betrug das mittlere Ausmaß der Resorption 30,5 mcg/h/ml (17 % CV).1,2 Die Bioverfügbarkeit der Kapsel im Vergleich zu einer intravenösen Dosis oder einer Lösung zum Einnehmen wurde nicht untersucht.
Nach einer oralen Einzeldosis von 1 Gramm wurden mittlere Spitzenplasmaspiegel im Bereich von 10-20 mcg/ml3 berichtet. Maximale Plasmaspiegel werden nach 2 bis 4 Stunden erreicht und die Eliminationshalbwertszeit beträgt etwa 2 Stunden. Nach Mehrfachdosen sind die Plasmaspiegel proportional zur Dosis, ohne Anzeichen einer Arzneimittelakkumulation. In einer Mehrfachdosisstudie mit normalen erwachsenen Probanden (n = 6), die viermal täglich 1-Gramm-Dosen Mefenaminsäure erhielten, wurden Steady-State-Konzentrationen von 20 µg/ml am zweiten Tag der Verabreichung erreicht, was mit der kurzen Halbzeit übereinstimmt. Leben.
Die Auswirkung von Nahrung auf die Geschwindigkeit und das Ausmaß der Resorption von Mefenaminsäure wurde nicht untersucht. Es hat sich gezeigt, dass die gleichzeitige Einnahme von Antazida, die Magnesiumhydroxid enthalten, die Geschwindigkeit und das Ausmaß der Resorption von Mefenaminsäure signifikant erhöht (siehe VORSICHTSMASSNAHMEN: WECHSELWIRKUNGEN MIT ARZNEIMITTELN ).1
Verteilung
Es wurde berichtet, dass Mefenaminsäure zu mehr als 90 % an Albumin gebunden ist.9 Die Beziehung des ungebundenen Anteils zur Arzneimittelkonzentration wurde nicht untersucht. Das geschätzte scheinbare Verteilungsvolumen (Vzss/F) nach einer oralen Dosis von 500 mg Mefenaminsäure betrug 1,06 l/kg.2
Aufgrund seiner physikalischen und chemischen Eigenschaften wird erwartet, dass Ponstel (Mefenaminsäure) in die Muttermilch ausgeschieden wird.
Stoffwechsel
Mefenaminsäure wird durch das Cytochrom-P450-Enzym CYP2C9 zu 3-Hydroxymethylmefenaminsäure (Metabolit I) metabolisiert. Eine weitere Oxidation zu einer 3-Carboxymefenaminsäure (Metabolit II) kann erfolgen.10 Die Aktivität dieser Metaboliten wurde nicht untersucht. Die Metaboliten können einer Glucuronidierung unterzogen werden und Mefenaminsäure wird auch direkt glucuronidiert. Nach 3 Stunden wurde für den Hydroxymetaboliten und sein Glucuronid (n = 6) nach einer Einzeldosis von 1 Gramm ein maximaler Plasmaspiegel von etwa 20 µg/ml beobachtet. In ähnlicher Weise wurde für den Carboxy-Metaboliten und sein Glucuronid nach 6-8 Stunden ein maximaler Plasmaspiegel von 8 mcg/ml beobachtet.3
Ausscheidung
Etwa zweiundfünfzig Prozent einer Mefenaminsäure-Dosis werden hauptsächlich als Glucuronide von Mefenaminsäure (6 %), 3-Hydroxymefenaminsäure (25 %) und 3-Carboxymefenaminsäure (21 %) mit dem Urin ausgeschieden. Der fäkale Ausscheidungsweg macht bis zu 20 % der Dosis aus, hauptsächlich in Form von unkonjugierter 3-Carboxymefenaminsäure.3
Die Eliminationshalbwertszeit von Mefenaminsäure beträgt etwa zwei Stunden. Halbwertszeiten der Metaboliten I und II wurden nicht genau angegeben, scheinen aber länger zu sein als die der Ausgangssubstanz.3 Die Metaboliten können sich bei Patienten mit Nieren- oder Leberversagen anreichern. Das Mefenaminsäureglucuronid kann irreversibel an Plasmaproteine binden. Da sowohl die renale als auch die hepatische Ausscheidung wichtige Eliminationswege sind, kann eine Dosisanpassung bei Patienten mit Nieren- oder Leberfunktionsstörungen erforderlich sein. Ponstel (Mefenaminsäure) sollte Patienten mit vorbestehender Nierenerkrankung oder Patienten mit erheblich eingeschränkter Nierenfunktion nicht verabreicht werden.
TABELLE 1: Schätzwerte der pharmakokinetischen Parameter für Mefenaminsäure
Besondere Populationen
Pädiatrie
Ponstel (Mefenaminsäure) wurde bei pädiatrischen Patienten unter 14 Jahren nicht ausreichend untersucht. Eine Studie an 17 Frühgeborenen, denen 2 mg/kg verabreicht wurden, zeigte, dass die Halbwertszeit etwa fünfmal so lang war wie bei Erwachsenen, was mit der geringen Aktivität von Stoffwechselenzymen bei Neugeborenen übereinstimmt. Die mittlere Cmax in dieser Studie betrug 4 µg/ml (Bereich 2,9-6,1). Die mittlere Zeit bis zur maximalen Konzentration (Tmax) betrug 8 Stunden (Bereich 2-18 Stunden).11
Wettrennen
Rassenbedingte pharmakokinetische Unterschiede wurden nicht festgestellt.
Leberinsuffizienz
Die Pharmakokinetik von Mefenaminsäure wurde bei Patienten mit Leberfunktionsstörung nicht untersucht. Da der hepatische Metabolismus ein wichtiger Eliminationsweg von Mefenaminsäure ist, benötigen Patienten mit akuten und chronischen Lebererkrankungen im Vergleich zu Patienten mit normaler Leberfunktion möglicherweise geringere Dosen von Ponstel (Mefenaminsäure).
Niereninsuffizienz
Die Pharmakokinetik von Mefenaminsäure wurde bei Patienten mit Niereninsuffizienz nicht untersucht. Da Mefenaminsäure, ihre Metaboliten und Konjugate hauptsächlich über die Nieren ausgeschieden werden, besteht die Möglichkeit einer Akkumulation von Mefenaminsäure-Metaboliten. Ponstel (Mefenaminsäure) sollte Patienten mit vorbestehender Nierenerkrankung oder Patienten mit erheblich eingeschränkter Nierenfunktion nicht verabreicht werden.
Klinische Studien
In kontrollierten, doppelblinden, klinischen Studien wurde Ponstel (Mefenaminsäure) für die Behandlung von primärer krampfhafter Dysmenorrhö untersucht. Die zur Bestimmung der Wirksamkeit verwendeten Parameter umfassten die Schmerzbewertung durch Patient und Prüfarzt; die Notwendigkeit einer gleichzeitigen analgetischen Medikation; und Bewertung der Änderung der Häufigkeit und Schwere von Symptomen, die für spasmodische Dysmenorrhoe charakteristisch sind. Die Patienten erhielten entweder Ponstel (Mefenaminsäure), 500 mg (2 Kapseln) als Anfangsdosis von 250 mg alle 6 Stunden, oder Placebo zu Beginn der Blutung oder der Schmerzen, je nachdem, was zuerst einsetzte. Nach drei Menstruationszyklen wurden die Patientinnen für weitere drei Zyklen auf die alternative Behandlung umgestellt. Ponstel (Mefenaminsäure) war Placebo in allen Parametern signifikant überlegen, und beide Behandlungen (Arzneimittel und Placebo) wurden gleichermaßen vertragen.
VERWEISE
1. Neuvonen PJ, Kivisto KT: Verbesserung der Arzneimittelabsorption durch Antazida. Eine unerkannte Arzneimittelwechselwirkung. Clin Pharmacokinet. 27:120-8, August 1994.
2. Tall AR, Mistilits SP: Studien zu Ponstan (Mefenaminsäure): I. Magen-Darm-Blutverlust; II. Aufnahme und Ausscheidung einer neuen Formulierung. J Int Med Res (Vereinigtes Königreich). 1975, 3 (3) S. 176-82.
3. Winder CV, Kaump DH, Glazko et al: Experimentelle Beobachtungen von Flufenaminsäure, Mefenaminsäure und Meclofenaminsäure. AnnPhys Med (Eng), Suppl p7-49.1967.
9. Champion GD, Graham GG: Pharmakokinetik von nicht-steroidalen entzündungshemmenden Mitteln. Aust NZ J Med. 8 (Beilage 1): 94-100, Juni 1978.
10. McGurk KA, Remmel RP, Hosagrahara VP, Tosh D, Burchell B: Reaktivität von Mefenaminsäure-1-o-acylglucuronid mit Proteinen in vitro und ex vivo. Drug Metab Dispos. August 1996, 24 (8) S. 842-9.
11. Ito K, Niida Y, Sato J et al: Pharmakokinetik von Mefenaminsäure bei Frühgeborenen mit offenem Ductus arteriosus. Acta Paediatr JPN. 36 (4): 387-91, 1994.
INFORMATIONEN ZUM PATIENTEN
Leitfaden für Medikamente für nichtsteroidale Antirheumatika (NSAIDs)
(Eine Liste verschreibungspflichtiger NSAID-Medikamente finden Sie am Ende dieses Arzneimittelleitfadens.)
Was sind die wichtigsten Informationen, die ich über sogenannte nichtsteroidale Antirheumatika (NSAIDs) wissen sollte?
NSAID-Arzneimittel können die Wahrscheinlichkeit eines Herzinfarkts oder Schlaganfalls erhöhen, der zum Tod führen kann. Diese Chance steigt:
NSAID-Medikamente sollten niemals direkt vor oder nach einer Herzoperation, die als „Koronararterien-Bypass-Transplantation (CABG)“ bezeichnet wird, angewendet werden.
NSAR-Arzneimittel können jederzeit während der Behandlung Geschwüre und Blutungen im Magen und Darm verursachen.
Geschwüre und Blutungen:
Die Wahrscheinlichkeit, dass eine Person ein Geschwür oder eine Blutung bekommt, steigt mit:
NSAID-Arzneimittel sollten nur verwendet werden:
Was sind nichtsteroidale Antirheumatika (NSAIDs)?
NSAID-Arzneimittel werden zur Behandlung von Schmerzen und Rötungen, Schwellungen und Hitze (Entzündung) aufgrund von Erkrankungen wie:
Wer sollte kein nichtsteroidales Antirheumatikum (NSAID) einnehmen?
Nehmen Sie kein NSAID-Arzneimittel ein:
Informieren Sie Ihren Arzt:
Was sind die möglichen Nebenwirkungen von nichtsteroidalen Antirheumatika (NSAIDs)?
Holen Sie sofort Hilfe, wenn Sie eines der folgenden Symptome haben:
Setzen Sie Ihr NSAID-Medikament ab und rufen Sie sofort Ihren Arzt an, wenn Sie eines der folgenden Symptome haben:
Dies sind nicht alle Nebenwirkungen von NSAR-Arzneimitteln. Wenden Sie sich an Ihren Arzt oder Apotheker, um weitere Informationen zu NSAID-Medikamenten zu erhalten.
Weitere Informationen zu nichtsteroidalen Antirheumatika (NSAIDs)
NSAR-Medikamente, die verschreibungspflichtig sind
Dieser Medikationsleitfaden wurde von der US Food and Drug Administration genehmigt. Datum des Inkrafttretens: 19.02.2008