Desyrel 25mg, 50mg, 100mg Trazodone Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Desyrel 100 mg und wie wird es angewendet?
Desyrel 100 mg ist ein verschreibungspflichtiges Arzneimittel, das bei Erwachsenen zur Behandlung einer Major Depression (MDD) angewendet wird. Desyrel gehört zu einer Klasse von Arzneimitteln, die als SSRIs (oder selektive Serotonin-Wiederaufnahmehemmer) bekannt sind.
Welche Nebenwirkungen kann Desyrel haben?
Desyrel kann schwerwiegende Nebenwirkungen oder den Tod verursachen, einschließlich:
Nur einige Menschen sind für diese Probleme gefährdet. Möglicherweise möchten Sie sich einer Augenuntersuchung unterziehen, um festzustellen, ob Sie gefährdet sind, und eine vorbeugende Behandlung erhalten, wenn dies der Fall ist.
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Die häufigsten Nebenwirkungen von Desyrel sind:
Dies sind nicht alle möglichen Nebenwirkungen von Desyrel. Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
WARNUNG
Selbstmordgedanken und Verhaltensweisen
In Kurzzeitstudien erhöhten Antidepressiva das Risiko von Suizidgedanken und -verhalten bei pädiatrischen und jungen erwachsenen Patienten. Alle mit Antidepressiva behandelten Patienten müssen engmaschig auf eine klinische Verschlechterung und das Auftreten von Suizidgedanken und -verhalten überwacht werden [siehe WARNHINWEISE UND VORSICHTSMASSNAHMEN]. DESYREL ist nicht für die Anwendung bei pädiatrischen Patienten zugelassen [siehe Anwendung bei bestimmten Patientengruppen].
BEZEICHNUNG
DESYREL (Trazodonhydrochlorid) Tabletten zur oralen Verabreichung enthalten Trazodonhydrochlorid, einen selektiven Serotonin-Wiederaufnahmehemmer und 5HT2-Rezeptorantagonisten. DESYREL ist ein Triazolopyridin-Derivat mit der Bezeichnung 2-[3-[4-(3-Chlorphenyl)-1-piperazinyl]propyl]-1,2,4-triazolo[4,3-a]pyridin-3(2H)-on Hydrochlorid. Es ist ein weißes, geruchloses, kristallines Pulver, das in Wasser frei löslich ist. Die Strukturformel wird wie folgt dargestellt:
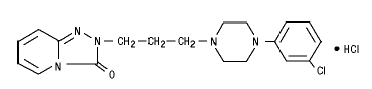
Molekularformel : C19H22CIN5O • HCl Molekulargewicht : 408,33
Jede Tablette zur oralen Verabreichung enthält 50 mg, 100 mg, 150 mg oder 300 mg Trazodonhydrochlorid, USP. Darüber hinaus enthält jede Tablette die folgenden Hilfsstoffe:
50 mg und 100 mg: Maisstärke, dibasisches Calciumphosphat, Hypromellose, Lactosemonohydrat, Magnesiumstearat, mikrokristalline Cellulose, Polyethylenglykol, Povidon, Natriumstärkeglykolat und Triacetin
150 mg: Magnesiumstearat, mikrokristalline Cellulose, vorgelatinierte Stärke und Stearinsäure
300 mg: Magnesiumstearat, mikrokristalline Cellulose, vorgelatinierte Stärke, Natriumstärkeglycolat und Stearinsäure
INDIKATIONEN
DESYREL® ist für die Behandlung von Major Depression (MDD) bei Erwachsenen indiziert.
DOSIERUNG UND ANWENDUNG
Dosisauswahl
Es wird eine Anfangsdosis von 150 mg/Tag in aufgeteilten Dosen empfohlen. Die Dosierung sollte mit einer niedrigen Dosis begonnen und schrittweise gesteigert werden, wobei das klinische Ansprechen und alle Anzeichen einer Unverträglichkeit zu beachten sind. Das Auftreten von Schläfrigkeit kann die Verabreichung eines größeren Teils der Tagesdosis vor dem Schlafengehen oder eine Dosisreduktion erfordern.
Die Dosis kann alle 3 bis 4 Tage um 50 mg/Tag erhöht werden. Die Höchstdosis für ambulante Patienten sollte in der Regel 400 mg/Tag in aufgeteilten Dosen nicht überschreiten. Stationären Patienten (dh schwerer depressiven Patienten) können bis zu, aber nicht mehr als 600 mg/Tag in aufgeteilten Dosen verabreicht werden.
Sobald ein angemessenes Ansprechen erreicht ist, kann die Dosis schrittweise reduziert werden, mit anschließender Anpassung je nach therapeutischem Ansprechen.
Wichtige Verwaltungsanweisungen
DESYREL® kann als Ganzes geschluckt oder als halbe Tablette verabreicht werden, indem die Tablette entlang der Bruchkerbe gebrochen wird.
DESYREL sollte kurz nach einer Mahlzeit oder einem leichten Snack eingenommen werden.
Screening auf bipolare Störung vor dem Start von DESYREL
Vor Beginn der Behandlung mit DESYREL 50 mg oder einem anderen Antidepressivum sollten Patienten auf eine persönliche oder familiäre Vorgeschichte von bipolarer Störung, Manie oder Hypomanie untersucht werden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Wechsel zu oder von Monoaminoxidase-Hemmern Antidepressivum
Zwischen dem Absetzen eines Monoaminooxidase-Hemmers (MAOI)-Antidepressivums und dem Beginn der Behandlung mit DESYREL müssen mindestens 14 Tage vergehen. Darüber hinaus müssen nach dem Absetzen von DESYREL 100 mg mindestens 14 Tage vergehen, bevor mit einem MAO-Hemmer-Antidepressivum begonnen werden kann [siehe KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Dosierungsempfehlungen für die gleichzeitige Anwendung mit starken CYP3A4-Hemmern oder -Induktoren
Gleichzeitige Verabreichung mit starken CYP3A4-Inhibitoren
Erwägen Sie, die Dosis von DESYREL 25 mg basierend auf der Verträglichkeit zu reduzieren, wenn DESYREL 100 mg zusammen mit einem starken CYP3A4-Hemmer verabreicht wird [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Gleichzeitige Verabreichung mit starken CYP3A4-Induktoren
Erwägen Sie eine Erhöhung der Dosis von DESYREL 100 mg basierend auf dem therapeutischen Ansprechen, wenn DESYREL 100 mg zusammen mit einem starken CYP3A4-Induktor verabreicht wird [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Absetzen der Behandlung mit DESYREL
Nach Absetzen von DESYREL können Nebenwirkungen auftreten [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ]. Reduzieren Sie die Dosierung schrittweise, anstatt DESYREL abrupt zu stoppen, wann immer dies möglich ist.
WIE GELIEFERT
Darreichungsformen und Stärken
Lagerung und Handhabung
50mg Weiße, runde Filmtablette mit Bruchrille; halbiert mit Prägung „50“ und „P 005“ auf der einen Seite und glatt auf der anderen Seite. Flaschen zu 100 NDC 58463-005-01
100mg : Weiße, runde Filmtablette mit Bruchrille; halbiert mit Prägung „100“ und „P 006“ auf der einen Seite und glatt auf der anderen Seite. Flaschen zu 100 NDC 58463-006-01
150mg : Weiße, rechteckige Tablette mit Bruchkerbe; Auf beiden Seiten dreigeteilt, auf der einen Seite mit „P“ und „007“ und auf der anderen Seite mit „50“, „50“, „50“ geprägt, mit einer Halbierung an jeder Kante. Flaschen zu 100 NDC 58463-007-01
300mg : Weiße, rechteckige Tablette mit Bruchrille; Auf der einen Seite dreigeteilt mit Prägung „100“, „100“, „100“ und auf der anderen Seite halbiert mit Prägung „P“ und „008“. Flaschen zu 100 NDC 58463-008-01
Bei 20 °C bis 25 °C (68 °F bis 77 °F) lagern. Abweichungen zwischen 15°C und 30°C (59°F bis 86°F) erlaubt [siehe USP kontrollierte Raumtemperatur ].
In einem dichten, lichtbeständigen Behälter gemäß USP abgeben.
Hergestellt in Kanada für: Pragma Pharmaceuticals, LLC. Vertrieb durch: Fera, Pharmaceuticals, LLC., Locust Valley, NY 11560. Überarbeitet im Okt.: 2018
NEBENWIRKUNGEN
Die folgenden schwerwiegenden Nebenwirkungen werden an anderer Stelle in der Kennzeichnung beschrieben:
Erfahrung mit klinischen Studien
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in den klinischen Studien zu einem Medikament beobachteten Nebenwirkungsraten nicht direkt mit den Raten in den klinischen Studien zu einem anderen Medikament verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Andere Nebenwirkungen, die bei der Anwendung von Trazodonhydrochlorid in den kontrollierten klinischen Studien mit einer Inzidenz von
Postmarketing-Erfahrung
Die folgenden Nebenwirkungen wurden während der Anwendung von DESYREL nach der Zulassung festgestellt. Da diese Reaktionen freiwillig aus einer Population unbekannter Größe gemeldet werden, ist es nicht immer möglich, ihre Häufigkeit abzuschätzen oder einen kausalen Zusammenhang mit der Arzneimittelexposition herzustellen:
Erkrankungen des Blutes und des Lymphsystems : hämolytische Anämie, Leukozytose
Herzerkrankungen Kardiospasmus, dekompensierte Herzinsuffizienz, Leitungsblock, orthostatische Hypotonie und Synkope, Palpitationen, Bradykardie, Vorhofflimmern, Myokardinfarkt, Herzstillstand, Arrhythmie, ventrikuläre ektopische Aktivität, einschließlich ventrikulärer Tachykardie und QT-Verlängerung. Verlängertes QT-Intervall, Torsade de Pointes und ventrikuläre Tachykardie wurden bei Dosen von 100 mg pro Tag oder weniger berichtet [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Endokrine Störungen : unangemessenes ADH-Syndrom
Augenerkrankungen : Diplopie
Gastrointestinale Störungen : erhöhter Speichelfluss, Übelkeit/Erbrechen
Allgemeine Erkrankungen und Beschwerden am Verabreichungsort : Schüttelfrost, Ödeme, ungeklärter Tod, Schwäche
Leber- und Gallenerkrankungen : Cholestase, Gelbsucht, Hyperbilirubinämie, Veränderungen der Leberenzyme
Untersuchungen : erhöhte Amylase
Stoffwechsel- und Ernährungsstörungen : Methämoglobinämie
Erkrankungen des Nervensystems Aphasie, Ataxie, Schlaganfall, extrapyramidale Symptome, Grand-Mal-Anfälle, Parästhesie, Spätdyskinesie, Schwindel
Psychische Störungen : anormale Träume, Erregung, Angst, Halluzinationen, Schlaflosigkeit, paranoide Reaktion, Psychose, Benommenheit
Erkrankungen der Nieren und Harnwege : Harninkontinenz, Harnverhalt
Störungen des Fortpflanzungssystems und der Brust : Brustvergrößerung oder Milchstau, Klitoris, Laktation, Priapismus [vgl WARNUNGEN UND VORSICHTSMASSNAHMEN ]
Erkrankungen der Atemwege, des Brustraums und Mediastinums : Apnoe
Erkrankungen der Haut und des Unterhautgewebes : Alopezie, Hirsutismus, Leukonychie, Pruritus, Psoriasis, Hautausschlag, Urtikaria
Gefäßerkrankungen : Vasodilatation
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Arzneimittel mit klinisch bedeutsamen Wechselwirkungen mit DESYREL
Drogenmissbrauch und -abhängigkeit
Kontrollierte Substanz
DESYREL® ist keine kontrollierte Substanz.
Missbrauch
Obwohl Trazodonhydrochlorid in präklinischen oder klinischen Studien nicht systematisch auf sein Missbrauchspotenzial untersucht wurde, wurden in den klinischen Studien mit Trazodonhydrochlorid keine Hinweise auf Drogensuchtverhalten gefunden.
WARNUNGEN
Eingeschlossen als Teil der VORSICHTSMASSNAHMEN Sektion.
VORSICHTSMASSNAHMEN
Suizidgedanken und Verhaltensweisen bei pädiatrischen und jungen erwachsenen Patienten
In gepoolten Analysen placebokontrollierter Studien mit Antidepressiva (SSRIs und andere Antidepressiva-Klassen), an denen etwa 77.000 erwachsene Patienten und über 4.400 pädiatrische Patienten teilnahmen, war die Häufigkeit von Suizidgedanken und -verhalten bei pädiatrischen und jungen erwachsenen Patienten bei mit Antidepressiva behandelten Patienten höher als bei Placebo-behandelten Patienten. Die Unterschiede zwischen Medikament und Placebo in der Anzahl der Fälle von Suizidgedanken und -verhalten pro 1000 behandelten Patienten sind in Tabelle 1 aufgeführt.
In keiner der pädiatrischen Studien traten Suizide auf. In den Studien mit Erwachsenen gab es Suizide, aber die Anzahl reichte nicht aus, um eine Schlussfolgerung über die Wirkung von Antidepressiva auf Suizide zu ziehen.
Es ist nicht bekannt, ob sich das Risiko von Suizidgedanken und -verhalten bei pädiatrischen und jungen erwachsenen Patienten auf eine längerfristige Anwendung, dh über vier Monate hinaus, erstreckt. Es gibt jedoch erhebliche Hinweise aus placebokontrollierten Erhaltungsstudien bei Erwachsenen mit MDD, dass Antidepressiva das Wiederauftreten von Depressionen verzögern.
Überwachen Sie alle mit Antidepressiva behandelten Patienten auf eine klinische Verschlechterung und das Auftreten von Suizidgedanken und -verhalten, insbesondere während der ersten Monate der Arzneimitteltherapie und bei Dosisänderungen. Beraten Sie Familienmitglieder oder Betreuer von Patienten, um auf Verhaltensänderungen zu achten und den Gesundheitsdienstleister zu warnen. Erwägen Sie eine Änderung des therapeutischen Schemas, einschließlich eines möglichen Absetzens von DESYREL 100 mg, bei Patienten, deren Depression sich anhaltend verschlimmert oder die aufkommende Suizidgedanken oder -verhalten zeigen.
Serotonin-Syndrom
Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRIs) und SSRIs, einschließlich DESYREL 25 mg, können das Serotonin-Syndrom auslösen, eine potenziell lebensbedrohliche Erkrankung. Das Risiko ist erhöht bei gleichzeitiger Anwendung von anderen serotonergen Arzneimitteln (einschließlich Triptanen, trizyklischen Antidepressiva, Fentanyl, Lithium, Tramadol, Tryptophan, Buspiron und Johanniskraut) und von Arzneimitteln, die den Stoffwechsel von Serotonin beeinträchtigen, dh MAO-Hemmern [sehen KONTRAINDIKATIONEN , WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ]. Ein Serotonin-Syndrom kann auch auftreten, wenn diese Medikamente allein verwendet werden.
Anzeichen und Symptome des Serotonin-Syndroms können Veränderungen des mentalen Status (z. B. Unruhe, Halluzinationen, Delirium und Koma), autonome Instabilität (z. B. Tachykardie, labiler Blutdruck, Schwindel, Diaphorese, Hitzewallungen, Hyperthermie), neuromuskuläre Symptome (z. B. Tremor, Steifheit, Myoklonus, Hyperreflexie, Koordinationsstörungen), Krampfanfälle und gastrointestinale Symptome (z. B. Übelkeit, Erbrechen, Durchfall).
Die gleichzeitige Anwendung von DESYREL mit MAO-Hemmern ist kontraindiziert. Darüber hinaus darf DESYREL nicht bei einem Patienten eingeleitet werden, der mit MAO-Hemmern wie Linezolid oder intravenösem Methylenblau behandelt wird. Es gab keine Berichte über die Verabreichung von Methylenblau auf anderen Wegen (wie z. B. Tabletten zum Einnehmen oder lokale Gewebeinjektion). Wenn es notwendig ist, bei einem Patienten, der DESYREL einnimmt, eine Behandlung mit einem MAO-Hemmer wie Linezolid oder intravenösem Methylenblau einzuleiten, setzen Sie DESYREL ab, bevor Sie eine Behandlung mit dem MAO-Hemmer beginnen [siehe KONTRAINDIKATIONEN , WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Überwachen Sie alle Patienten, die DESYREL 50 mg einnehmen, auf das Auftreten eines Serotonin-Syndroms. Brechen Sie die Behandlung mit DESYREL und allen begleitenden serotonergen Arzneimitteln sofort ab, wenn die oben genannten Symptome auftreten, und leiten Sie eine unterstützende symptomatische Behandlung ein. Wenn die gleichzeitige Anwendung von DESYREL mit anderen serotonergen Arzneimitteln klinisch gerechtfertigt ist, informieren Sie die Patienten über das erhöhte Risiko für ein Serotoninsyndrom und überwachen Sie sie auf Symptome.
Herzrhythmusstörungen
Klinische Studien weisen darauf hin, dass Trazodonhydrochlorid bei Patienten mit vorbestehender Herzerkrankung arrhythmogen sein kann. Zu den identifizierten Arrhythmien gehören isolierte VES, ventrikuläre Couplets, Tachykardie mit Synkope und Torsade de Pointes. Postmarketing-Ereignisse, einschließlich Torsade de Pointes, wurden bei Dosen von 100 mg oder weniger mit der schnell freisetzenden Form von DESYREL berichtet. DESYREL sollte auch bei Patienten mit Herzrhythmusstörungen in der Vorgeschichte sowie anderen Umständen vermieden werden, die das Risiko des Auftretens von Torsade de Pointes und/oder plötzlichem Herztod erhöhen können, einschließlich symptomatischer Bradykardie, Hypokaliämie oder Hypomagnesiämie und angeborener Erkrankungen Verlängerung des QT-Intervalls. DESYREL wird nicht zur Anwendung während der anfänglichen Genesungsphase nach einem Myokardinfarkt empfohlen. Bei der Verabreichung von DESYREL 100 mg an Patienten mit Herzerkrankungen ist Vorsicht geboten, und solche Patienten sollten engmaschig überwacht werden, da Antidepressiva (einschließlich DESYREL) Herzrhythmusstörungen verursachen können [siehe NEBENWIRKUNGEN ].
DESYREL verlängert das QT/QTc-Intervall. Die Anwendung von DESYREL sollte bei Patienten mit bekannter QT-Verlängerung oder in Kombination mit anderen Arzneimitteln vermieden werden, die CYP3A4-Hemmer sind (z. B. Itraconazol, Clarithromycin, Voriconazol) oder bekanntermaßen das QT-Intervall verlängern, einschließlich Antiarrhythmika der Klasse 1A (z. B. Chinidin, Procainamid). ) oder Antiarrhythmika der Klasse 3 (z. B. Amiodaron, Sotalol), bestimmte Antipsychotika (z. B. Ziprasidon, Chlorpromazin, Thioridazin) und bestimmte Antibiotika (z. B. Gatifloxacin). Die gleichzeitige Verabreichung von Arzneimitteln kann das Risiko von Herzrhythmusstörungen erhöhen [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Orthostatische Hypotonie und Synkope
Bei Patienten, die Trazodonhydrochlorid erhielten, wurde über Hypotonie einschließlich orthostatischer Hypotonie und Synkope berichtet. Die gleichzeitige Anwendung mit einem Antihypertensivum kann eine Verringerung der Dosis des Antihypertensivums erfordern.
Erhöhtes Blutungsrisiko
Arzneimittel, die in die Serotonin-Wiederaufnahmehemmung eingreifen, einschließlich DESYREL 100 mg, erhöhen das Risiko von Blutungsereignissen. Die gleichzeitige Anwendung von Aspirin, nichtsteroidalen Antirheumatika (NSAIDS), anderen Thrombozytenaggregationshemmern, Warfarin und anderen Antikoagulanzien kann dieses Risiko erhöhen. Fallberichte und epidemiologische Studien (Fall-Kontroll- und Kohortendesign) haben einen Zusammenhang zwischen der Einnahme von Arzneimitteln, die die Serotonin-Wiederaufnahme beeinträchtigen, und dem Auftreten von gastrointestinalen Blutungen gezeigt. Blutungsereignisse im Zusammenhang mit Arzneimitteln, die die Wiederaufnahme von Serotonin beeinträchtigen, reichen von Blutergüssen, Hämatomen, Epistaxis und Petechien bis hin zu lebensbedrohlichen Blutungen.
Informieren Sie die Patienten über das Blutungsrisiko bei gleichzeitiger Anwendung von DESYREL 25 mg und Thrombozytenaggregationshemmern oder Antikoagulanzien. Überwachen Sie bei Patienten, die Warfarin einnehmen, sorgfältig die Gerinnungsindizes, wenn Sie DESYREL beginnen, auftitrieren oder absetzen.
Priapismus
Fälle von Priapismus (schmerzhafte Erektionen, die länger als 6 Stunden andauern) wurden bei Männern berichtet, die DESYREL erhielten. Priapismus kann, wenn er nicht rechtzeitig behandelt wird, zu irreversiblen Schäden an den Schwellkörpern führen. Männer, die eine Erektion haben, die länger als 4 Stunden anhält, ob schmerzhaft oder nicht, sollten das Medikament sofort absetzen und einen Notarzt aufsuchen [siehe NEBENWIRKUNGEN , ÜBERDOSIERUNG ].
DESYREL 100 mg sollte bei Männern mit Erkrankungen, die sie für Priapismus prädisponieren könnten (z. B. Sichelzellenanämie, multiples Myelom oder Leukämie), oder bei Männern mit anatomischer Verformung des Penis (z. B. Angulation, Schwellkörperfibrose oder Peyronie-Krankheit).

Aktivierung von Manie oder Hypomanie
Bei Patienten mit bipolarer Störung kann die Behandlung einer depressiven Episode mit DESYREL 50 mg oder einem anderen Antidepressivum eine gemischte/manische Episode auslösen. Bei einem kleinen Teil der Patienten mit schweren affektiven Störungen, die mit Antidepressiva behandelt wurden, wurde über die Aktivierung von Manie/Hypomanie berichtet. Vor Beginn der Behandlung mit DESYREL sollten Patienten auf persönliche oder familiäre Vorgeschichte von bipolarer Störung, Manie oder Hypomanie untersucht werden [siehe DOSIERUNG UND ANWENDUNG ].
Abbruchsyndrom
Zu den Nebenwirkungen nach Absetzen von serotonergen Antidepressiva, insbesondere nach abruptem Absetzen, gehören: Übelkeit, Schwitzen, dysphorische Stimmung, Reizbarkeit, Unruhe, Schwindel, Sensibilitätsstörungen (z. Lethargie, emotionale Labilität, Schlaflosigkeit, Hypomanie, Tinnitus und Krampfanfälle. Wann immer möglich, wird eine allmähliche Reduzierung der Dosierung anstelle eines abrupten Absetzens empfohlen [siehe DOSIERUNG UND ANWENDUNG ].
Potenzial für kognitive und motorische Beeinträchtigungen
DESYREL® kann Schläfrigkeit oder Sedierung verursachen und die geistige und/oder körperliche Fähigkeit beeinträchtigen, die für die Durchführung potenziell gefährlicher Aufgaben erforderlich ist. Patienten sollten davor gewarnt werden, gefährliche Maschinen, einschließlich Autos, zu bedienen, bis sie hinreichend sicher sind, dass die medikamentöse Behandlung sie nicht beeinträchtigt.
Engwinkelglaukom
Die Pupillenerweiterung, die nach der Anwendung vieler Antidepressiva, einschließlich DESYREL 25 mg, auftritt, kann bei einem Patienten mit anatomisch engen Winkeln, der keine offene Iridektomie hat, eine Engwinkelattacke auslösen. Vermeiden Sie die Anwendung von Antidepressiva, einschließlich DESYREL, bei Patienten mit unbehandelten anatomisch engen Winkeln.
Hyponatriämie
Hyponatriämie kann als Folge einer Behandlung mit SNRIs und SSRIs, einschließlich DESYREL, auftreten. Es wurden Fälle mit Serumnatriumwerten unter 110 mmol/l berichtet. Anzeichen und Symptome einer Hyponatriämie sind Kopfschmerzen, Konzentrationsschwierigkeiten, Gedächtnisstörungen, Verwirrtheit, Schwäche und Unsicherheit, die zu Stürzen führen können. Anzeichen und Symptome im Zusammenhang mit schwereren und/oder akuten Fällen waren Halluzinationen, Synkopen, Krampfanfälle, Koma, Atemstillstand und Tod. In vielen Fällen scheint diese Hyponatriämie das Ergebnis des Syndroms der inadäquaten Sekretion des antidiuretischen Hormons (SIADH) zu sein.
Bei Patienten mit symptomatischer Hyponatriämie DESYREL 25 mg absetzen und eine geeignete medizinische Intervention einleiten. Ältere Patienten, Patienten, die Diuretika einnehmen, und Patienten mit Volumenmangel können unter SSRIs und SNRIs einem höheren Risiko ausgesetzt sein, eine Hyponatriämie zu entwickeln [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
Informationen zur Patientenberatung
Weisen Sie den Patienten an, die von der FDA zugelassene Patientenkennzeichnung ( Leitfaden für Medikamente ).
Selbstmordgedanken und Verhaltensweisen
Weisen Sie Patienten und Pflegepersonal an, auf das Auftreten von Suizidalität zu achten, insbesondere zu Beginn der Behandlung und wenn die Dosis nach oben oder unten angepasst wird, und weisen Sie sie an, solche Symptome dem medizinischen Fachpersonal zu melden [siehe KASTENWARNUNG und WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Dosierung und Anwendung
Weisen Sie die Patienten darauf hin, dass DESYREL kurz nach einer Mahlzeit oder einem leichten Snack eingenommen werden sollte. Weisen Sie die Patienten darauf hin, wie wichtig es ist, die Anweisungen zur Dosistitration zu befolgen [siehe DOSIERUNG UND ANWENDUNG ].
Serotonin-Syndrom
Warnen Sie Patienten vor dem Risiko eines Serotonin-Syndroms, insbesondere bei gleichzeitiger Anwendung von DESYREL mit anderen serotonergen Arzneimitteln, einschließlich Triptanen, trizyklischen Antidepressiva, Fentanyl, Lithium, Tramadol, Tryptophan, Buspiron, Johanniskraut und mit Arzneimitteln, die den Serotoninstoffwechsel beeinträchtigen ( insbesondere MAO-Hemmer, sowohl solche, die zur Behandlung psychiatrischer Störungen bestimmt sind, als auch andere, wie Linezolid). Patienten sollten sich an ihren Arzt wenden oder sich in der Notaufnahme melden, wenn sie Anzeichen oder Symptome eines Serotonin-Syndroms bemerken [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN und WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Aktivierung von Manie/Hypomanie
Weisen Sie die Patienten und ihre Betreuer an, auf Anzeichen einer Aktivierung von Manie/Hypomanie zu achten, und weisen Sie sie an, solche Symptome dem medizinischen Fachpersonal zu melden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Erhöhtes Blutungsrisiko
Informieren Sie die Patienten über die gleichzeitige Anwendung von DESYREL mit Aspirin, NSAIDs, anderen Thrombozytenaggregationshemmern, Warfarin oder anderen Antikoagulanzien, da die kombinierte Anwendung von Arzneimitteln, die die Serotonin-Wiederaufnahme beeinträchtigen, und diesen Arzneimitteln mit einem erhöhten Blutungsrisiko in Verbindung gebracht wurde. Raten Sie ihnen, ihren Arzt zu informieren, wenn sie verschreibungspflichtige oder rezeptfreie Medikamente einnehmen oder die Einnahme planen, die das Blutungsrisiko erhöhen [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Abbruchsyndrom
Weisen Sie die Patienten darauf hin, DESYREL 100 mg nicht abrupt abzusetzen und ein Ausschleichen mit ihrem Arzt zu besprechen. Nebenwirkungen können auftreten, wenn DESYREL 50 mg abgesetzt wird [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Begleitmedikation
Raten Sie den Patienten, ihren Arzt zu informieren, wenn sie verschreibungspflichtige oder rezeptfreie Medikamente einnehmen oder planen, diese einzunehmen, da die Möglichkeit von Wechselwirkungen besteht [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Schwangerschaft
Weisen Sie Patientinnen darauf hin, ihren Arzt zu informieren, wenn sie schwanger werden oder beabsichtigen, während der Therapie mit DESYREL schwanger zu werden. Weisen Sie die Patientinnen darauf hin, dass es ein Schwangerschaftsexpositionsregister gibt, das die Schwangerschaftsausgänge bei Frauen überwacht, die während der Schwangerschaft DESYREL 25 mg ausgesetzt waren [siehe Verwendung in speziellen Bevölkerungsgruppen ].
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Karzinogenese
Bei Ratten, die Trazodon in oralen Tagesdosen bis zum 7,3-fachen der maximal empfohlenen Humandosis (MRHD) von 400 mg/Tag bei Erwachsenen auf mg/m²-Basis erhielten, war kein arzneimittel- oder dosisabhängiges Auftreten von Karzinogenese erkennbar.
Mutagenese
Mit Trazodon wurden keine Genotoxizitätsstudien durchgeführt.
Beeinträchtigung der Fruchtbarkeit
Trazodon hat bei Ratten in Dosen bis zum 7,3-fachen der MRHD bei Erwachsenen auf mg/m²-Basis keinen Einfluss auf die Fertilität.
Verwendung in bestimmten Bevölkerungsgruppen
Schwangerschaft
Schwangerschafts-Expositionsregister
Es gibt ein Schwangerschafts-Expositionsregister, das die Schwangerschaftsausgänge bei Frauen überwacht, die während der Schwangerschaft Antidepressiva ausgesetzt waren. Gesundheitsdienstleister werden ermutigt, Patienten zu registrieren, indem sie das National Pregnancy Registry for Antidepressants unter 1-844-405-6185 anrufen oder online unter https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/antidepressants/ besuchen.
Zusammenfassung der Risiken
Veröffentlichte prospektive Kohortenstudien, Fallserien und Fallberichte über mehrere Jahrzehnte mit der Anwendung von DESYREL 50 mg bei Schwangeren haben keine arzneimittelbedingten Risiken für schwerwiegende Geburtsfehler, Fehlgeburten oder unerwünschte mütterliche oder fetale Folgen identifiziert (siehe Daten ). Es wurde gezeigt, dass Trazodonhydrochlorid bei Ratten eine erhöhte fetale Resorption und andere Nebenwirkungen auf den Fötus verursacht, wenn es in Dosierungen verabreicht wird, die etwa dem 7,3- bis 11-Fachen der maximal empfohlenen Humandosis (MRHD) von 400 mg/Tag bei Erwachsenen auf einem mg/m² entsprechen Basis. Es gab auch eine Zunahme angeborener Anomalien beim Kaninchen bei etwa dem 7,3- bis 22-fachen der MRHD auf mg/m²-Basis (siehe Daten ).
Das geschätzte Hintergrundrisiko schwerer Geburtsfehler und Fehlgeburten für die angegebene Population ist unbekannt. Alle Schwangerschaften haben ein Hintergrundrisiko für Geburtsfehler, Verlust oder andere nachteilige Folgen. In der US-Allgemeinbevölkerung liegt das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten bei klinisch erkannten Schwangerschaften bei 2 bis 4 % bzw. 15 bis 20 %.
Klinische Überlegungen
Krankheitsbedingtes mütterliches und/oder embryofetales Risiko
Eine prospektive Längsschnittstudie folgte 201 schwangeren Frauen mit einer Vorgeschichte von schweren depressiven Störungen, die euthymisch waren und zu Beginn der Schwangerschaft Antidepressiva einnahmen. Frauen, die Antidepressiva während der Schwangerschaft absetzten, erlitten mit größerer Wahrscheinlichkeit einen Rückfall einer schweren Depression als Frauen, die Antidepressiva weiter einnahmen. Berücksichtigen Sie das Risiko einer unbehandelten Depression, wenn Sie die Behandlung mit Antidepressiva während der Schwangerschaft und nach der Geburt abbrechen oder ändern.
Daten
Menschliche Daten
Während verfügbare Studien das Fehlen eines Risikos nicht definitiv belegen können, haben veröffentlichte Daten aus prospektiven Kohortenstudien, Fallserien und Fallberichten über mehrere Jahrzehnte keinen Zusammenhang mit der Anwendung von Trazodon während der Schwangerschaft und schwerwiegenden Geburtsfehlern, Fehlgeburten oder anderen unerwünschten mütterlichen oder fetalen Nebenwirkungen festgestellt Ergebnisse. Alle verfügbaren Studien haben methodische Einschränkungen, einschließlich kleiner Stichprobengröße und inkonsistenter Vergleichsgruppen.
Tierdaten
Es wurden keine teratogenen Wirkungen beobachtet, wenn Trazodon trächtigen Ratten und Kaninchen während der Organogenese in oralen Dosen von bis zu 450 mg/kg/Tag verabreicht wurde. Diese Dosis entspricht bei Ratten bzw. Kaninchen dem 11- bzw. 22-Fachen der maximal empfohlenen Humandosis (MRHD) von 400 mg/Tag bei Erwachsenen auf mg/m²-Basis. Erhöhte fötale Resorption und andere nachteilige Wirkungen auf den Fötus wurden bei Ratten beim 7,3- bis 11-fachen der MRHD und eine Zunahme angeborener Anomalien bei Kaninchen beim 7,3- bis 22-fachen der MRHD auf mg/m²-Basis beobachtet. Weitere Details zu diesen Studien liegen nicht vor.
Stillzeit
Zusammenfassung der Risiken
Daten aus der veröffentlichten Literatur berichten über den Übergang von Trazodon in die Muttermilch. Es liegen keine Daten zur Wirkung von Trazodon auf die Milchproduktion vor. Begrenzte Daten aus Berichten nach Markteinführung haben keinen Zusammenhang mit unerwünschten Wirkungen auf das gestillte Kind identifiziert. Die Entwicklungs- und Gesundheitsvorteile des Stillens sollten zusammen mit dem klinischen Bedarf der Mutter an DESYREL und möglichen Nebenwirkungen von DESYREL oder der zugrunde liegenden Erkrankung der Mutter auf das gestillte Kind berücksichtigt werden.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit bei Kindern und Jugendlichen wurden nicht nachgewiesen. Antidepressiva erhöhten das Risiko von Suizidgedanken und -verhalten bei pädiatrischen Patienten [siehe Eingerahmte Warnung , WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Geriatrische Verwendung
Berichtete klinische Literatur und Erfahrungen mit Trazodon haben keine Unterschiede im Ansprechen zwischen älteren und jüngeren Patienten festgestellt. Da jedoch die Erfahrung mit Trazodonhydrochlorid bei älteren Patienten begrenzt ist, sollte es bei geriatrischen Patienten mit Vorsicht angewendet werden.
Serotonerge Antidepressiva wurden mit Fällen von klinisch signifikanter Hyponatriämie bei älteren Patienten in Verbindung gebracht, die möglicherweise ein höheres Risiko für diese Nebenwirkung haben [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Nierenfunktionsstörung
Trazodon wurde bei Patienten mit eingeschränkter Nierenfunktion nicht untersucht. Trazodon sollte bei dieser Patientengruppe mit Vorsicht angewendet werden.
Leberfunktionsstörung
Trazodon wurde bei Patienten mit eingeschränkter Leberfunktion nicht untersucht. Trazodon sollte bei dieser Patientengruppe mit Vorsicht angewendet werden.
ÜBERDOSIS
Todesfälle durch Überdosierung sind bei Patienten aufgetreten, die DESYREL und andere zentral dämpfende Arzneimittel (Alkohol, Alkohol und Chloralhydrat und Diazepam, Amobarbital, Chlordiazepoxid oder Meprobamat) gleichzeitig eingenommen haben.
Die schwersten berichteten Reaktionen bei einer Überdosierung von DESYREL allein waren Priapismus, Atemstillstand, Krampfanfälle und EKG-Veränderungen, einschließlich QT-Verlängerung. Die am häufigsten berichteten Reaktionen waren Benommenheit und Erbrechen. Eine Überdosierung kann eine Zunahme der Inzidenz oder des Schweregrades einer der berichteten Nebenwirkungen verursachen.
Es gibt kein spezifisches Antidot für eine Überdosierung mit Trazodonhydrochlorid. Berücksichtigen Sie bei der Behandlung einer Überdosierung die Möglichkeit einer Beteiligung mehrerer Arzneimittel. Wenden Sie sich für aktuelle Informationen zum Umgang mit Vergiftungen oder Überdosierungen an eine Giftnotrufzentrale (1-800-222-1222 oder www.poison.org).
KONTRAINDIKATIONEN
DESYREL 25mg ist kontraindiziert bei:
KLINISCHE PHARMAKOLOGIE
Wirkmechanismus
Der Mechanismus der antidepressiven Wirkung von Trazodon ist nicht vollständig geklärt, es wird jedoch angenommen, dass es mit seiner Verstärkung der serotonergen Aktivität im ZNS zusammenhängt. Trazodon ist sowohl ein selektiver Serotonin-Wiederaufnahmehemmer (SSRI) als auch ein 5HT2-Rezeptorantagonist, und das Nettoergebnis dieser Wirkung auf die serotonerge Übertragung und seine Rolle bei der antidepressiven Wirkung von Trazodon ist unbekannt.
Pharmakodynamik
Präklinische Studien haben gezeigt, dass Trazodon selektiv die neuronale Wiederaufnahme von Serotonin (Ki = 367 nM) hemmt und als Antagonist an 5-HT-2A-Serotoninrezeptoren (Ki = 35,6 nM) wirkt. Trazodon ist auch ein Antagonist an mehreren anderen monoaminergen Rezeptoren, einschließlich 5-HT2B (Ki = 78,4 nM), 5-HT2C (Ki = 224 nM), α1A (Ki = 153 nM), α2C (Ki = 155 nM) Rezeptoren und es ist ein partieller Agonist am 5-HT1A (Ki = 118 nM)-Rezeptor.
Trazodon antagonisiert alpha-1-adrenerge Rezeptoren, eine Eigenschaft, die mit posturaler Hypotonie in Verbindung gebracht werden kann.
Pharmakokinetik
Absorption
Beim Menschen wird Trazodonhydrochlorid nach oraler Gabe ohne selektive Lokalisation in irgendeinem Gewebe resorbiert. Wenn Trazodonhydrochlorid kurz nach der Nahrungsaufnahme eingenommen wird, kann es zu einem Anstieg der resorbierten Arzneimittelmenge, einer Abnahme der maximalen Konzentration und einer Verlängerung der Zeit bis zur maximalen Konzentration kommen. Maximale Plasmaspiegel treten etwa eine Stunde nach der Einnahme auf, wenn Trazodonhydrochlorid auf nüchternen Magen eingenommen wird, oder 2 Stunden nach der Einnahme, wenn es zusammen mit einer Mahlzeit eingenommen wird.
Stoffwechsel
In-vitro-Studien an menschlichen Lebermikrosomen zeigen, dass Trazodon durch CYP3A4 über oxidative Spaltung zu einem aktiven Metaboliten, Mchlorphenylpiperazin (mCPP), metabolisiert wird. Andere Stoffwechselwege, die möglicherweise am Metabolismus von Trazodon beteiligt sind, wurden nicht gut charakterisiert. Trazodon wird weitgehend metabolisiert; weniger als 1 % einer oralen Dosis wird unverändert im Urin ausgeschieden.
Beseitigung
Bei manchen Patienten kann sich Trazodon im Plasma anreichern.
Proteinbindung
Trazodon ist in vitro bei Konzentrationen, die mit therapeutischen Dosen beim Menschen erreicht werden, zu 89 bis 95 % proteingebunden.
Klinische Studien
Die Wirksamkeit und Sicherheit von Trazodonhydrochlorid wurden in stationären und ambulanten Studien mit der Formulierung von Trazodon mit sofortiger Freisetzung bei der Behandlung von schweren depressiven Störungen nachgewiesen.
INFORMATIONEN ZUM PATIENTEN
DESYREL® (DEZ ur el) (Trazodonhydrochlorid) Tabletten zum Einnehmen
Was sind die wichtigsten Informationen, die ich über DESYREL wissen sollte?
Antidepressiva, Depressionen oder andere schwere psychische Erkrankungen und Selbstmordgedanken oder -handlungen: Sprechen Sie mit Ihrem Arzt über:
Rufen Sie sofort einen Arzt an, wenn Sie eines der folgenden Symptome haben, insbesondere wenn sie neu oder schlimmer sind oder Sie beunruhigen:
Was muss ich sonst noch über Antidepressiva wissen?
Es ist nicht bekannt, ob DESYREL bei Kindern sicher und wirksam ist.
Was ist DESYREL 100 mg?
DESYREL ist ein verschreibungspflichtiges Arzneimittel, das bei Erwachsenen zur Behandlung einer Major Depression (MDD) angewendet wird. DESYREL gehört zu einer Klasse von Arzneimitteln, die als SSRIs (oder selektive Serotonin-Wiederaufnahmehemmer) bekannt sind.
Desyrel darf nicht eingenommen werden:
Bevor Sie DESYREL einnehmen, informieren Sie Ihren Arzt über alle Ihre Erkrankungen, auch wenn Sie:
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen, einschließlich verschreibungspflichtiger und rezeptfreier Arzneimittel, Vitamine und Kräuterergänzungen. Die Anwendung von DESYREL mit bestimmten anderen Arzneimitteln kann sich gegenseitig beeinflussen und schwerwiegende Nebenwirkungen verursachen.
Informieren Sie Ihren Arzt insbesondere, wenn Sie Folgendes einnehmen:
Informieren Sie sich über die Medikamente, die Sie einnehmen. Führen Sie eine Liste darüber und zeigen Sie diese Ihrem Arzt und Apotheker, wenn Sie ein neues Arzneimittel erhalten.
Wie sollte ich DESYREL 25 mg einnehmen?
Was sollte ich während der Einnahme von DESYREL 25 mg vermeiden?
Welche Nebenwirkungen kann DESYREL haben?
DESYREL 100 mg kann schwerwiegende Nebenwirkungen oder den Tod verursachen, einschließlich:
Nur einige Menschen sind für diese Probleme gefährdet. Möglicherweise möchten Sie sich einer Augenuntersuchung unterziehen, um festzustellen, ob Sie gefährdet sind, und eine vorbeugende Behandlung erhalten, wenn dies der Fall ist.
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigsten Nebenwirkungen von DESYREL gehören:
Dies sind nicht alle möglichen Nebenwirkungen von DESYREL. Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
Wie ist DESYREL 100 mg aufzubewahren?
Bewahren Sie DESYREL 100 mg und alle Arzneimittel außerhalb der Reichweite von Kindern auf.
Allgemeine Informationen zur sicheren und wirksamen Anwendung von DESYREL.
Medikamente werden manchmal für andere als die in einem Medikationsleitfaden aufgeführten Zwecke verschrieben. Verwenden Sie DESYREL 100 mg nicht für einen Zustand, für den es nicht verschrieben wurde. Geben Sie DESYREL 25 mg nicht an andere Personen, selbst wenn diese die gleichen Symptome wie Sie haben. Es kann ihnen schaden. Sie können Ihren Apotheker oder Gesundheitsdienstleister nach Informationen zu DESYREL 100 mg fragen, die für Angehörige der Gesundheitsberufe bestimmt sind.
Was sind die Inhaltsstoffe von DESYREL 100 mg?
Wirkstoff: Trazo Done Hydrochlorid, USP
Inaktive Zutaten: 50 mg und 100 mg: Maisstärke, dibasisches Calciumphosphat, Hypromellose, Lactosemonohydrat, Magnesiumstearat, mikrokristalline Cellulose, Polyethylenglykol, Povidon, Natriumstärkeglykolat und Triacetin 150 mg: Magnesiumstearat, mikrokristalline Cellulose, vorgelatinierte Stärke und Stearinsäure 300 mg: Magnesiumstearat, mikrokristalline Cellulose, vorgelatinierte Stärke, Natriumstärkeglycolat und Stearinsäure
Dieser Medikationsleitfaden wurde von der US Food and Drug Administration genehmigt.