Luvox 100mg, 50mg Fluvoxamine Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Luvox (Fluvoxaminmaleat) und wie wird es angewendet?
Luvox 100 mg ist ein verschreibungspflichtiges Arzneimittel zur Behandlung der Symptome von Zwangsstörungen. Luvox kann allein oder mit anderen Medikamenten verwendet werden.
Luvox 100 mg gehört zu einer Klasse von Arzneimitteln, die Antidepressiva, SSRIs genannt werden.
Es ist nicht bekannt, ob Luvox 100 mg bei Kindern unter 8 Jahren sicher und wirksam ist.
Welche Nebenwirkungen kann Luvox haben?
Luvox kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Die häufigsten Nebenwirkungen von Luvox 50 mg sind:
Teilen Sie dem Arzt mit, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Luvox. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
SUIZIDALITÄT UND ANTIDEPRESSIONSMITTEL
Antidepressiva erhöhten im Vergleich zu Placebo das Risiko für suizidales Denken und Verhalten (Suizidalität) bei Kindern, Jugendlichen und jungen Erwachsenen in Kurzzeitstudien zu Major Depression (MDD) und anderen psychiatrischen Erkrankungen. Jeder, der die Anwendung von Fluvox 50 mgaminmaleat-Tabletten oder anderen Antidepressiva bei einem Kind, Jugendlichen oder jungen Erwachsenen in Betracht zieht, muss dieses Risiko mit der klinischen Notwendigkeit abwägen. Kurzzeitstudien zeigten bei Erwachsenen über 24 Jahren keine Erhöhung des Suizidalitätsrisikos mit Antidepressiva im Vergleich zu Placebo; Bei Erwachsenen ab 65 Jahren war das Risiko unter Antidepressiva im Vergleich zu Placebo geringer. Depressionen und bestimmte andere psychiatrische Störungen sind selbst mit einem erhöhten Suizidrisiko verbunden. Patienten jeden Alters, die mit einer antidepressiven Therapie begonnen werden, sollten angemessen überwacht und engmaschig auf klinische Verschlechterung, Suizidalität oder ungewöhnliche Verhaltensänderungen beobachtet werden. Familien und Betreuer sollten auf die Notwendigkeit einer genauen Beobachtung und Kommunikation mit dem verschreibenden Arzt hingewiesen werden. Fluvox 50 mgamin Maleat Tabletten sind nicht für die Anwendung bei pädiatrischen Patienten zugelassen, mit Ausnahme von Patienten mit Zwangsstörungen (OCD). [Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN - Klinische Verschlechterung und Suizidrisiko ].
BEZEICHNUNG
Fluvoxaminmaleat ist ein selektiver Serotonin (5-HT)-Wiederaufnahmehemmer (SSRI) aus der chemischen Reihe der 2-Aminoethyloximether von Aralkylketonen.
Es wird chemisch als 5-Methoxy-4'-(trifluormethyl)valerophenon-(E)-O-(2-aminoethyl)oximmaleat (1:1) bezeichnet und hat die empirische Formel C15H21O2N2F3·C4H4O4. Sein Molekulargewicht beträgt 434,41. Die Strukturformel lautet:
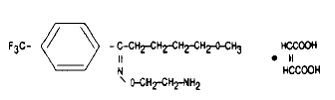
Fluvox 100 mg Aminmaleat ist ein weißes bis cremefarbenes, geruchloses, kristallines Pulver, das in Wasser schwer löslich, in Ethanol und Chloroform frei löslich und in Diethylether praktisch unlöslich ist.
Fluvoxaminmaleat-Tabletten sind in Stärken von 25 mg, 50 mg und 100 mg zur oralen Verabreichung erhältlich. Zusätzlich zum Wirkstoff Fluvox 100 mgaminmaleat enthält jede Tablette die folgenden Hilfsstoffe: Carnaubawachs, Hypromellose, Mannit, Polyethylenglykol, Polysorbat 80, vorverkleisterte Stärke (Kartoffel), Siliciumdioxid, Natriumstearylfumarat, Stärke (Mais), und Titandioxid. Die 50-mg- und 100-mg-Tabletten enthalten außerdem synthetische Eisenoxide.
INDIKATIONEN
Zwangsstörung
Fluvoxaminmaleat-Tabletten sind angezeigt zur Behandlung von Zwangsgedanken und Zwangshandlungen bei Patienten mit Zwangsstörungen (OCD), wie in DSM-III-R oder DSM-IV definiert. Die Zwangsgedanken oder Zwangshandlungen verursachen erhebliches Leiden, sind zeitraubend oder beeinträchtigen das soziale oder berufliche Funktionieren erheblich.
Zwangsstörungen sind gekennzeichnet durch wiederkehrende und anhaltende Ideen, Gedanken, Impulse oder Vorstellungen (Obsessionen), die Ich-dystonisch sind, und/oder sich wiederholende, zielgerichtete und absichtliche Verhaltensweisen (Zwänge), die von der Person als übertrieben oder unvernünftig erkannt werden.
Die Wirksamkeit von Fluvox 100-mgamin-Maleat-Tabletten wurde in vier Studien mit ambulanten Patienten mit Zwangsstörungen nachgewiesen: zwei 10-wöchige Studien mit Erwachsenen, eine 10-wöchige Studie mit pädiatrischen Patienten (Alter 8-17) und eine Erhaltungsstudie mit Erwachsenen [siehe Klinische Studien ].
DOSIERUNG UND ANWENDUNG
Erwachsene
Die empfohlene Anfangsdosis für Fluvox 50-mgamin-Maleat-Tabletten bei erwachsenen Patienten beträgt 50 mg, verabreicht als tägliche Einzeldosis vor dem Schlafengehen. In den kontrollierten klinischen Studien, in denen die Wirksamkeit von Fluvoxaminmaleat-Tabletten bei Zwangsstörungen nachgewiesen wurde, wurden die Patienten innerhalb eines Dosisbereichs von 100 bis 300 mg/Tag titriert. Folglich sollte die Dosis je nach Verträglichkeit alle 4 bis 7 Tage in 50-mg-Schritten erhöht werden, bis der maximale therapeutische Nutzen erreicht ist, und 300 mg pro Tag nicht überschreiten. Es wird empfohlen, eine Tagesgesamtdosis von mehr als 100 mg in zwei getrennten Dosen zu verabreichen. Wenn die Dosen nicht gleich sind, sollte die größere Dosis vor dem Schlafengehen gegeben werden.
Pädiatrische Population (Kinder und Jugendliche)
Die empfohlene Anfangsdosis für Fluvoxaminmaleat-Tabletten bei Kindern und Jugendlichen (im Alter von 8 bis 17 Jahren) beträgt 25 mg, verabreicht als tägliche Einzeldosis vor dem Schlafengehen. In einer kontrollierten klinischen Studie zur Untersuchung der Wirksamkeit von Fluvoxaminmaleat-Tabletten bei Zwangsstörungen wurden pädiatrische Patienten (im Alter von 8 bis 17 Jahren) innerhalb eines Dosisbereichs von 50 bis 200 mg/Tag titriert. Ärzte sollten bei der Dosierung von pädiatrischen Patienten Alters- und Geschlechtsunterschiede berücksichtigen. Die maximale Dosis bei Kindern bis zum Alter von 11 Jahren sollte 200 mg/Tag nicht überschreiten. Eine therapeutische Wirkung bei weiblichen Kindern kann mit niedrigeren Dosen erzielt werden. Eine Dosisanpassung bei Jugendlichen (bis zur Maximaldosis von 300 mg für Erwachsene) kann angezeigt sein, um einen therapeutischen Nutzen zu erzielen. Die Dosis sollte je nach Verträglichkeit alle 4 bis 7 Tage in 25-mg-Schritten erhöht werden, bis der maximale therapeutische Nutzen erreicht ist. Es wird empfohlen, eine Tagesgesamtdosis von mehr als 50 mg in zwei getrennten Dosen zu verabreichen. Wenn die beiden aufgeteilten Dosen nicht gleich sind, sollte die größere Dosis vor dem Schlafengehen gegeben werden.
Ältere oder hepatisch eingeschränkte Patienten
Bei älteren Patienten und Patienten mit eingeschränkter Leberfunktion wurde eine verringerte Clearance von Fluvoxaminmaleat beobachtet. Daher kann es angebracht sein, die Anfangsdosis und die anschließende Dosistitration für diese Patientengruppen zu modifizieren.
Umstellung eines Patienten auf oder von einem Monoaminoxidase-Hemmer (MAOI) zur Behandlung psychiatrischer Störungen
Zwischen dem Absetzen eines MAO-Hemmers zur Behandlung psychiatrischer Erkrankungen und dem Beginn einer Therapie mit Fluvox 50 mg-Maleat-Tabletten sollten mindestens 14 Tage vergehen. Umgekehrt sollten nach dem Absetzen von Fluvox 100 mg-Maleat-Tabletten mindestens 14 Tage gewartet werden, bevor mit einem MAO-Hemmer begonnen wird, der zur Behandlung psychiatrischer Erkrankungen bestimmt ist [siehe KONTRAINDIKATIONEN ].
Verwendung von Fluvoxaminmaleat-Tabletten mit anderen MAOIs wie Linezolid oder Methylenblau
Beginnen Sie nicht mit Fluvoxaminmaleat-Tabletten bei einem Patienten, der mit Linezolid oder intravenösem Methylenblau behandelt wird, da ein erhöhtes Risiko für ein Serotonin-Syndrom besteht. Bei einem Patienten, der eine dringendere Behandlung einer psychiatrischen Erkrankung benötigt, sollten andere Interventionen, einschließlich eines Krankenhausaufenthalts, in Betracht gezogen werden [siehe KONTRAINDIKATIONEN ].
In einigen Fällen kann ein Patient, der bereits eine Therapie mit Fluvox 50 mgaminmaleat-Tabletten erhält, eine dringende Behandlung mit Linezolid oder intravenösem Methylenblau benötigen. Wenn keine akzeptablen Alternativen zur Behandlung mit Linezolid oder intravenösem Methylenblau verfügbar sind und der potenzielle Nutzen einer Behandlung mit Linezolid oder intravenösem Methylenblau die Risiken eines Serotonin-Syndroms bei einem bestimmten Patienten überwiegen, sollte Fluvoxaminmaleat sofort abgesetzt und Linezolid oder intravenös verabreicht werden Methylenblau verabreicht werden. Der Patient sollte zwei Wochen lang oder bis 24 Stunden nach der letzten Dosis von Linezolid oder intravenösem Methylenblau, je nachdem, was zuerst eintritt, auf Symptome des Serotonin-Syndroms überwacht werden. Die Therapie mit Fluvox 100-mgamin-Maleat-Tabletten kann 24 Stunden nach der letzten Linezolid- oder intravenösen Gabe von Methylenblau wieder aufgenommen werden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Das Risiko der Verabreichung von Methylenblau auf nicht-intravenösem Weg (z. B. als Tabletten zum Einnehmen oder durch lokale Injektion) oder in intravenösen Dosen von viel weniger als 1 mg/kg mit Fluvox 100 mg/min Maleat-Tabletten ist unklar. Der Arzt sollte sich jedoch der Möglichkeit bewusst sein, dass bei einer solchen Anwendung Symptome des Serotonin-Syndroms auftreten können [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Erhaltung/Fortsetzung Erweiterte Behandlung
Es ist allgemein anerkannt, dass Zwangsstörungen mehrere Monate oder länger einer anhaltenden pharmakologischen Therapie bedürfen. Der Nutzen der Erhaltung von Patienten mit Zwangsstörungen auf Fluvoxaminmaleat-Tabletten nach Erreichen eines Ansprechens für eine durchschnittliche Dauer von etwa 4 Wochen in einer 10-wöchigen einfach verblindeten Phase, während der die Patienten auf die Wirkung titriert wurden, wurde in einer kontrollierten Studie nachgewiesen [siehe Klinische Versuche ].
Der Arzt, der sich für die Anwendung von Fluvoxaminmaleat-Tabletten über einen längeren Zeitraum entscheidet, sollte den langfristigen Nutzen des Arzneimittels für den einzelnen Patienten regelmäßig neu bewerten.
Absetzen der Behandlung mit Fluvoxaminmaleat-Tabletten
Es wurden Symptome im Zusammenhang mit dem Absetzen anderer SSRIs oder SNRIs berichtet [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ]. Patienten sollten auf diese Symptome hin überwacht werden, wenn sie die Behandlung abbrechen. Wann immer möglich, wird eine allmähliche Reduzierung der Dosis anstelle eines abrupten Absetzens empfohlen. Wenn nach einer Verringerung der Dosis oder beim Absetzen der Behandlung unerträgliche Symptome auftreten, kann eine Wiederaufnahme der zuvor verschriebenen Dosis in Betracht gezogen werden. Anschließend kann der Arzt die Dosis weiter verringern, jedoch mit einer allmählicheren Rate.
WIE GELIEFERT
Darreichungsformen und Stärken
Fluvoxamine Maleate Tablets USP sind erhältlich als:
Tabletten 25 mg: weiße, elliptische Filmtabletten ohne Bruchrille (Prägung „1222“ auf einer Seite)
Tabletten 50 mg: gelbe, elliptische Filmtabletten mit Bruchrille (Prägung „1225“ auf einer Seite und Bruchkerbe auf der anderen Seite)
Tabletten 100 mg: mit Bruchkerbe, beige, elliptisch, mit Film überzogen (Prägung „1221“ auf einer Seite und Bruchkerbe auf der anderen Seite)
Lagerung und Handhabung
Fluvox 50mgamine Maleate Tablets USP sind in den folgenden Stärken, Farben, Aufdrucken und Darreichungsformen erhältlich:
ungeritzt, weiß, elliptisch, folienbeschichtet (Prägung „1222“ auf einer Seite)
Flaschen zu 100 ............ NDC 62559-158-01
geritzt, gelb, elliptisch, folienbeschichtet (Prägung „1225“ auf einer Seite und gerillt auf der anderen)
Flaschen zu 100 ............ NDC 62559-159-01
geritzt, beige, elliptisch, folienbeschichtet (Prägung „1221“ auf einer Seite und geritzt auf der anderen)
Flaschen zu 100 ............ NDC 62559-160-01
Außerhalb der Reichweite von Kindern aufbewahren.
Fluvoxaminmaleat-Tabletten sollten vor hoher Feuchtigkeit geschützt und bei 20° bis 25°C (68° bis 77°F) gelagert werden; Exkursionen erlaubt bis 15° bis 30°C (59° bis 86°F) [siehe USP kontrollierte Raumtemperatur ].
In dichten Behältern abgeben.
Hergestellt von: ANI Pharmaceuticals, Inc., Baudette, MN 56623. Überarbeitet: Juli 2021
NEBENWIRKUNGEN
Da klinische Studien unter sehr unterschiedlichen Bedingungen durchgeführt werden, können die in den klinischen Studien zu einem Medikament beobachteten Nebenwirkungsraten nicht direkt mit den Raten in den klinischen Studien zu einem anderen Medikament verglichen werden und spiegeln möglicherweise nicht die in der Praxis beobachteten Raten wider.
Nebenwirkungen, die zum Abbruch der Behandlung führen
Von den 1087 Patienten mit Zwangsstörungen und Depressionen, die in kontrollierten klinischen Studien in Nordamerika mit Fluvoxaminmaleat behandelt wurden, brachen 22 % die Behandlung aufgrund einer Nebenwirkung ab. Nebenwirkungen, die bei mindestens 2 % der mit Fluvoxaminmaleat behandelten Patienten in diesen Studien zum Absetzen führten, waren: Übelkeit (9 %), Schlaflosigkeit (4 %), Somnolenz (4 %), Kopfschmerzen (3 %) und Asthenie, Erbrechen , Nervosität, Erregung und Schwindel (jeweils 2 %).
Inzidenz in kontrollierten Studien
Häufig beobachtete Nebenwirkungen in kontrollierten klinischen Studien
Fluvox 100 mgaminmaleat-Tabletten wurden in 10-wöchigen kontrollierten Kurzzeitstudien zu Zwangsstörungen (N = 320) und Depressionen (N = 1350) untersucht. Im Allgemeinen waren die Nebenwirkungsraten in den beiden Datensätzen sowie in der pädiatrischen OCD-Studie ähnlich. Die am häufigsten beobachteten Nebenwirkungen im Zusammenhang mit der Anwendung von Fluvoxaminmaleat-Tabletten, die wahrscheinlich arzneimittelbedingt waren (Inzidenz von 5 % oder mehr und mindestens doppelt so hoch wie bei Placebo), abgeleitet aus Tabelle 2, waren: Übelkeit, Somnolenz, Schlaflosigkeit, Asthenie, Nervosität, Dyspepsie, abnormale Ejakulation, Schwitzen, Anorexie, Zittern und Erbrechen. In einem Pool von zwei Studien, an denen nur Patienten mit Zwangsstörungen teilnahmen, wurden die folgenden zusätzlichen Reaktionen unter Anwendung der obigen Regel identifiziert: Anorgasmie, verminderte Libido, Mundtrockenheit, Rhinitis, Geschmacksveränderungen und häufiges Wasserlassen. In einer Studie an pädiatrischen Patienten mit Zwangsstörungen wurden die folgenden zusätzlichen Reaktionen anhand der obigen Regel identifiziert: Agitiertheit, Depression, Dysmenorrhoe, Flatulenz, Hyperkinesie und Hautausschlag.
Nebenwirkungen, die bei einer Inzidenz von 1 % auftreten
Tabelle 2 listet Nebenwirkungen auf, die bei Erwachsenen mit einer Häufigkeit von 1 % oder mehr auftraten und häufiger auftraten als in der Placebogruppe, bei Patienten, die in zwei Placebo-kontrollierten Kurzzeitstudien zu Zwangsstörungen (10 Wochen) mit Fluvoxaminmaleat-Tabletten behandelt wurden, und Depressionen Studien (6 Wochen), in denen den Patienten Dosierungen im Bereich von im Allgemeinen 100 bis 300 mg/Tag verabreicht wurden. Diese Tabelle zeigt den Prozentsatz der Patienten in jeder Gruppe, bei denen zu irgendeinem Zeitpunkt während ihrer Behandlung mindestens einmal eine Reaktion auftrat. Gemeldete Nebenwirkungen wurden unter Verwendung einer Standardterminologie des COSTART-basierten Wörterbuchs klassifiziert.
Der verschreibende Arzt sollte sich darüber im Klaren sein, dass diese Zahlen nicht dazu verwendet werden können, das Auftreten von Nebenwirkungen im Rahmen der üblichen medizinischen Praxis vorherzusagen, da sich Patientencharakteristika und andere Faktoren von denen in klinischen Studien unterscheiden können. Ebenso können die angegebenen Häufigkeiten nicht mit Zahlen verglichen werden, die aus anderen klinischen Studien mit unterschiedlichen Behandlungen, Anwendungen und Prüfärzten stammen. Die zitierten Zahlen bieten dem verschreibenden Arzt jedoch eine gewisse Grundlage für die Schätzung des relativen Beitrags von medikamentösen und nichtmedikamentösen Faktoren zur Inzidenzrate von Nebenwirkungen in der untersuchten Population.
TABELLE 2: VORKOMMENSRATEN VON UNTER BEHANDLUNG ENTSTEHENDEN NEBENWIRKUNGEN NACH KÖRPERSYSTEM BEI ERWACHSENEN POPULATIONEN MIT OCD UND DEPRESSIONEN KOMBINIERT1
Nebenwirkungen in Placebo-kontrollierten Studien zu Zwangsstörungen, die sich in der Rate deutlich von den gepoolten Reaktionsraten in Placebo-kontrollierten Studien zu Zwangsstörungen und Depressionen unterscheiden (definiert als mindestens zweifache Differenz).
Die Reaktionen in OCD-Studien mit einer zweifachen Abnahme der Rate im Vergleich zu den Reaktionsraten in OCD- und Depressionsstudien waren Dysphagie und Amblyopie (meistens verschwommenes Sehen). Zusätzlich gab es eine ungefähr 25%ige Abnahme der Übelkeit.
Die Reaktionen in OCD-Studien mit einer zweifachen Erhöhung der Rate im Vergleich zu den Reaktionsraten in OCD- und Depressionsstudien waren: Asthenie, abnormale Ejakulation (meistens verzögerte Ejakulation), Angst, Rhinitis, Anorgasmie (bei Männern), Depression, verminderte Libido, Pharyngitis , Unruhe, Impotenz, Myoklonus/Zucken, Durst, Gewichtsverlust, Beinkrämpfe, Myalgie und Harnverhalt. Diese Reaktionen sind in der Reihenfolge abnehmender Raten in den OCD-Studien aufgeführt.
Andere Nebenwirkungen bei der pädiatrischen OCD-Population
Bei pädiatrischen Patienten (N = 57), die mit Fluvox 100 mgamin Maleat-Tabletten behandelt wurden, war das Gesamtprofil der Nebenwirkungen im Allgemeinen ähnlich wie in Studien mit Erwachsenen, wie in Tabelle 2 gezeigt. Die folgenden Nebenwirkungen, die nicht in Tabelle 2 aufgeführt sind, traten jedoch auf: wurden bei zwei oder mehr pädiatrischen Patienten berichtet und traten unter Fluvoxaminmaleat-Tabletten häufiger auf als unter Placebo: Hustenzunahme, Dysmenorrhoe, Ekchymose, emotionale Labilität, Nasenbluten, Hyperkinesie, manische Reaktion, Hautausschlag, Sinusitis und Gewichtsabnahme.
Männliche und weibliche sexuelle Dysfunktion mit SSRIs
Obwohl Veränderungen des sexuellen Verlangens, der sexuellen Leistung und der sexuellen Befriedigung oft als Manifestationen einer psychiatrischen Störung und mit zunehmendem Alter auftreten, können sie auch eine Folge einer pharmakologischen Behandlung sein. Insbesondere deuten einige Hinweise darauf hin, dass selektive Serotonin-Wiederaufnahmehemmer (SSRIs) solche unerwünschten sexuellen Erfahrungen verursachen können.
Zuverlässige Schätzungen der Häufigkeit und des Schweregrades unerwünschter Erfahrungen im Zusammenhang mit sexuellem Verlangen, sexueller Leistung und Befriedigung sind jedoch schwierig zu erhalten, zum Teil, weil Patienten und Ärzte möglicherweise zögern, darüber zu sprechen. Dementsprechend ist es wahrscheinlich, dass Schätzungen der Häufigkeit von unerwünschten sexuellen Erfahrungen und Verhaltensweisen, die in der Produktkennzeichnung angegeben werden, ihre tatsächliche Häufigkeit unterschätzen.
Tabelle 3 zeigt die Inzidenz sexueller Nebenwirkungen, die von mindestens 2 % der Patienten berichtet wurden, die Fluvox 100-mgamin-Maleat-Tabletten in placebokontrollierten Studien zu Depressionen und Zwangsstörungen einnahmen.
TABELLE 3: PROZENTSATZ DER PATIENTEN, DIE SEXUELLE NEBENWIRKUNGEN IN PLACEBO-KONTROLLIERTEN STUDIEN VON ERWACHSENEN ZU OCD UND DEPRESSION BERICHTEN
Es gibt keine adäquaten und gut kontrollierten Studien, die sexuelle Funktionsstörungen bei einer Behandlung mit Fluvoxamin untersuchen.
Die Behandlung mit Fluvox 50 mgamin wurde mit mehreren Fällen von Priapismus in Verbindung gebracht. In den Fällen mit bekanntem Ausgang erholten sich die Patienten ohne Folgeerscheinungen und nach Absetzen von Fluvox 50 mgamin.
Obwohl es schwierig ist, das genaue Risiko einer sexuellen Dysfunktion im Zusammenhang mit der Anwendung von SSRIs zu kennen, sollten sich Ärzte routinemäßig nach solchen möglichen Nebenwirkungen erkundigen.
Veränderungen der Vitalzeichen
Vergleiche von Fluvoxaminmaleat- und Placebo-Gruppen in getrennten Pools von Kurzzeit-OCD- und Depressionsstudien zu (1) der medianen Veränderung gegenüber dem Ausgangswert bei verschiedenen Vitalparametervariablen und (2) der Inzidenz von Patienten, die die Kriterien für potenziell wichtige Veränderungen gegenüber dem Ausgangswert bei verschiedenen Vitalparametern erfüllen Vorzeichenvariablen zeigten keine wesentlichen Unterschiede zwischen Fluvoxaminmaleat und Placebo.
Änderungen im Labor
Vergleiche von Fluvoxaminmaleat- und Placebo-Gruppen in getrennten Pools von Kurzzeit-OCD- und Depressionsstudien zu (1) medianer Veränderung gegenüber dem Ausgangswert bei verschiedenen Serumchemie-, Hämatologie- und Urinanalysevariablen und zu (2) Inzidenz von Patienten, die die Kriterien für potenziell wichtige Veränderungen erfüllen Von der Basislinie an zeigten verschiedene Serumchemie-, Hämatologie- und Urinanalyse-Variablen keine wesentlichen Unterschiede zwischen Fluvox 100 mgaminmaleat und Placebo.
EKG-Veränderungen
Vergleiche von Fluvox 50 mgamin Maleat und Placebo-Gruppen in separaten Pools von Kurzzeit-OCD- und Depressionsstudien zu (1) mittlerer Veränderung gegenüber dem Ausgangswert bei verschiedenen EKG-Variablen und (2) Inzidenz von Patienten, die die Kriterien für potenziell wichtige Veränderungen gegenüber dem Ausgangswert bei verschiedenen EKGs erfüllen Variablen zeigten keine wesentlichen Unterschiede zwischen Fluvoxaminmaleat und Placebo.
Andere Reaktionen, die während der Premarketing-Evaluierung von Fluvox 100-mgamin-Maleat-Tabletten beobachtet wurden
Während klinischer Premarketing-Studien, die in Nordamerika und Europa durchgeführt wurden, wurden Mehrfachdosen von Fluvoxaminmaleat für insgesamt 2737 Patientenexpositionen bei Patienten mit Zwangsstörungen oder Major Depression verabreicht. Unerwünschte Reaktionen im Zusammenhang mit dieser Exposition wurden von klinischen Forschern unter Verwendung einer beschreibenden Terminologie ihrer eigenen Wahl aufgezeichnet. Folglich ist es nicht möglich, eine aussagekräftige Schätzung des Anteils der Personen zu liefern, bei denen Nebenwirkungen aufgetreten sind, ohne zuerst ähnliche Arten von Nebenwirkungen in eine begrenzte (dh reduzierte) Anzahl von Standardreaktionskategorien einzuteilen.
In den folgenden Tabellen wurde eine Standardterminologie des COSTART-basierten Wörterbuchs verwendet, um gemeldete Nebenwirkungen zu klassifizieren. Wenn der COSTART-Begriff für eine Reaktion so allgemein war, dass er nicht informativ war, wurde er durch einen informativeren Begriff ersetzt. Die dargestellten Häufigkeiten stellen daher den Anteil der 2737 Patienten dar, die Mehrfachdosen von 100 mg Fluvox-Maleat ausgesetzt waren und bei denen während der Behandlung mit Fluvoxamin-Maleat mindestens einmal eine Reaktion der genannten Art auftrat. Alle gemeldeten Reaktionen sind in der nachstehenden Liste enthalten, mit folgenden Ausnahmen: 1) Die bereits in Tabelle 2 aufgeführten Reaktionen, die die Inzidenzraten häufiger unerwünschter Ereignisse in placebokontrollierten klinischen Studien zu Zwangsstörungen und Depressionen tabelliert, sind ausgeschlossen; 2) jene Reaktionen, für die eine medikamentöse Ursache als nicht wahrscheinlich erachtet wurde, werden weggelassen; 3) Reaktionen, für die der COSTART-Begriff zu vage war, um klinisch bedeutsam zu sein, und nicht durch einen aussagekräftigeren Begriff ersetzt werden konnten; und 4) Reaktionen, die nur bei einem Patienten berichtet wurden und als nicht potenziell schwerwiegend eingestuft wurden, sind nicht enthalten. Es ist wichtig zu betonen, dass, obwohl die berichteten Reaktionen während der Behandlung mit Fluvoxaminmaleat auftraten, kein kausaler Zusammenhang mit Fluvoxaminmaleat hergestellt wurde.
Reaktionen werden weiter in Körpersystemkategorien eingeteilt und nach abnehmender Häufigkeit unter Verwendung der folgenden Definitionen aufgezählt: häufige Nebenwirkungen sind definiert als solche, die bei mindestens 1/100 Patienten einmal oder mehrmals auftreten; seltene Nebenwirkungen treten bei 1/100 bis 1/1000 Patienten auf; und seltene Nebenwirkungen treten bei weniger als 1/1000 Patienten auf.
Körper als Ganzes - Häufig: Unwohlsein; Selten: Lichtempfindlichkeitsreaktion und Suizidversuch.
Herz-Kreislauf-System - Häufig: Synkope.
Verdauungstrakt - Selten: Magen-Darm-Blutungen und Meläna; Selten: Hämatemesis.
Hämisches und lymphatisches System - Selten: Anämie und Ekchymose; Selten: Purpura.
Stoffwechsel- und Ernährungssysteme - Häufig: Gewichtszunahme und Gewichtsverlust.
Nervöses System - Häufig: Hyperkinesie, manische Reaktion und Myoklonus; Selten: anormale Träume, Akathisie, Krämpfe, Dyskinesie, Dystonie, Euphorie, extrapyramidales Syndrom und Zuckungen; Selten: Entzugssyndrom.
Atmungssystem - Selten: Nasenbluten. Selten: Hämoptyse und Laryngismus.
Haut - Selten: Urtikaria.
Urogenitalsystem* - Selten: Hämaturie, Menorrhagie und Vaginalblutung; Selten: Hämospermie.
* Basierend auf der Anzahl der Männchen oder Weibchen, je nachdem.
Postmarketing-Berichte
Die folgenden Nebenwirkungen wurden während der Anwendung von Fluvox 100 mgaminmaleat-Tabletten nach der Zulassung festgestellt. Da diese Reaktionen freiwillig aus einer Population unbekannter Größe gemeldet werden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen oder einen kausalen Zusammenhang mit der Arzneimittelexposition herzustellen.
Freiwillige Berichte über Nebenwirkungen bei Patienten, die Fluvox 50 mgaminmaleat-Tabletten einnahmen, die seit der Markteinführung erhalten wurden und in einem unbekannten kausalen Zusammenhang mit der Anwendung von Fluvoxaminmaleat-Tabletten stehen, umfassen: akutes Nierenversagen, Agranulozytose, Amenorrhoe, anaphylaktische Reaktion, Angioödem, aplastische Anämie, bullöser Ausschlag , Henoch-Schoenlein-Purpura, Hepatitis, Ileus, Pankreatitis, Porphyrie, Stevens-Johnson-Syndrom, toxische epidermale Nekrolyse, Vaskulitis und ventrikuläre Tachykardie (einschließlich Torsade de Pointes).
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Mögliche Wechselwirkungen mit Arzneimitteln, die Cytochrom-P450-Isoenzyme hemmen oder von ihnen metabolisiert werden
Mehrere hepatische Cytochrom-P450-Isoenzyme sind an der oxidativen Biotransformation einer großen Anzahl von strukturell unterschiedlichen Arzneimitteln und endogenen Verbindungen beteiligt. Das verfügbare Wissen über die Beziehung zwischen Fluvoxamin und dem Cytochrom-P450-Isoenzymsystem stammt hauptsächlich aus pharmakokinetischen Wechselwirkungsstudien, die an gesunden Freiwilligen durchgeführt wurden, aber einige vorläufige In-vitro-Daten sind ebenfalls verfügbar. Basierend auf einer Feststellung wesentlicher Wechselwirkungen von Fluvox 50 mgamin mit bestimmten dieser Arzneimittel [siehe spätere Teile dieses Abschnitts und auch WARNUNGEN UND VORSICHTSMASSNAHMEN ] und begrenzten In-vitro-Daten für CYP3A4 scheint es, dass Fluvox 100 mgamin mehrere Cytochrom-P450-Isoenzyme hemmt, von denen bekannt ist, dass sie am Metabolismus anderer Arzneimittel beteiligt sind, wie z , Warfarin), CYP3A4 (z. B. Alprazolam) und CYP2C19 (z. B. Omeprazol).
In-vitro-Daten deuten darauf hin, dass Fluvoxamin ein relativ schwacher Inhibitor von CYP2D6 ist.
Etwa 7 % der Normalbevölkerung haben einen genetischen Code, der zu einer verminderten Aktivität von CYP2D6 führt. Solche Personen wurden als „poor metabolizers“ (PM) von Arzneimitteln wie Debrisoquin, Dextromethorphan und trizyklischen Antidepressiva bezeichnet. Während keines der auf Arzneimittelwechselwirkungen untersuchten Arzneimittel die Pharmakokinetik von Fluvox 50 mgamin signifikant beeinflusste, zeigte eine In-vivo-Studie zur Fluvoxamin-Einzeldosis-Pharmakokinetik bei 13 PM-Probanden veränderte pharmakokinetische Eigenschaften im Vergleich zu 16 „extensiven Metabolisierern“ (EM): mittlere Cmax, AUC und die Halbwertszeit waren in der PM-Gruppe im Vergleich zur EM-Gruppe um 52 %, 200 % bzw. 62 % erhöht. Dies deutet darauf hin, dass Fluvox 100 mgamin zumindest teilweise durch CYP2D6 metabolisiert wird. Vorsicht ist geboten bei Patienten, von denen bekannt ist, dass sie eine verringerte CYP2D6-Aktivität aufweisen, und bei Patienten, die gleichzeitig Arzneimittel erhalten, von denen bekannt ist, dass sie dieses Cytochrom-P450-Isoenzym hemmen (z. B. Chinidin).
Der Metabolismus von Fluvoxamin wurde nicht vollständig charakterisiert und die Wirkungen einer starken Hemmung des Isoenzyms Cytochrom P450, wie z. B. der Ketoconazol-Hemmung von CYP3A4, auf den Metabolismus von Fluvox 100 mgamin wurden nicht untersucht.
Eine klinisch signifikante Fluvoxamin-Wechselwirkung ist mit Arzneimitteln möglich, die ein enges therapeutisches Verhältnis haben, wie Pimozid, Warfarin, Theophyllin, bestimmte Benzodiazepine, Omeprazol und Phenytoin. Wenn Fluvox 100 mgaminmaleat-Tabletten zusammen mit einem Arzneimittel verabreicht werden sollen, das durch oxidativen Metabolismus ausgeschieden wird und ein enges therapeutisches Fenster hat, sollten die Plasmaspiegel und/oder pharmakodynamischen Wirkungen des letzteren Arzneimittels engmaschig überwacht werden, zumindest bis Steady-State-Bedingungen erreicht sind erreicht [vgl KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN ].
ZNS-aktive Medikamente
Antipsychotika: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Benzodiazepine: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Alprazolam: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Diazepam: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Lorazepam: Eine Studie mit Mehrfachdosen von Fluvoxaminmaleat (50 mg zweimal täglich) an gesunden männlichen Probanden (N = 12) und einer Einzeldosis Lorazepam (4 mg Einzeldosis) zeigte keine signifikante pharmakokinetische Wechselwirkung. Im Durchschnitt führten sowohl Lorazepam allein als auch Lorazepam mit Fluvoxamin zu erheblichen Abnahmen der kognitiven Funktion; die gleichzeitige Verabreichung von Fluvoxamin und Lorazepam führte jedoch nicht zu größeren mittleren Abnahmen im Vergleich zu Lorazepam allein.
Alkohol: Studien mit Einzeldosen von 40 g Ethanol (orale Gabe in einer Studie und intravenös in der anderen) und mehrfacher Gabe von Fluvox 100 mg Aminmaleat (50 mg zweimal täglich) zeigten keine Wirkung eines der beiden Arzneimittel auf die Pharmakokinetik oder Pharmakodynamik des anderen. Wie bei anderen psychotropen Arzneimitteln sollten die Patienten darauf hingewiesen werden, Alkohol während der Einnahme von Fluvoxaminmaleat-Tabletten zu vermeiden.
Carbamazepin: Erhöhte Carbamazepin-Spiegel und Toxizitätssymptome wurden bei gleichzeitiger Anwendung von Fluvox 100 mgaminmaleat und Carbamazepin berichtet.
Clozapin: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Lithium: Wie bei anderen serotonergen Arzneimitteln kann Lithium die serotonergen Wirkungen von Fluvoxamin verstärken, weshalb die Kombination mit Vorsicht angewendet werden sollte. Krampfanfälle wurden bei gleichzeitiger Anwendung von Fluvox 50 mg Aminmaleat und Lithium berichtet.
Methadon: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Monoaminoxidase-Hemmer: Sehen DOSIERUNG UND ANWENDUNG , KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN .
Pimozid: Sehen KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN .
Ramleteon: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Serotonerge Medikamente: Sehen DOSIERUNG UND ANWENDUNG , KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN .
Tacrin: In einer Studie mit 13 gesunden, männlichen Probanden war eine Einzeldosis von 40 mg Tacrin, die zusätzlich zu Fluvox 50 mgamin 100 mg/Tag im Steady-State verabreicht wurde, mit einem fünf- bzw. achtfachen Anstieg der Cmax und der AUC von Tacrin im Vergleich zu verbunden die Verabreichung von Tacrin allein. Bei fünf Probanden traten nach gleichzeitiger Verabreichung Übelkeit, Erbrechen, Schwitzen und Durchfall auf, was mit den cholinergen Wirkungen von Tacrin übereinstimmt.
Thioridazin: Sehen KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN .
Tizanidin: Sehen KONTRAINDIKATIONEN , WARNUNGEN UND VORSICHTSMASSNAHMEN .
Trizyklische Antidepressiva (TCAs): Bei gleichzeitiger Anwendung von Fluvoxaminmaleat und Amitriptylin, Clomipramin oder Imipramin wurde über signifikant erhöhte Plasma-TCA-Spiegel berichtet. Vorsicht ist geboten bei gleichzeitiger Anwendung von Fluvoxaminmaleat-Tabletten und TCAs; Die TCA-Plasmakonzentrationen müssen möglicherweise überwacht und die TCA-Dosis möglicherweise reduziert werden.
Triptane: Es gab seltene Postmarketing-Berichte über ein Serotonin-Syndrom bei der Anwendung eines SSRI und eines Triptans. Wenn die gleichzeitige Behandlung von Fluvox 50 mgamin mit einem Triptan klinisch gerechtfertigt ist, wird eine sorgfältige Überwachung des Patienten angeraten, insbesondere zu Beginn der Behandlung und bei Dosiserhöhungen [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Sumatriptan: Es gab seltene Postmarketing-Berichte, in denen Patienten mit Schwäche, Hyperreflexie und Koordinationsstörungen nach der Anwendung eines selektiven Serotonin-Wiederaufnahmehemmers (SSRI) und Sumatriptan beschrieben wurden. Wenn eine gleichzeitige Behandlung mit Sumatriptan und einem SSRI (z. B. Fluoxetin, Fluvoxamin, Paroxetin, Sertralin) klinisch gerechtfertigt ist, wird eine angemessene Überwachung des Patienten empfohlen.
Tryptophan: Tryptophan kann die serotonergen Wirkungen von Fluvoxamin verstärken, daher sollte die Kombination mit Vorsicht angewendet werden. Bei gleichzeitiger Anwendung von Fluvoxaminmaleat und Tryptophan wurde über schweres Erbrechen berichtet [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Andere Drogen
Alosetron: Sehen GEGENANZEIGEN , WARNUNGEN UND VORSICHTSMASSNAHMEN , und Packungsbeilage von Lotronex™ (Alosetron).
Digoxin: Die Verabreichung von 100 mg Fluvox 100 mg Aminmaleat täglich über 18 Tage (N = 8) hatte keinen signifikanten Einfluss auf die Pharmakokinetik einer intravenösen Einzeldosis von 1,25 mg Digoxin.
Diltiazem: Bei gleichzeitiger Anwendung von Fluvoxaminmaleat und Diltiazem wurde über Bradykardie berichtet.
Mexiletin: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Propranolol und andere Betablocker: Die gleichzeitige Gabe von 100 mg Fluvoxaminmaleat pro Tag und 160 mg Propranolol pro Tag führte bei gesunden Probanden zu einem mittleren fünffachen Anstieg (Bereich 2 bis 17) der minimalen Propranolol-Plasmakonzentrationen. In dieser Studie gab es eine leichte Potenzierung der durch Propranolol induzierten Verringerung der Herzfrequenz und der Verringerung des diastolischen Belastungsdrucks.
Ein Fall von Bradykardie und Hypotonie und ein zweiter Fall von orthostatischer Hypotonie wurden bei gleichzeitiger Anwendung von Fluvoxaminmaleat und Metoprolol berichtet.
Wenn Propranolol oder Metoprolol zusammen mit Fluvox 50 mgaminmaleat-Tabletten angewendet werden, wird eine Verringerung der Betablocker-Anfangsdosis und eine vorsichtigere Dosistitration empfohlen. Für Fluvoxaminmaleat-Tabletten ist keine Dosisanpassung erforderlich.
Die gleichzeitige Verabreichung von Fluvoxaminmaleat 100 mg pro Tag mit Atenolol 100 mg pro Tag (N = 6) beeinflusste die Plasmakonzentrationen von Atenolol nicht. Im Gegensatz zu Propranolol und Metoprolol, die hepatisch metabolisiert werden, wird Atenolol hauptsächlich renal ausgeschieden.
Theophyllin: Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Warfarin und andere Medikamente, die die Blutstillung beeinträchtigen (NSAIDs, Aspirin usw.): Sehen WARNUNGEN UND VORSICHTSMASSNAHMEN .
Auswirkungen des Rauchens auf den Fluvoxaminstoffwechsel
Raucher hatten im Vergleich zu Nichtrauchern einen um 25 % erhöhten Metabolismus von Fluvox 100 mgamin.
Elektrokrampftherapie (ECT)
Es gibt keine klinischen Studien, die den Nutzen oder die Risiken einer kombinierten Anwendung von ECT und 100 mg Fluvox-Maleat belegen.
Drogenmissbrauch und -abhängigkeit
Kontrollierte Substanz
Fluvoxamine Maleate Tablets sind keine kontrollierte Substanz.
Abhängigkeit
Das Potenzial für Missbrauch, Toleranz und körperliche Abhängigkeit von Fluvox 100 mgaminmaleat wurde in einem nichtmenschlichen Primatenmodell untersucht. Hinweise auf Abhängigkeitsphänomene wurden nicht gefunden. Die Auswirkungen des Absetzens von Fluvoxaminmaleat-Tabletten wurden nicht systematisch in kontrollierten klinischen Studien untersucht. Fluvoxaminmaleat-Tabletten wurden in klinischen Studien nicht systematisch auf Missbrauchspotenzial untersucht, aber es gab in klinischen Studien keinen Hinweis auf Drogensuchverhalten. Es sollte jedoch beachtet werden, dass Patienten mit einem Risiko für Drogenabhängigkeit systematisch von den Prüfstudien mit Fluvox 100 mg Aminmaleat ausgeschlossen wurden. Im Allgemeinen ist es nicht möglich, auf der Grundlage präklinischer oder vor der Markteinführung durchgeführter klinischer Erfahrungen vorherzusagen, inwieweit ein ZNS-aktives Arzneimittel nach seiner Markteinführung missbraucht, abgezweigt und/oder missbraucht wird. Folglich sollten Ärzte Patienten sorgfältig auf Drogenmissbrauch in der Vorgeschichte untersuchen und diese Patienten engmaschig überwachen und sie auf Anzeichen von Fluvoxaminmaleat-Missbrauch oder -Missbrauch (dh Entwicklung einer Toleranz, Erhöhung der Dosis, Suchtverhalten) beobachten.
WARNUNGEN
Eingeschlossen als Teil der VORSICHTSMASSNAHMEN Sektion.
VORSICHTSMASSNAHMEN
Klinische Verschlechterung und Suizidrisiko
Bei Patienten mit schwerer depressiver Störung (MDD), sowohl bei Erwachsenen als auch bei Kindern, kann es zu einer Verschlechterung ihrer Depression und/oder zum Auftreten von Suizidgedanken und -verhalten (Suizidalität) oder zu ungewöhnlichen Verhaltensänderungen kommen, unabhängig davon, ob sie Antidepressiva einnehmen oder nicht Das Risiko kann bestehen bleiben, bis eine signifikante Remission eintritt. Selbstmord ist ein bekanntes Risiko für Depressionen und bestimmte andere psychiatrische Störungen, und diese Störungen selbst sind die stärksten Prädiktoren für Selbstmord. Es besteht jedoch seit langem die Sorge, dass Antidepressiva bei bestimmten Patienten in den frühen Phasen der Behandlung eine Rolle bei der Induktion einer Verschlechterung der Depression und dem Auftreten von Suizidalität spielen könnten. Gepoolte Analysen placebokontrollierter Kurzzeitstudien mit Antidepressiva (SSRIs und andere) zeigten, dass diese Medikamente das Risiko für suizidales Denken und Verhalten (Suizidalität) bei Kindern, Jugendlichen und jungen Erwachsenen (im Alter von 18 bis 24 Jahren) mit schweren depressiven Störungen erhöhen ( MDD) und andere psychiatrische Erkrankungen. Kurzzeitstudien zeigten bei Erwachsenen über 24 Jahren keine Erhöhung des Suizidalitätsrisikos mit Antidepressiva im Vergleich zu Placebo; bei Erwachsenen ab 65 Jahren kam es unter Antidepressiva im Vergleich zu Placebo zu einer Reduktion.
Die gepoolten Analysen placebokontrollierter Studien bei Kindern und Jugendlichen mit MDD, Zwangsstörungen (OCD) oder anderen psychiatrischen Erkrankungen umfassten insgesamt 24 Kurzzeitstudien mit 9 Antidepressiva bei über 4400 Patienten. Die gepoolten Analysen placebokontrollierter Studien bei Erwachsenen mit MDD oder anderen psychiatrischen Erkrankungen umfassten insgesamt 295 Kurzzeitstudien (mediane Dauer von 2 Monaten) mit 11 Antidepressiva bei über 77.000 Patienten. Es gab beträchtliche Schwankungen des Suizidalitätsrisikos zwischen den Medikamenten, aber bei fast allen untersuchten Medikamenten eine Tendenz zu einem Anstieg bei den jüngeren Patienten. Es gab Unterschiede im absoluten Suizidalitätsrisiko zwischen den verschiedenen Indikationen, mit der höchsten Inzidenz bei MDD. Die Risikounterschiede (Medikament vs. Placebo) waren jedoch innerhalb der Altersschichten und über Indikationen hinweg relativ stabil. Diese Risikounterschiede (Arzneimittel-Placebo-Unterschied in der Anzahl der Fälle von Suizidalität pro 1000 behandelten Patienten) sind in Tabelle 1 aufgeführt.
TABELLE 1: DROGEN-PLACEBO-UNTERSCHIEDE BEI DER ANZAHL DER SUIZIDALITÄTSFÄLLE PRO 1000 BEHANDELTEN PATIENTEN
In keiner der pädiatrischen Studien kam es zu Suiziden. Es gab Suizide in den Studien mit Erwachsenen, aber die Anzahl reichte nicht aus, um eine Schlussfolgerung über die Wirkung des Medikaments auf Suizide zu ziehen.
Es ist nicht bekannt, ob sich das Suizidrisiko auf eine längerfristige Anwendung erstreckt, dh über mehrere Monate hinaus. Es gibt jedoch erhebliche Hinweise aus placebokontrollierten Erhaltungsstudien bei Erwachsenen mit Depressionen, dass die Anwendung von Antidepressiva das Wiederauftreten von Depressionen verzögern kann.
Alle Patienten, die mit Antidepressiva aus beliebigen Indikationen behandelt werden, sollten angemessen überwacht und engmaschig auf eine klinische Verschlechterung, Suizidalität und ungewöhnliche Verhaltensänderungen beobachtet werden, insbesondere während der ersten Monate einer medikamentösen Therapie oder bei Dosisänderungen oder -steigerungen oder abnimmt.
Die folgenden Symptome, Angst, Agitiertheit, Panikattacken, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie (psychomotorische Ruhelosigkeit), Hypomanie und Manie, wurden bei erwachsenen und pädiatrischen Patienten berichtet, die ebenfalls mit Antidepressiva wegen schwerer depressiver Störung behandelt wurden wie für andere Indikationen, sowohl psychiatrische als auch nichtpsychiatrische. Obwohl ein kausaler Zusammenhang zwischen dem Auftreten solcher Symptome und entweder der Verschlechterung einer Depression und/oder dem Auftreten suizidaler Impulse nicht hergestellt werden konnte, besteht die Sorge, dass solche Symptome Vorboten einer aufkommenden Suizidalität sein könnten.
Bei Patienten, deren Depression sich anhaltend verschlimmert oder die an Suizidalität oder Symptomen leiden, die Vorboten einer Verschlechterung der Depression oder Suizidalität sein könnten, sollte eine Änderung des therapeutischen Schemas, einschließlich eines möglichen Absetzens der Medikation, in Betracht gezogen werden, insbesondere wenn diese Symptome schwerwiegend und abrupt sind zu Beginn oder waren nicht Teil der Symptome des Patienten.
Wenn die Entscheidung getroffen wurde, die Behandlung abzubrechen, sollte die Medikation so schnell wie möglich ausgeschlichen werden, jedoch unter Berücksichtigung, dass ein abruptes Absetzen mit bestimmten Symptomen und Risiken verbunden sein kann [siehe DOSIERUNG UND ANWENDUNG ].
Familien und Betreuer von Patienten, die wegen einer schweren depressiven Störung oder anderen Indikationen, sowohl psychiatrischen als auch nichtpsychiatrischen, mit Antidepressiva behandelt werden, sollten auf die Notwendigkeit aufmerksam gemacht werden, Patienten auf das Auftreten von Unruhe, Reizbarkeit, ungewöhnlichen Verhaltensänderungen und den anderen oben beschriebenen Symptomen zu überwachen , sowie das Auftreten von Suizidalität, und solche Symptome unverzüglich dem Gesundheitsdienstleister zu melden. Eine solche Überwachung sollte die tägliche Beobachtung durch Familien und Betreuer umfassen. Rezepte für Fluvoxaminmaleat-Tabletten sollten für die kleinste Menge an Tabletten ausgestellt werden, die mit einem guten Patientenmanagement vereinbar ist, um das Risiko einer Überdosierung zu verringern.
Screening von Patienten auf bipolare Störungen
Eine schwere depressive Episode kann die anfängliche Präsentation einer bipolaren Störung sein. Es wird allgemein angenommen (obwohl dies nicht in kontrollierten Studien nachgewiesen wurde), dass die Behandlung einer solchen Episode mit einem Antidepressivum allein die Wahrscheinlichkeit des Auftretens einer gemischten/manischen Episode bei Patienten mit einem Risiko für eine bipolare Störung erhöhen kann. Ob eines der oben beschriebenen Symptome eine solche Konversion darstellt, ist unbekannt. Vor Beginn der Behandlung mit einem Antidepressivum sollten Patienten mit depressiven Symptomen jedoch angemessen untersucht werden, um festzustellen, ob bei ihnen ein Risiko für eine bipolare Störung besteht; Ein solches Screening sollte eine detaillierte psychiatrische Vorgeschichte umfassen, einschließlich einer Familienanamnese von Selbstmord, bipolarer Störung und Depression. Es sollte beachtet werden, dass Fluvox 50mgamine Maleate Tabletten nicht zur Behandlung von bipolarer Depression zugelassen sind.
Serotonin-Syndrom
Die Entwicklung eines potenziell lebensbedrohlichen Serotonin-Syndroms wurde mit SNRIs und SSRIs, einschließlich Fluvoxaminmaleat-Tabletten, allein, aber insbesondere bei gleichzeitiger Anwendung von serotonergen Arzneimitteln (einschließlich Triptanen, trizyklischen Antidepressiva, Fentanyl, Lithium, Tramadol, Tryptophan, Busipiron, Amphetaminen) berichtet und Johanniskraut) und mit Arzneimitteln, die den Serotoninstoffwechsel beeinträchtigen (insbesondere MAO-Hemmer, sowohl zur Behandlung psychiatrischer Erkrankungen als auch andere, wie Linezolid und intravenöses Methylenblau).
Zu den Symptomen des Serotonin-Syndroms können Veränderungen des mentalen Zustands (z. B. Unruhe, Halluzinationen, Delirium und Koma), autonome Instabilität (z. B. Tachykardie, labiler Blutdruck, Schwindel, Diaphorese, Hitzewallungen, Hyperthermie), neuromuskuläre Aberrationen (z. B. Tremor, Steifheit, Myoklonus, Hyperreflexie, Koordinationsstörungen), Krampfanfälle und/oder gastrointestinale Symptome (z. B. Übelkeit, Erbrechen, Durchfall). Die Patienten sollten auf das Auftreten eines Serotonin-Syndroms überwacht werden.
Die gleichzeitige Anwendung von Fluvoxaminmaleat-Tabletten mit MAO-Hemmern zur Behandlung psychiatrischer Erkrankungen ist kontraindiziert. Fluvoxaminmaleat-Tabletten sollten auch nicht bei einem Patienten begonnen werden, der mit MAO-Hemmern wie Linezolid oder intravenösem Methylenblau behandelt wird. Alle Berichte mit Methylenblau, die Informationen zum Verabreichungsweg enthielten, betrafen die intravenöse Verabreichung im Dosisbereich von 1 mg/kg bis 8 mg/kg. Es gab keine Berichte über die Verabreichung von Methylenblau auf anderem Wege (wie z. B. Tabletten zum Einnehmen oder lokale Gewebeinjektion) oder in niedrigeren Dosen. Es kann Umstände geben, in denen es erforderlich ist, bei einem Patienten, der Fluvox 50 mgaminmaleat-Tabletten einnimmt, eine Behandlung mit einem MAO-Hemmer wie Linezolid oder Methylenblau intravenös zu beginnen. Fluvox 50 mgaminmaleat-Tabletten sollten abgesetzt werden, bevor eine Behandlung mit dem MAO-Hemmer begonnen wird [siehe KONTRAINDIKATIONEN , DOSIERUNG UND ANWENDUNG ].
Wenn die gleichzeitige Anwendung von Fluvoxaminmaleat-Tabletten mit anderen serotonergen Arzneimitteln, einschließlich Triptanen, trizyklischen Antidepressiva, Fentanyl, Lithium, Tramadol, Buspiron, Tryptophan, Amphetaminen und Johanniskraut, klinisch gerechtfertigt ist, sollten die Patienten darauf aufmerksam gemacht werden a potenziell erhöhtes Risiko für ein Serotonin-Syndrom, insbesondere zu Behandlungsbeginn und bei Dosiserhöhungen.
Die Behandlung mit Fluvoxaminmaleat-Tabletten und allen begleitenden serotonergen Arzneimitteln sollte sofort abgebrochen werden, wenn die oben genannten Ereignisse auftreten, und eine unterstützende symptomatische Behandlung eingeleitet werden.
Engwinkelglaukom
Die Pupillenerweiterung, die nach der Anwendung vieler Antidepressiva, einschließlich Fluvoxaminmaleat-Tabletten, auftritt, kann bei Patienten mit anatomisch engen Winkeln, die keine offene Iridektomie haben, einen Winkelverschlussanfall auslösen.
Mögliche Thioridazin-Wechselwirkung
Die Wirkung von Fluvoxamin (25 mg zweimal täglich für eine Woche) auf die Steady-State-Konzentrationen von Thioridazin wurde bei 10 männlichen stationären Patienten mit Schizophrenie untersucht. Die Konzentrationen von Thioridazin und seinen zwei aktiven Metaboliten, Mesoridazin und Sulforidazin, stiegen nach gleichzeitiger Verabreichung von Fluvox 100 mgamin um das Dreifache.
Die Verabreichung von Thioridazin führt zu einer dosisabhängigen Verlängerung des QTc-Intervalls, was mit schweren ventrikulären Arrhythmien, wie z. B. Arrhythmien vom Torsades-de-Pointes-Typ, und plötzlichem Herztod einhergeht. Es ist wahrscheinlich, dass diese Erfahrung das Ausmaß des Risikos unterschätzt, das bei höheren Thioridazin-Dosen auftreten kann. Darüber hinaus kann die Wirkung von Fluvox 100 mgamin noch ausgeprägter sein, wenn es in höheren Dosen verabreicht wird. Daher sollten Fluvoxamin und Thioridazin nicht gleichzeitig verabreicht werden [siehe KONTRAINDIKATIONEN ].
Mögliche Tizanidin-Wechselwirkung
Fluvoxamin ist ein starker Inhibitor von CYP1A2 und Tizanidin ist ein CYP1A2-Substrat. Die Wirkung von Fluvox 50 mgamin (100 mg täglich über 4 Tage) auf die Pharmakokinetik und Pharmakodynamik einer Einzeldosis von 4 mg Tizanidin wurde an 10 gesunden männlichen Probanden untersucht. Die Cmax von Tizanidin war ungefähr 12-fach erhöht (Bereich 5-fach bis 32-fach), die Eliminationshalbwertszeit war fast 3-fach verlängert und die AUC war 33-fach erhöht (Bereich 14-fach bis 103-fach). Die mittlere maximale Wirkung auf den Blutdruck war eine Abnahme des systolischen Blutdrucks um 35 mm Hg, eine Abnahme des diastolischen Blutdrucks um 20 mm Hg und eine Abnahme der Herzfrequenz um 4 Schläge/min. Die Schläfrigkeit war signifikant erhöht und die Leistung bei der psychomotorischen Aufgabe war signifikant beeinträchtigt. Fluvoxamin und Tizanidin sollten nicht zusammen angewendet werden [siehe KONTRAINDIKATIONEN ].
Mögliche Interaktion mit Pimozid
Pimozid wird durch das Isoenzym Cytochrom P4503A4 metabolisiert, und es wurde gezeigt, dass Ketoconazol, ein starker Inhibitor von CYP3A4, den Metabolismus dieses Arzneimittels blockiert, was zu erhöhten Plasmakonzentrationen des Ausgangsarzneimittels führt. Eine erhöhte Plasmakonzentration von Pimozid verursacht eine QT-Verlängerung und wurde mit einer ventrikulären Tachykardie vom Torsades-de-Pointes-Typ, manchmal mit tödlichem Ausgang, in Verbindung gebracht. Wie unten angemerkt, wurde eine erhebliche pharmakokinetische Wechselwirkung für Fluvox 100 mgamin in Kombination mit Alprazolam, einem Arzneimittel, das bekanntermaßen durch CYP3A4 metabolisiert wird, beobachtet. Obwohl nicht eindeutig nachgewiesen wurde, dass Fluvox 100 mgamin ein starker CYP3A4-Hemmer ist, ist dies angesichts der erheblichen Wechselwirkung von Fluvox 50 mgamin mit Alprazolam wahrscheinlich. Daher wird empfohlen, Fluvoxamin nicht in Kombination mit Pimozid zu verwenden [siehe KONTRAINDIKATIONEN ].
Mögliche Alosetron-Wechselwirkung
Da Alosetron durch eine Vielzahl hepatischer Enzyme, die CYP-Medikamente metabolisieren, metabolisiert wird, können Induktoren oder Inhibitoren dieser Enzyme die Clearance von Alosetron verändern. Fluvox 50 mgamin ist ein bekannter starker Inhibitor von CYP1A2 und hemmt auch CYP3A4, CYP2C9 und CYP2C19. In einer pharmakokinetischen Studie erhielten 40 gesunde weibliche Probanden Fluvox 100 mgamin in ansteigenden Dosen von 50 mg bis 200 mg pro Tag für 16 Tage, mit gleichzeitiger Verabreichung von Alosetron 1 mg am letzten Tag. Fluvox 50 mgamin erhöhte die mittlere Alosetron-Plasmakonzentration (AUC) etwa um das 6-Fache und verlängerte die Halbwertszeit um etwa das 3-Fache. [Sehen KONTRAINDIKATIONEN und Lotronex™ (Alosetron) Packungsbeilage].
Andere potenziell wichtige Arzneimittelwechselwirkungen
Benzodiazepine
Durch hepatische Oxidation metabolisierte Benzodiazepine (z. B. Alprazolam, Midazolam, Triazolam usw.) sollten mit Vorsicht angewendet werden, da die Clearance dieser Arzneimittel wahrscheinlich durch Fluvoxamin verringert wird. Es ist unwahrscheinlich, dass die Clearance von Benzodiazepinen, die durch Glucuronidierung metabolisiert werden (z. B. Lorazepam, Oxazepam, Temazepam), durch Fluvox 100 mgamin beeinflusst wird.
Alprazolam
Bei gleichzeitiger Gabe von Fluvoxaminmaleat (100 mg qd) und Alprazolam (1 mg qid) bis zum Steady State waren die Plasmakonzentrationen und andere pharmakokinetischen Parameter (AUC, Cmax, T½) von Alprazolam etwa doppelt so hoch wie bei alleiniger Gabe von Alprazolam; Die orale Clearance war um etwa 50 % reduziert. Die erhöhten Alprazolam-Plasmakonzentrationen führten zu einer verminderten psychomotorischen Leistungsfähigkeit und Gedächtnisleistung. Diese Wechselwirkung, die bei höheren Dosen von Fluvoxamin nicht untersucht wurde, kann ausgeprägter sein, wenn eine Tagesdosis von 300 mg gleichzeitig verabreicht wird, insbesondere da Fluvox 50 mgamin über den Dosierungsbereich von 100-300 mg eine nichtlineare Pharmakokinetik aufweist. Wenn Alprazolam zusammen mit Fluvox 50 mg Aminmaleat-Tabletten angewendet wird, sollte die Anfangsdosis von Alprazolam mindestens halbiert und eine Titration auf die niedrigste wirksame Dosis empfohlen werden. Für Fluvox 100mgamine Maleate Tablets ist keine Dosisanpassung erforderlich.
Diazepam
Die gleichzeitige Anwendung von Fluvoxaminmaleat-Tabletten und Diazepam ist im Allgemeinen nicht ratsam. Da Fluvoxamin die Clearance sowohl von Diazepam als auch seines aktiven Metaboliten Ndesmethyldiazepam reduziert, besteht eine hohe Wahrscheinlichkeit einer erheblichen Akkumulation beider Spezies während einer chronischen gleichzeitigen Verabreichung.
Belege für die Schlussfolgerung, dass die gleichzeitige Verabreichung von Fluvoxamin und Diazepam nicht ratsam ist, stammen aus einer Studie, in der gesunden Freiwilligen, die täglich 150 mg Fluvox 50 mgamin einnahmen, eine orale Einzeldosis von 10 mg Diazepam verabreicht wurde. Bei diesen Probanden (N = 8) war die Clearance von Diazepam um 65 % reduziert und die von N-Desmethyldiazepam auf ein Niveau, das zu niedrig war, um im Laufe der 2-wöchigen Studie gemessen zu werden.
Es ist wahrscheinlich, dass diese Erfahrung das Ausmaß der Akkumulation, das bei wiederholter Verabreichung von Diazepam auftreten kann, deutlich unterschätzt. Darüber hinaus kann, wie bei Alprazolam festgestellt, die Wirkung von Fluvox 50 mgamin sogar noch ausgeprägter sein, wenn es in höheren Dosen verabreicht wird.
Dementsprechend sollten Diazepam und Fluvoxamin normalerweise nicht gleichzeitig verabreicht werden.
Clozapin
Erhöhte Serumspiegel von Clozapin wurden bei Patienten berichtet, die Fluvox 100 mgaminmaleat und Clozapin einnahmen. Da Clozapin-bedingte Krampfanfälle und orthostatische Hypotonie dosisabhängig zu sein scheinen, kann das Risiko dieser Nebenwirkungen bei gleichzeitiger Anwendung von Fluvoxamin und Clozapin höher sein. Patienten sollten engmaschig überwacht werden, wenn Fluvoxaminmaleat und Clozapin gleichzeitig angewendet werden.

Methadon
Signifikant erhöhte Methadon-Verhältnisse (Plasmaspiegel:Dosis) wurden berichtet, wenn Fluvox 50 mgaminmaleat Patienten verabreicht wurde, die eine Methadon-Erhaltungstherapie erhielten, wobei bei einem Patienten Symptome einer Opioidvergiftung auftraten. Bei einem anderen Patienten wurden nach Absetzen von Fluvoxaminmaleat Opioid-Entzugserscheinungen berichtet.
Mexiletin
Die Wirkung von Fluvoxamin im Steady-State (50 mg zweimal täglich für 7 Tage) auf die Pharmakokinetik einer Einzeldosis von Mexiletin (200 mg) wurde bei 6 gesunden japanischen Männern untersucht. Die Clearance von Mexiletin war nach gleichzeitiger Verabreichung mit Fluvox 100 mgamin im Vergleich zu Mexiletin allein um 38 % verringert. Bei gleichzeitiger Anwendung von Fluvoxamin und Mexiletin sollten die Mexiletinspiegel im Serum überwacht werden.
Ramleteon
Wenn Fluvox 50 mgamin 100 mg zweimal täglich 3 Tage lang vor der gleichzeitigen Gabe einer Einzeldosis von Ramelteon 16 mg und Fluvoxamin verabreicht wurde, stieg die AUC von Ramelteon etwa um das 190-Fache und die Cmax um etwa das 70-Fache im Vergleich zu Ramelteon allein. Ramelteon sollte nicht in Kombination mit Fluvoxamin angewendet werden.
Theophyllin
Die Wirkung von Steady-State-Fluvox 50 mgamin (50 mg zweimal täglich) auf die Pharmakokinetik einer Einzeldosis von Theophyllin (375 mg als 442 mg Aminophyllin) wurde bei 12 gesunden, männlichen, nicht rauchenden Probanden untersucht. Die Clearance von Theophyllin war etwa um das Dreifache verringert. Wenn Theophyllin zusammen mit Fluvoxaminmaleat verabreicht wird, sollte daher die Dosis auf ein Drittel der üblichen täglichen Erhaltungsdosis reduziert und die Plasmakonzentrationen von Theophyllin überwacht werden. Für Fluvox 100mgamine Maleate Tablets ist keine Dosisanpassung erforderlich.
Warfarin und andere Medikamente, die die Blutstillung beeinträchtigen (NSAIDs, Aspirin usw.)
Die Serotoninfreisetzung durch Blutplättchen spielt eine wichtige Rolle bei der Hämostase. Epidemiologische Studien zum Fall-Kontroll- und Kohorten-Design haben einen Zusammenhang zwischen der Einnahme von Psychopharmaka, die die Serotonin-Wiederaufnahme beeinträchtigen, und dem Auftreten von Blutungen im oberen Gastrointestinaltrakt gezeigt. Diese Studien haben auch gezeigt, dass die gleichzeitige Anwendung eines NSAID oder Aspirin dieses Blutungsrisiko potenzieren kann. Daher sollten Patienten vor der gleichzeitigen Anwendung solcher Arzneimittel mit Fluvoxamin gewarnt werden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Warfarin
Wenn Fluvox 50 mgaminmaleat (50 mg dreimal täglich) zwei Wochen lang gleichzeitig mit Warfarin verabreicht wurde, stiegen die Plasmakonzentrationen von Warfarin um 98 % und die Prothrombinzeiten verlängerten sich. Daher sollte bei Patienten, die orale Antikoagulanzien und Fluvoxaminmaleat-Tabletten erhalten, die Prothrombinzeit überwacht und die Dosis des Antikoagulans entsprechend angepasst werden. Für Fluvoxaminmaleat-Tabletten ist keine Dosisanpassung erforderlich.
Absetzen der Behandlung mit Fluvox 100mgaminmaleat-Tabletten
Während der Vermarktung von Fluvoxaminmaleat-Tabletten und anderen SSRIs und SNRIs (Serotonin- und Noradrenalin-Wiederaufnahmehemmer) gab es spontane Berichte über Nebenwirkungen, die nach Absetzen dieser Arzneimittel auftraten, insbesondere bei abruptem Absetzen, einschließlich der folgenden: dysphorische Stimmung, Reizbarkeit, Unruhe, Schwindel , sensorische Störungen (z. B. Parästhesien, wie Elektroschocks), Angst, Verwirrtheit, Kopfschmerzen, Lethargie, emotionale Labilität, Schlaflosigkeit und Hypomanie. Obwohl diese Ereignisse im Allgemeinen selbstlimitierend sind, gab es Berichte über schwerwiegende Absetzsymptome.
Patienten sollten auf diese Symptome überwacht werden, wenn sie die Behandlung mit Fluvox 50 mgaminmaleat-Tabletten abbrechen. Wann immer möglich, wird eine allmähliche Reduzierung der Dosis anstelle eines abrupten Absetzens empfohlen. Wenn nach einer Verringerung der Dosis oder beim Absetzen der Behandlung unerträgliche Symptome auftreten, kann eine Wiederaufnahme der zuvor verschriebenen Dosis in Betracht gezogen werden. Anschließend kann der Arzt die Dosis weiter verringern, jedoch langsamer [siehe DOSIERUNG UND ANWENDUNG ].
Abnorme Blutung
SSRIs und SNRIs, einschließlich Fluvoxaminmaleat-Tabletten, können das Risiko von Blutungsereignissen erhöhen. Die gleichzeitige Anwendung von Aspirin, nichtsteroidalen Antirheumatika, Warfarin und anderen Antikoagulanzien kann dieses Risiko erhöhen. Fallberichte und epidemiologische Studien (Fall-Kontroll- und Kohortendesign) haben einen Zusammenhang zwischen der Einnahme von Arzneimitteln, die die Serotonin-Wiederaufnahme beeinträchtigen, und dem Auftreten von gastrointestinalen Blutungen gezeigt. Blutungsereignisse im Zusammenhang mit SSRIs und SNRIs reichten von Ekchymosen, Hämatomen, Epistaxis und Petechien bis hin zu lebensbedrohlichen Blutungen.
Patienten sollten vor dem Blutungsrisiko gewarnt werden, das mit der gleichzeitigen Anwendung von Fluvox 100-mgamin-Maleat-Tabletten und NSAIDs, Aspirin oder anderen Arzneimitteln, die die Blutgerinnung beeinflussen, verbunden ist [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Aktivierung von Manie/Hypomanie
In Studien vor der Markteinführung mit primär depressiven Patienten trat bei etwa 1 % der mit Fluvoxamin behandelten Patienten Hypomanie oder Manie auf. In einer zehnwöchigen pädiatrischen OCD-Studie traten bei 2 von 57 Patienten (4 %), die mit Fluvoxamin behandelt wurden, manische Reaktionen auf, verglichen mit keinem der 63 Placebo-Patienten. Bei einem kleinen Teil der Patienten mit schweren affektiven Störungen, die mit anderen handelsüblichen Antidepressiva behandelt wurden, wurde auch über die Aktivierung von Manie/Hypomanie berichtet. Wie alle Antidepressiva sollten Fluvoxaminmaleat-Tabletten bei Patienten mit Manie in der Anamnese mit Vorsicht angewendet werden.
Krampfanfälle
In Studien vor der Markteinführung wurden bei 0,2 % der mit Fluvoxamin behandelten Patienten Krampfanfälle berichtet. Vorsicht ist geboten, wenn das Medikament Patienten mit Krampfanfällen in der Vorgeschichte verabreicht wird. Fluvox 100 mgamin sollte bei Patienten mit instabiler Epilepsie vermieden werden und Patienten mit kontrollierter Epilepsie sollten sorgfältig überwacht werden. Die Behandlung mit Fluvoxamin sollte abgebrochen werden, wenn Krampfanfälle auftreten oder die Anfallshäufigkeit zunimmt.
Hyponatriämie
Hyponatriämie kann als Folge einer Behandlung mit SSRIs und SNRIs, einschließlich Fluvoxaminmaleat-Tabletten, auftreten. In vielen Fällen scheint diese Hyponatriämie das Ergebnis des Syndroms des inadäquaten antidiuretischen Hormons (SIADH) zu sein. Es wurden Fälle mit Serumnatriumwerten unter 110 mmol/l berichtet. Ältere Patienten können unter SSRIs und SNRIs einem höheren Risiko ausgesetzt sein, eine Hyponatriämie zu entwickeln [siehe Verwendung in bestimmten Bevölkerungsgruppen ]. Auch Patienten, die Diuretika einnehmen oder anderweitig an Volumenmangel leiden, können einem höheren Risiko ausgesetzt sein. Bei Patienten mit symptomatischer Hyponatriämie sollte ein Absetzen von Fluvox 100 mgaminmaleat-Tabletten in Betracht gezogen und eine angemessene medizinische Intervention eingeleitet werden.
Anzeichen und Symptome einer Hyponatriämie sind Kopfschmerzen, Konzentrationsschwierigkeiten, Gedächtnisstörungen, Verwirrtheit, Schwäche und Unsicherheit, die zu Stürzen führen können. Anzeichen und Symptome im Zusammenhang mit schwereren und/oder akuten Fällen waren Halluzinationen, Synkopen, Krampfanfälle, Koma, Atemstillstand und Tod.
Anwendung bei Patienten mit Begleiterkrankungen
Engmaschig überwachte klinische Erfahrungen mit Fluvox 50-mgamin-Maleat-Tabletten bei Patienten mit gleichzeitiger systemischer Erkrankung sind begrenzt. Bei der Verabreichung von Fluvoxaminmaleat-Tabletten an Patienten mit Krankheiten oder Zuständen, die die hämodynamischen Reaktionen oder den Stoffwechsel beeinflussen könnten, ist Vorsicht geboten.
Fluvoxaminmaleat-Tabletten wurden bei Patienten mit kürzlich aufgetretenem Myokardinfarkt oder instabiler Herzerkrankung nicht untersucht oder in nennenswertem Umfang angewendet. Patienten mit diesen Diagnosen wurden während der Premarketing-Tests des Produkts systematisch von vielen klinischen Studien ausgeschlossen. Die Auswertung der Elektrokardiogramme von Patienten mit Depressionen oder Zwangsstörungen, die an Studien vor der Markteinführung teilnahmen, ergab keine Unterschiede zwischen Fluvox 100 mgamin und Placebo in Bezug auf das Auftreten klinisch bedeutsamer EKG-Veränderungen.
Patienten mit eingeschränkter Leberfunktion
Bei Patienten mit Leberfunktionsstörungen war die Clearance von Fluvox 50 mg um etwa 30 % verringert. Patienten mit Leberfunktionsstörungen sollten mit einer niedrigen Dosis von Fluvoxaminmaleat-Tabletten beginnen und diese unter sorgfältiger Überwachung langsam steigern.
Labortests
Es werden keine spezifischen Labortests empfohlen.
Sexuelle Funktionsstörung
Die Anwendung von SSRIs, einschließlich Fluvoxaminmaleat-Tabletten, kann Symptome einer sexuellen Dysfunktion hervorrufen [siehe NEBENWIRKUNGEN 4)]. Bei männlichen Patienten kann die Anwendung von SSRI zu Ejakulationsverzögerung oder -versagen, verminderter Libido und erektiler Dysfunktion führen. Bei weiblichen Patienten kann die Anwendung von SSRI zu einer verminderten Libido und einem verzögerten oder ausbleibenden Orgasmus führen.
Es ist wichtig, dass sich der verschreibende Arzt vor Beginn der Behandlung mit Fluvoxaminmaleat-Tabletten nach der Sexualfunktion erkundigt und sich während der Behandlung speziell nach Veränderungen der Sexualfunktion erkundigt, da die Sexualfunktion möglicherweise nicht spontan gemeldet wird. Bei der Beurteilung von Veränderungen der Sexualfunktion ist es wichtig, eine detaillierte Anamnese (einschließlich des Zeitpunkts des Auftretens der Symptome) zu erheben, da sexuelle Symptome andere Ursachen haben können, einschließlich der zugrunde liegenden psychiatrischen Störung. Besprechen Sie mögliche Behandlungsstrategien, um Patienten dabei zu unterstützen, fundierte Entscheidungen über die Behandlung zu treffen.
Informationen zur Patientenberatung
Weisen Sie den Patienten an, die von der FDA zugelassene Patientenkennzeichnung ( Leitfaden für Medikamente ).
Verschreibende Ärzte oder andere Angehörige der Gesundheitsberufe sollten Patienten, ihre Familien und ihre Betreuer über die Vorteile und Risiken im Zusammenhang mit der Behandlung mit Fluvoxaminmaleat-Tabletten informieren und sie bezüglich der angemessenen Anwendung beraten. Für Fluvox 100-mgamin-Maleat-Tabletten ist ein Medikationsleitfaden für Patienten über „Antidepressiva, Depressionen und andere schwere psychische Erkrankungen sowie Selbstmordgedanken oder -handlungen“ verfügbar. Der verschreibende Arzt oder medizinisches Fachpersonal sollte Patienten, ihre Familien und ihre Betreuer anweisen, den Medikationsleitfaden zu lesen, und ihnen helfen, seinen Inhalt zu verstehen. Den Patienten sollte Gelegenheit gegeben werden, den Inhalt des Medikationsleitfadens zu diskutieren und Antworten auf eventuelle Fragen zu erhalten. Der vollständige Text des Medikationsleitfadens ist am Ende dieses Dokuments abgedruckt.
Die Patienten sollten auf die folgenden Probleme hingewiesen und gebeten werden, ihren verschreibenden Arzt zu informieren, wenn diese während der Einnahme von Fluvox 100-mgamin-Maleat-Tabletten auftreten.
Klinische Verschlechterung und Suizidrisiko
Patienten, ihre Familien und ihre Betreuer sollten ermutigt werden, auf das Auftreten von Angstzuständen, Unruhe, Panikattacken, Schlaflosigkeit, Reizbarkeit, Feindseligkeit, Aggressivität, Impulsivität, Akathisie (psychomotorische Unruhe), Hypomanie, Manie und anderen ungewöhnlichen Verhaltensänderungen zu achten , Verschlechterung von Depressionen und Suizidgedanken, besonders früh während der Behandlung mit Antidepressiva und wenn die Dosis nach oben oder unten angepasst wird. Familien und Betreuer von Patienten sollten angewiesen werden, täglich auf das Auftreten solcher Symptome zu achten, da Änderungen abrupt sein können. Solche Symptome sollten dem verschreibenden Arzt oder medizinischen Fachpersonal des Patienten gemeldet werden, insbesondere wenn sie schwerwiegend sind, abrupt einsetzen oder nicht zu den Symptomen des Patienten gehörten. Symptome wie diese können mit einem erhöhten Risiko für Suizidgedanken und -verhalten verbunden sein und weisen auf die Notwendigkeit einer sehr engmaschigen Überwachung und möglicherweise einer Änderung der Medikation hin [siehe Eingerahmte Warnung , WARNUNGEN UND VORSICHTSMASSNAHMEN ]
Serotonin-Syndrom
Patienten sollten vor dem Risiko eines Serotonin-Syndroms gewarnt werden, insbesondere bei gleichzeitiger Anwendung von Fluvoxamin mit anderen serotonergen Mitteln (einschließlich Triptanen, trizyklischen Antidepressiva, Fentanyl, Lithium, Tramadol, Tryptophan, Buspiron, Amphetaminen und Johanniskraut). [sehen WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Engwinkelglaukom
Die Patienten sollten darauf hingewiesen werden, dass die Einnahme von Fluvoxaminmaleat-Tabletten eine leichte Pupillenerweiterung verursachen kann, die bei empfindlichen Personen zu einer Episode eines Engwinkelglaukoms führen kann. Ein vorbestehendes Glaukom ist fast immer ein Offenwinkelglaukom, da ein Winkelblockglaukom, wenn es diagnostiziert wird, definitiv mit einer Iridektomie behandelt werden kann. Das Offenwinkelglaukom ist kein Risikofaktor für das Engwinkelglaukom. Patienten möchten möglicherweise untersucht werden, um festzustellen, ob sie für Winkelverschluss anfällig sind, und sich einem prophylaktischen Verfahren (z. B. Iridektomie) unterziehen, wenn sie anfällig sind [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Beeinträchtigung der kognitiven oder motorischen Leistung
Da jedes psychoaktive Medikament das Urteilsvermögen, das Denken oder die motorischen Fähigkeiten beeinträchtigen kann, sollten die Patienten vor dem Bedienen gefährlicher Maschinen, einschließlich Autos, gewarnt werden, bis sie sicher sind, dass die Therapie mit Fluvox 100 mgaminmaleat-Tabletten ihre Fähigkeit zur Teilnahme an solchen Aktivitäten nicht beeinträchtigt.
Schwangerschaft
Stillzeit
Raten Sie stillenden Frauen, die Fluvox 100 mgaminmaleat-Tabletten anwenden, Säuglinge auf Durchfall, Erbrechen, Schlafstörungen und Unruhe zu überwachen und einen Arzt aufzusuchen, wenn sie diese Anzeichen bemerken [siehe Verwendung in bestimmten Bevölkerungsgruppen ].
Begleitmedikation
Patienten sollten angewiesen werden, ihren Arzt zu informieren, wenn sie verschreibungspflichtige oder rezeptfreie Arzneimittel einnehmen oder deren Einnahme beabsichtigen, da die Möglichkeit klinisch bedeutsamer Wechselwirkungen mit Fluvox 50-mgamin-Maleat-Tabletten besteht.
Patienten sollten vor der gleichzeitigen Anwendung von Fluvoxamin und NSAIDs, Aspirin oder anderen Arzneimitteln, die die Blutgerinnung beeinflussen, gewarnt werden, da die kombinierte Anwendung von Psychopharmaka, die die Serotonin-Wiederaufnahme beeinträchtigen, und diesen Arzneimitteln mit einem erhöhten Blutungsrisiko in Verbindung gebracht wurde [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Aufgrund des potenziell erhöhten Risikos schwerwiegender Nebenwirkungen einschließlich starker Blutdrucksenkung und Sedierung bei gleichzeitiger Anwendung von Fluvoxamin und Tizanidin sollte Fluvox 50 mgamin nicht zusammen mit Tizanidin angewendet werden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Aufgrund des potenziell erhöhten Risikos schwerwiegender Nebenwirkungen bei gleichzeitiger Anwendung von Fluvoxamin und Alosetron sollte Fluvox 50 mgamin nicht zusammen mit LotronexTM (Alosetron) angewendet werden [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Sexuelle Funktionsstörung
Weisen Sie die Patienten darauf hin, dass die Anwendung von Fluvox 50-mgamin-Maleat-Tabletten sowohl bei männlichen als auch bei weiblichen Patienten Symptome einer sexuellen Dysfunktion hervorrufen kann. Informieren Sie die Patienten darüber, dass sie alle Veränderungen der Sexualfunktion und potenzielle Behandlungsstrategien mit ihrem Arzt besprechen sollten [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Alkohol
Wie bei anderen psychotropen Arzneimitteln sollten die Patienten darauf hingewiesen werden, Alkohol während der Einnahme von Fluvox 50 mgaminmaleat-Tabletten zu vermeiden.
Allergische Reaktionen
Patienten sollten angewiesen werden, ihren Arzt zu benachrichtigen, wenn sie während der Therapie mit Fluvoxaminmaleat-Tabletten Hautausschlag, Nesselsucht oder ein damit zusammenhängendes allergisches Phänomen entwickeln.
Alle aufgeführten Markennamen sind eingetragene Warenzeichen ihrer jeweiligen Eigentümer und keine Warenzeichen von ANI Pharmaceuticals, Inc.
Nichtklinische Toxikologie
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Karzinogenese
Es gab keine Hinweise auf Karzinogenität bei Ratten, die 30 Monate lang oral mit Fluvoxaminmaleat behandelt wurden, oder bei Hamstern, die 20 (Weibchen) oder 26 (Männer) Monate oral mit Fluvox 50 mgaminmaleat behandelt wurden. Die Tagesdosen in den hohen Dosisgruppen dieser Studien wurden im Verlauf der Studie von minimal 160 mg/kg auf maximal 240 mg/kg bei Ratten und von minimal 135 mg/kg auf maximal erhöht von 240 mg/kg bei Hamstern. Die Höchstdosis von 240 mg/kg entspricht ungefähr dem 5- bzw. 6-Fachen (bei Hamstern und Ratten) der MRHD, die Kindern auf mg/m²-Basis verabreicht wird.
Mutagenese
In einem Maus-Mikrokerntest, einem In-vitro-Chromosomenaberrationstest oder dem mikrobiellen Mutagentest von Ames mit oder ohne metabolische Aktivierung wurden keine Hinweise auf ein genotoxisches Potenzial beobachtet.
Beeinträchtigung der Fruchtbarkeit
In einer Studie, in der männlichen und weiblichen Ratten vor und während der Paarung und Trächtigkeit Fluvox 100 mgamin (60, 120 oder 240 mg/kg) verabreicht wurde, wurde die Fertilität bei oralen Dosen von 120 mg/kg (dem 3-fachen der verabreichten MRHD) beeinträchtigt Jugendliche auf einer mg/m²-Basis) oder höher, was sich in einer erhöhten Latenz bis zur Paarung, einer verringerten Spermienzahl, einem verringerten Nebenhodengewicht und einer verringerten Schwangerschaftsrate zeigt. Darüber hinaus war die Zahl der Implantationen und Embryonen bei der höchsten Dosis (6-fache MRHD bei Jugendlichen auf mg/m²-Basis) verringert. Die No-Effect-Dosis für die Beeinträchtigung der Fertilität betrug 60 mg/kg (das 1,6-fache der MRHD, die Jugendlichen auf mg/m²-Basis verabreicht wird).
Verwendung in bestimmten Bevölkerungsgruppen
Schwangerschaft
Schwangerschafts-Expositionsregister
Es gibt ein Schwangerschafts-Expositionsregister, das die Schwangerschaftsausgänge bei Frauen überwacht, die während der Schwangerschaft Antidepressiva ausgesetzt waren. Gesundheitsdienstleister werden ermutigt, Patienten zu registrieren, indem sie das National Pregnancy Registry for Antidepressants unter 1-844-405-6185 anrufen oder online unter https://womensmentalhealth.org/clinical-and-research-programs/pregnancyregistry/antidepressants/ besuchen.
Zusammenfassung der Risiken
Langjährige Erfahrungen mit Fluvox 100 mgamin bei Schwangeren über Jahrzehnte hinweg, basierend auf veröffentlichten Beobachtungsstudien, haben kein eindeutiges arzneimittelbedingtes Risiko für schwere Geburtsfehler oder Fehlgeburten ergeben (siehe Daten ). Es gibt Risiken im Zusammenhang mit einer unbehandelten Depression in der Schwangerschaft und Risiken einer persistierenden pulmonalen Hypertonie des Neugeborenen (PPHN) und einer schlechten neonatalen Anpassung bei Exposition gegenüber selektiven Serotonin-Wiederaufnahmehemmern (SSRIs), einschließlich Fluvoxamin, während der Schwangerschaft (siehe Klinische Überlegungen ).
Wenn trächtige Ratten während der Organogenese oral mit Fluvoxamin behandelt wurden, wurde bei Dosierungen, die das ≥ 3-Fache der maximal empfohlenen Humandosis (MRHD) von 300 mg/Tag erhielten, ein vermehrter embryofötaler Tod und eine erhöhte Inzidenz fötaler Augenanomalien (gefaltete Netzhäute) beobachtet Jugendliche auf mg/m²-Basis. Darüber hinaus wurde bei einer Dosis, die das 6-Fache der MRHD betrug, die Jugendlichen auf mg/m²-Basis verabreicht wurde, ein verringertes fötales Körpergewicht beobachtet. Bei Kaninchen, die mit Fluvoxamin während der Organogenese bis zu einer Dosis behandelt wurden, die dem Zweifachen der MRHD-Dosis entsprach, die Jugendlichen auf mg/m²-Basis verabreicht wurde, traten keine nachteiligen Auswirkungen auf die Entwicklung auf. Wenn Fluvox 50 mgamin Ratten während der Trächtigkeit und Laktation oral verabreicht wurde, wurde eine erhöhte Jungtiersterblichkeit bei der Geburt bei einer Dosis beobachtet, die das Zweifache der MRHD betrug, die Heranwachsenden auf mg/m²-Basis verabreicht wurde. Darüber hinaus wurde bei Dosen, die dem ≥ 0,13-fachen der MRHD bei Jugendlichen entsprachen, eine Abnahme des Körpergewichts und der Überlebensrate der Jungtiere beobachtet (siehe Daten ).
Das geschätzte Hintergrundrisiko schwerer Geburtsfehler und Fehlgeburten für die angegebene Population ist unbekannt. Alle Schwangerschaften haben ein Hintergrundrisiko für Geburtsfehler, Verlust oder andere nachteilige Folgen. In der US-Allgemeinbevölkerung liegt das geschätzte Hintergrundrisiko für schwere Geburtsfehler und Fehlgeburten bei klinisch anerkannten Schwangerschaften bei 2 bis 4 % bzw. 15 bis 20 %.
Klinische Überlegungen
Krankheitsbedingtes mütterliches und/oder embryonale/fetales Risiko
Frauen, die Antidepressiva während der Schwangerschaft absetzen, erleiden mit größerer Wahrscheinlichkeit einen Rückfall einer schweren Depression als Frauen, die Antidepressiva weiter einnehmen. Dieses Ergebnis stammt aus einer prospektiven Längsschnittstudie, die 201 schwangere Frauen mit einer Vorgeschichte einer schweren depressiven Störung, die euthymisch waren und zu Beginn der Schwangerschaft Antidepressiva einnahmen, beobachtete. Berücksichtigen Sie das Risiko einer unbehandelten Depression, wenn Sie die Behandlung mit Antidepressiva während der Schwangerschaft und nach der Geburt abbrechen oder ändern.
Fetale/neonatale Nebenwirkungen
Neugeborene, die gegen Ende des dritten Trimesters Fluvoxaminmaleat-Tabletten und anderen SSRIs oder SNRIs ausgesetzt waren, entwickelten Komplikationen, die einen verlängerten Krankenhausaufenthalt, Atemunterstützung und Sondenernährung erforderten. Solche Komplikationen können unmittelbar nach der Geburt auftreten. Zu den berichteten klinischen Befunden gehörten Atemnot, Zyanose, Apnoe, Krampfanfälle, Temperaturinstabilität, Schwierigkeiten beim Füttern, Erbrechen, Hypoglykämie, Hypotonie, Hypertonie, Hyperreflexie, Zittern, Nervosität, Reizbarkeit und ständiges Weinen. Diese Merkmale stimmen entweder mit einer direkten toxischen Wirkung von SSRIs und SNRIs oder möglicherweise mit einem Arzneimittelabsetzsyndrom überein. Es sollte beachtet werden, dass das klinische Bild in einigen Fällen mit dem Serotonin-Syndrom übereinstimmt [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Daten
Menschliche Daten
Die Exposition gegenüber SSRIs während der späten Schwangerschaft kann ein erhöhtes Risiko für eine persistierende pulmonale Hypertonie des Neugeborenen (PPHN) haben. PPHN tritt bei 1–2 von 1000 Lebendgeburten in der Allgemeinbevölkerung auf und ist mit einer erheblichen neonatalen Morbidität und Mortalität verbunden.
Tierdaten
Wenn trächtige Ratten orale Dosen von Fluvox 100 mgamin (60, 120 oder 240 mg/kg) während der gesamten Organogenese erhielten, wurde eine Entwicklungstoxizität in Form von erhöhtem embryofötalem Tod und erhöhtem Auftreten von fötalen Augenanomalien (gefaltete Netzhaut) beobachtet Dosen von 120 mg/kg oder mehr (das Dreifache der MRHD von 300 mg/Tag, verabreicht an Jugendliche auf mg/m²-Basis). Bei der hohen Dosis von 240 mg/kg/Tag (6-fache der MRHD, die Jugendlichen auf mg/m²-Basis verabreicht wird) wurde ein vermindertes fötales Körpergewicht beobachtet. Die No-Effect-Dosis für Entwicklungstoxizität betrug in dieser Studie 60 mg/kg/Tag (das 1,6-fache der MRHD, die Jugendlichen auf mg/m²-Basis verabreicht wird).
In einer Studie, in der trächtigen Kaninchen während der Organogenese Dosen von bis zu 40 mg/kg verabreicht wurden (etwa das 2,1-fache der MRHD, die Jugendlichen auf mg/m²-Basis verabreicht wird), wurden keine nachteiligen Auswirkungen auf die embryofetale Entwicklung beobachtet.
In anderen Reproduktionsstudien, in denen weiblichen Ratten während der Trächtigkeit und Laktation eine orale Dosis (5, 20, 80 oder 160 mg/kg) verabreicht wurde, wurde bei Dosen von 80 mg/kg/Tag (dem 2-fachen der MRHD) eine erhöhte Jungtiersterblichkeit bei der Geburt beobachtet bei Heranwachsenden auf mg/m²-Basis) oder höher, und es wurde bei allen Dosierungen (Low-Effect-Dosis etwa das 0,13-fache der MRHD bei Heranwachsenden auf mg/m²-Basis) eine Abnahme des Körpergewichts und der Überlebensrate der Jungtiere beobachtet.
Stillzeit
Daten aus der veröffentlichten Literatur berichten über das Vorhandensein von Fluvoxamin in der Muttermilch (vgl Daten ). In den meisten Fällen der mütterlichen Anwendung von Fluvox 50 mgamin während des Stillens wurden keine unerwünschten Wirkungen auf den gestillten Säugling berichtet. Es gibt jedoch Berichte über Durchfall, Erbrechen, verminderten Schlaf und Unruhe (vgl Klinische Überlegungen ). Es liegen keine Daten zur Wirkung von Fluvox 100 mgamin auf die Milchproduktion vor. Die Entwicklungs- und Gesundheitsvorteile des Stillens sollten zusammen mit dem klinischen Bedarf der Mutter an Fluvox 50 mgamin und allen potenziellen Nebenwirkungen von Fluvoxamin oder dem zugrunde liegenden Zustand der Mutter auf das gestillte Kind berücksichtigt werden.
Klinische Überlegungen
Überwachen Sie Säuglinge, die Fluvoxamin über die Muttermilch ausgesetzt waren, auf Durchfall, Erbrechen, verminderten Schlaf und Unruhe.
Daten
In veröffentlichten Fallberichten und Fallserien wurden Arzneimittelkonzentrationen in der Milch von ≤ 425 ng/ml nach mütterlicher Gabe von Fluvox 100 mgamin 25 mg/Tag bis 300 mg/Tag beobachtet.
Weibchen und Männchen mit reproduktivem Potenzial
Unfruchtbarkeit
Tierexperimentelle Befunde deuten darauf hin, dass die Fruchtbarkeit während der Einnahme von Fluvox 50 mgamin beeinträchtigt sein kann [siehe Nichtklinische Toxikologie ].
Pädiatrische Verwendung
Die Wirksamkeit von Fluvox 100 mgaminmaleat zur Behandlung von Zwangsstörungen wurde in einer 10-wöchigen multizentrischen placebokontrollierten Studie mit 120 ambulanten Patienten im Alter von 8 bis 17 Jahren nachgewiesen. Darüber hinaus setzten 99 dieser ambulanten Patienten die unverblindete Behandlung mit Fluvoxaminmaleat bis zu weiteren ein bis drei Jahren fort, was 94 Patientenjahren entspricht. Das in dieser Studie beobachtete Nebenwirkungsprofil war im Allgemeinen ähnlich dem, das in Studien mit Fluvoxamin an Erwachsenen beobachtet wurde [siehe NEBENWIRKUNGEN , DOSIERUNG UND ANWENDUNG ].
Verminderter Appetit und Gewichtsverlust wurden im Zusammenhang mit der Anwendung von Fluvoxamin sowie anderen SSRIs beobachtet. Daher wird eine regelmäßige Überwachung von Gewicht und Wachstum empfohlen, wenn die Behandlung eines Kindes mit einem SSRI langfristig fortgesetzt werden soll.
Die Risiken, die gegebenenfalls mit einer längeren Anwendung von Fluvox 50 mgamin bei Kindern und Jugendlichen mit Zwangsstörungen verbunden sind, wurden nicht systematisch bewertet. Der verschreibende Arzt sollte bedenken, dass die Beweise, auf die er sich stützt, um zu dem Schluss zu kommen, dass Fluvoxamin für die Anwendung bei Kindern und Jugendlichen sicher ist, aus relativ kurzfristigen klinischen Studien und aus der Extrapolation von Erfahrungen mit erwachsenen Patienten stammen. Insbesondere gibt es keine Studien, die die Wirkungen einer Langzeitanwendung von Fluvoxamin auf das Wachstum, die kognitive Verhaltensentwicklung und die Reifung von Kindern und Jugendlichen direkt bewerten. Obwohl es keinen positiven Befund gibt, der darauf hindeutet, dass Fluvoxamin die Fähigkeit besitzt, das Wachstum, die Entwicklung oder die Reifung nachteilig zu beeinflussen, ist das Fehlen solcher Befunde kein zwingender Beweis dafür, dass Fluvoxamin bei chronischer Anwendung keine potenziellen Nebenwirkungen haben kann [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Unbedenklichkeit und Wirksamkeit bei Kindern und Jugendlichen mit Ausnahme von Kindern und Jugendlichen mit Zwangsstörungen wurden nicht nachgewiesen [siehe Eingerahmte Warnung ; WARNUNGEN UND VORSICHTSMASSNAHMEN ]. Jeder, der die Anwendung von Fluvox 100-mgamin-Maleat-Tabletten bei einem Kind oder Jugendlichen in Betracht zieht, muss die potenziellen Risiken mit der klinischen Notwendigkeit abwägen.
Geriatrische Verwendung
Ungefähr 230 Patienten, die an kontrollierten Premarketing-Studien mit Fluvoxaminmaleat-Tabletten teilnahmen, waren 65 Jahre oder älter. Insgesamt wurden keine Unterschiede in der Sicherheit zwischen diesen Patienten und jüngeren Patienten beobachtet. Andere berichtete klinische Erfahrungen haben keine Unterschiede im Ansprechen zwischen älteren und jüngeren Patienten festgestellt. SSRIs und SNRIs, einschließlich Fluvoxaminmaleat-Tabletten, wurden jedoch mit mehreren Fällen von klinisch signifikanter Hyponatriämie bei älteren Patienten in Verbindung gebracht, die möglicherweise ein höheres Risiko für dieses unerwünschte Ereignis haben [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ]. Darüber hinaus ist die Clearance von Fluvoxamin bei älteren Patienten im Vergleich zu jüngeren Patienten um etwa 50 % verringert [vgl KLINISCHE PHARMAKOLOGIE ], und auch eine erhöhte Empfindlichkeit einiger älterer Personen kann nicht ausgeschlossen werden. Daher sollte bei älteren Patienten eine niedrigere Anfangsdosis in Betracht gezogen werden und Fluvox 50 mgaminmaleat-Tabletten sollten zu Beginn der Therapie langsam titriert werden.
ÜBERDOSIS
Folgendes wurde im Zusammenhang mit einer Überdosierung von Fluvox 100 mgamin Tabletten berichtet:
Eine Magen-Darm-Dekontamination mit Aktivkohle sollte bei Patienten erwogen werden, die sich früh nach einer Fluvoxamin-Überdosis vorstellen.
Erwägen Sie, sich an ein Giftzentrum (1-800-221-2222) oder einen medizinischen Toxikologen zu wenden, um Empfehlungen zum Umgang mit einer Überdosierung zu erhalten.
KONTRAINDIKATIONEN
Koadministration
Die gleichzeitige Anwendung von Tizanidin, Thioridazin, Alosetron oder Pimozid mit Fluvox 50 mgaminmaleat-Tabletten ist kontraindiziert [siehe WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Serotonin-Syndrom und Monoaminoxidase-Hemmer (MAO-Hemmer)
Die Anwendung von MAO-Hemmern zur Behandlung psychiatrischer Erkrankungen mit Fluvoxaminmaleat-Tabletten oder innerhalb von 14 Tagen nach Beendigung der Behandlung mit Fluvoxaminmaleat-Tabletten ist aufgrund eines erhöhten Risikos für ein Serotonin-Syndrom kontraindiziert. Die Anwendung von Fluvox 50 mgaminmaleat-Tabletten innerhalb von 14 Tagen nach Absetzen eines MAO-Hemmers zur Behandlung psychiatrischer Erkrankungen ist ebenfalls kontraindiziert [siehe DOSIERUNG UND ANWENDUNG , WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Die Einnahme von Fluvoxaminmaleat-Tabletten bei einem Patienten, der mit MAO-Hemmern wie Linezolid oder intravenösem Methylenblau behandelt wird, ist ebenfalls kontraindiziert, da ein erhöhtes Risiko für ein Serotonin-Syndrom besteht [siehe DOSIERUNG UND ANWENDUNG , WARNUNGEN UND VORSICHTSMASSNAHMEN ].
KLINISCHE PHARMAKOLOGIE
Wirkmechanismus
Es wird angenommen, dass der Wirkungsmechanismus von Fluvox 50 mg Aminmaleat bei Zwangsstörungen mit seiner spezifischen Hemmung der Serotonin-Wiederaufnahme in Gehirnneuronen zusammenhängt. Fluvox 100 mgamin hat sich in präklinischen Studien sowohl in vitro als auch in vivo als wirksamer Hemmer des Serotonin-Wiederaufnahmetransporters erwiesen.
Pharmakodynamik
In In-vitro-Studien hatte Fluvox 100 mgaminmaleat keine signifikante Affinität zu histaminergen, alpha- oder beta-adrenergen, muskarinergen oder dopaminergen Rezeptoren. Es wird angenommen, dass der Antagonismus einiger dieser Rezeptoren mit verschiedenen sedativen, kardiovaskulären, anticholinergen und extrapyramidalen Wirkungen einiger Psychopharmaka verbunden ist.
Pharmakokinetik
Absorption
Die absolute Bioverfügbarkeit von Fluvoxaminmaleat beträgt 53 %. Die orale Bioverfügbarkeit wird durch Nahrung nicht signifikant beeinflusst.
In einer Dosisproportionalitätsstudie mit Fluvoxaminmaleat in Dosierungen von 100, 200 und 300 mg/Tag an 10 aufeinanderfolgenden Tagen bei 30 gesunden Probanden wurde nach etwa einer Woche Dosierung ein Steady State erreicht. Maximale Plasmakonzentrationen im Steady State traten innerhalb von 3 bis 8 Stunden nach der Einnahme auf und erreichten Konzentrationen von durchschnittlich 88, 283 bzw. 546 ng/ml. Somit hatte Fluvoxamin über diesen Dosisbereich eine nichtlineare Pharmakokinetik, dh höhere Dosen von Fluvox 100 mgaminmaleat erzeugten unverhältnismäßig höhere Konzentrationen als aufgrund der niedrigeren Dosis vorhergesagt.
Verteilung
Das mittlere scheinbare Verteilungsvolumen von Fluvoxamin beträgt etwa 25 l/kg, was auf eine ausgedehnte Gewebeverteilung hindeutet.
Ungefähr 80 % von Fluvox 100 mgamin werden in einem Konzentrationsbereich von 20 bis 2000 ng/ml an Plasmaproteine, hauptsächlich Albumin, gebunden.
Stoffwechsel
Fluvox 100 mg Aminmaleat wird weitgehend von der Leber metabolisiert; die Hauptstoffwechselwege sind oxidative Demethylierung und Desaminierung. Neun Metaboliten wurden nach einer radioaktiv markierten 5-mg-Dosis von Fluvox 100 mgaminmaleat identifiziert, die etwa 85 % der Urinausscheidungsprodukte von Fluvox 100 mgamin ausmachen. Der wichtigste menschliche Metabolit war Fluvox 100 mg Aminsäure, das zusammen mit seinem N-acetylierten Analogon etwa 60 % der Urinausscheidungsprodukte ausmachte. Ein dritter Metabolit, Fluvoxethanol, der durch oxidative Desaminierung gebildet wird, machte etwa 10 % aus. Fluvox 100 mg Aminsäure und Fluvox 100 mg Ethanol wurden in einem In-vitro-Test auf Serotonin- und Norepinephrin-Wiederaufnahmehemmung bei Ratten getestet; sie waren außer einer schwachen Wirkung des früheren Metaboliten auf die Hemmung der Serotoninaufnahme (1–2 Größenordnungen weniger wirksam als die Ausgangsverbindung) inaktiv. Ungefähr 2 % von Fluvox 100 mgamin wurden unverändert im Urin ausgeschieden [siehe WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ].
Beseitigung
Nach einer 14C-markierten oralen Dosis von Fluvox 50 mg Aminmaleat (5 mg) wurden innerhalb von 71 Stunden durchschnittlich 94 % der arzneimittelbezogenen Produkte im Urin wiedergefunden.
Die mittlere Plasmahalbwertszeit von Fluvox 100 mgamin im Steady State nach mehrfacher oraler Gabe von 100 mg/Tag bei gesunden, jungen Probanden betrug 15,6 Stunden.
Ältere Themen
In einer Studie mit Fluvoxaminmaleat-Tabletten bei 50 und 100 mg, bei der ältere (66-73 Jahre) und junge Probanden (19-35 Jahre) verglichen wurden, waren die mittleren maximalen Plasmakonzentrationen bei älteren Personen um 40 % höher. Die Eliminationshalbwertszeit nach Mehrfachgabe von Fluvox 50 mgamin betrug 17,4 und 25,9 Stunden bei älteren Patienten im Vergleich zu 13,6 und 15,6 Stunden bei jungen Probanden im Steady State für 50- bzw. 100-mg-Dosen. Bei älteren Patienten war die Clearance von Fluvox 100 mgamin um etwa 50 % reduziert und daher sollten Fluvox 100 mgamin-Maleat-Tabletten zu Beginn der Therapie langsam titriert werden [siehe DOSIERUNG UND ANWENDUNG ].
Pädiatrische Fächer
Die Pharmakokinetik von Fluvox 50 mgamin nach Mehrfachgabe wurde bei männlichen und weiblichen Kindern (im Alter von 6 bis 11 Jahren) und Jugendlichen (im Alter von 12 bis 17 Jahren) bestimmt. Steady-State-Plasmakonzentrationen von Fluvox 100 mgamin waren bei Kindern 2- bis 3-mal höher als bei Jugendlichen. AUC und Cmax waren bei Kindern 1,5- bis 2,7-mal höher als bei Jugendlichen. (Siehe Tabelle 4.) Wie bei Erwachsenen zeigten sowohl Kinder als auch Jugendliche eine nichtlineare Pharmakokinetik nach Mehrfachgabe. Weibliche Kinder zeigten signifikant höhere AUC (0-12) und Cmax im Vergleich zu männlichen Kindern, und daher können niedrigere Dosen von Fluvoxaminmaleat-Tabletten einen therapeutischen Nutzen haben. (Siehe Tabelle 5.) Bei Jugendlichen wurden keine geschlechtsspezifischen Unterschiede beobachtet. Die Steady-State-Plasmakonzentrationen von Fluvoxamin waren bei Erwachsenen und Jugendlichen bei einer Dosis von 300 mg/Tag ähnlich, was darauf hindeutet, dass die Exposition gegenüber Fluvox 100 mg/Tag in diesen beiden Populationen ähnlich war. (Siehe Tabelle 4.) Eine Dosisanpassung bei Jugendlichen (bis zur Maximaldosis von 300 mg für Erwachsene) kann angezeigt sein, um einen therapeutischen Nutzen zu erzielen [siehe DOSIERUNG UND ANWENDUNG ].
TABELLE 4: VERGLEICH DER MITTELWERTEN (SD) DER PHARMAKOKINETISCHEN PARAMETER VON FLUVOX 50 mgAMIN ZWISCHEN KINDERN, JUGENDLICHEN UND ERWACHSENEN
TABELLE 5: VERGLEICH DER DURCHSCHNITTLICHEN (SD) PHARMAKOKINETISCHEN PARAMETER VON FLUVOX 50 mgAMIN ZWISCHEN MÄNNLICHEN UND WEIBLICHEN KINDERN (6 BIS 11 JAHRE)
Leber- und Nierenerkrankungen
Ein studienübergreifender Vergleich (gesunde Probanden versus Patienten mit Leberfunktionsstörung) deutete auf eine 30 %ige Abnahme der Clearance von Fluvox 50 mgamin in Verbindung mit Leberfunktionsstörung hin. Die mittleren minimalen Plasmakonzentrationen bei Patienten mit eingeschränkter Nierenfunktion (Kreatinin-Clearance von 5 bis 45 ml/min) nach 4 und 6 Behandlungswochen (50 mg zweimal täglich, N = 13) waren miteinander vergleichbar, was darauf hindeutet, dass es bei diesen Patienten nicht zu einer Akkumulation von Fluvoxamin kam [sehen WARNUNGEN UND VORSICHTSMASSNAHMEN ].
Klinische Studien
OCD-Studien für Erwachsene
Die Wirksamkeit von Fluvoxaminmaleat-Tabletten zur Behandlung von Zwangsstörungen (OCD) wurde in zwei 10-wöchigen multizentrischen Parallelgruppenstudien mit erwachsenen ambulanten Patienten nachgewiesen. Die Patienten in diesen Studien wurden in den ersten zwei Wochen der Studie auf eine tägliche Gesamtdosis von 50 mg Fluvox Fluvox 50 mg/Tag titriert, wonach die Dosis innerhalb eines Bereichs von 100–300 mg/Tag angepasst wurde (nach einem bid-Plan). , auf der Grundlage von Reaktion und Toleranz. Die Patienten in diesen Studien hatten eine mittelschwere bis schwere Zwangsstörung (DSM-III-R) mit mittleren Ausgangsbewertungen auf der Yale-Brown Obsessive Compulsive Scale (Y-BOCS), Gesamtpunktzahl von 23. Bei Patienten, die Fluvox 50 mg Aminmaleat erhielten, kam es zu einer mittleren Reduktion von ungefähr 4 bis 5 Einheiten auf dem Y-BOCS-Gesamtscore, verglichen mit einer Reduzierung um 2 Einheiten bei Placebo-Patienten.
Tabelle 6 zeigt die Ergebnisklassifikation nach Behandlungsgruppe für das Element „Globale Verbesserung“ der Skala „Clinical Global Impressions“ (CGI) für beide Studien zusammen.
TABELLE 6: ERGEBNISKLASSIFIZIERUNG (%) AUF CGI-GLOBAL-VERBESSERUNGSELEMENT FÜR ABSCHLIESSENDE IN EINEM POOL VON ZWEI OCD-STUDIEN FÜR ERWACHSENE
Explorative Analysen zu Auswirkungen von Alter und Geschlecht auf die Ergebnisse deuteten nicht auf eine unterschiedliche Ansprechbarkeit auf der Grundlage von Alter oder Geschlecht hin.
OCD-Erhaltungsstudie für Erwachsene
In einer Erhaltungsstudie mit erwachsenen ambulanten Patienten mit Zwangsstörungen wurden 114 Patienten, die die DSM-IV-Kriterien für Zwangsstörungen erfüllten und einen Score von ≥ 18 auf der Yale-Brown Obsessive Compulsive Scale (Y-BOCS) aufwiesen, auf eine wirksame Dosis von 100 bis 300 mg Fluvoxaminmaleat-Tabletten titriert /Tag im Rahmen einer anfänglich 10-wöchigen einfach verblindeten Behandlungsphase. Das Ansprechen auf die Behandlung während dieser einfach verblindeten Phase wurde definiert als Y-BOCS-Scores, die am Ende der Wochen 8 und 10 mindestens 30 % unter dem Ausgangswert lagen. Bei den Patienten, die auf die Behandlung ansprachen, betrug ihre durchschnittliche Ansprechdauer 4 Wochen. Patienten, die während dieser Anfangsphase auf die Behandlung ansprachen, wurden in einer doppelblinden Phase zur Beobachtung eines Rückfalls entweder zur Fortsetzung der Behandlung mit Fluvox 50-mgamin-Maleat-Tabletten (N = 56) oder zur Behandlung mit Placebo (N = 58) randomisiert. Ein Rückfall während der doppelblinden Phase wurde definiert als ein Anstieg des Y-BOCS-Scores um mindestens 30 % gegenüber dem Ausgangswert für diese Phase oder die Weigerung des Patienten, die Behandlung aufgrund einer erheblichen Zunahme der Zwangsstörungssymptome fortzusetzen. In der doppelblinden Phase hatten Patienten, die die Behandlung mit Fluvoxaminmaleat-Tabletten fortgesetzt erhielten, im Durchschnitt eine signifikant niedrigere Rückfallrate als Patienten, die Placebo erhielten.
Eine Untersuchung von Bevölkerungsuntergruppen aus dieser Studie ergab keine eindeutigen Hinweise auf einen unterschiedlichen Erhaltungseffekt auf der Grundlage von Alter oder Geschlecht.
Pädiatrische OCD-Studie
Die Wirksamkeit von Fluvoxaminmaleat-Tabletten zur Behandlung von Zwangsstörungen wurde auch in einer 10-wöchigen multizentrischen Parallelgruppenstudie bei einer ambulanten pädiatrischen Population (Kinder und Jugendliche im Alter von 8 bis 17 Jahren) nachgewiesen. Die Patienten in dieser Studie wurden in den ersten zwei Wochen der Studie auf eine tägliche Gesamtdosis von Fluvox 100 mg/Tag von etwa 100 mg/Tag titriert, wonach die Dosis innerhalb eines Bereichs von 50–200 mg/Tag (nach einem bid-Zeitplan) angepasst wurde. auf der Grundlage von Reaktion und Toleranz. Alle Patienten hatten eine mittelschwere bis schwere Zwangsstörung (DSM-III-R) mit einem mittleren Ausgangswert von 24 auf der Kinder-Yale-Brown-Obsessive-Compulsive-Scale (CY-BOCS). ungefähr sechs Einheiten auf dem CY-BOCS-Gesamtscore, verglichen mit einer Reduzierung um drei Einheiten bei Placebo-Patienten.
Tabelle 7 zeigt die Ergebnisklassifikation nach Behandlungsgruppe auf dem Punkt „Globale Verbesserung“ der Skala „Clinical Global Impression“ (CGI) für die pädiatrische Studie.
TABELLE 7: ERGEBNISKLASSIFIZIERUNG (%) BEI CGI-GLOBAL-VERBESSERUNGSELEMENTEN FÜR ABSCHLIESSENDE IN PÄDIATRISCHEN STUDIEN
Explorative Post-hoc-Analysen für geschlechtsspezifische Auswirkungen auf die Ergebnisse deuteten nicht auf eine unterschiedliche Reaktionsfähigkeit auf der Grundlage des Geschlechts hin. Weitere explorative Analysen zeigten einen deutlichen Behandlungseffekt in der Altersgruppe der 8- bis 11-Jährigen und im Wesentlichen keinen Effekt in der Altersgruppe der 12- bis 17-Jährigen. Während die Signifikanz dieser Ergebnisse nicht klar ist, sind die 2- bis 3-fach höheren Fluvoxamin-Plasmakonzentrationen im Steady-State bei Kindern im Vergleich zu Jugendlichen [vgl KLINISCHE PHARMAKOLOGIE ] deutet darauf hin, dass eine verringerte Exposition bei Jugendlichen ein Faktor gewesen sein könnte, und eine Dosisanpassung bei Jugendlichen (bis zur Höchstdosis von 300 mg für Erwachsene) kann angezeigt sein, um einen therapeutischen Nutzen zu erzielen.
INFORMATIONEN ZUM PATIENTEN
Fluvox 100mgamin (Flu VOX ah meen) Maleat-Tabletten
Lesen Sie den mit Fluvox 100mgamine Maleate Tablets gelieferten Medikationsleitfaden, bevor Sie mit der Einnahme beginnen und jedes Mal, wenn Sie eine Nachfüllung erhalten. Möglicherweise gibt es neue Informationen. Dieser Medikationsleitfaden ersetzt nicht das Gespräch mit Ihrem Gesundheitsdienstleister über Ihren Gesundheitszustand oder Ihre Behandlung. Sprechen Sie mit Ihrem Arzt, wenn Sie etwas nicht verstehen oder mehr darüber erfahren möchten.
Was sind die wichtigsten Informationen, die ich über Fluvox 50-mgamin-Maleat-Tabletten wissen sollte?
Fluvoxamin ist die gleiche Art von Arzneimittel wie die zur Behandlung von Depressionen und kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
1. Selbstmordgedanken oder -handlungen:
Halten Sie alle Nachsorgetermine bei Ihrem Arzt und rufen Sie zwischen den Terminen an, wenn Sie sich wegen der Symptome Sorgen machen.
Rufen Sie sofort Ihren Arzt an, wenn Sie eines der folgenden Symptome haben, oder rufen Sie 911 an, wenn ein Notfall auftritt, insbesondere wenn sie neu oder schlimmer sind oder Sie sich Sorgen machen:
Informieren Sie sofort Ihren Arzt, wenn Sie eines der folgenden Symptome haben, oder rufen Sie im Notfall 911 an. Fluvoxaminmaleat-Tabletten können mit diesen schwerwiegenden Nebenwirkungen in Verbindung gebracht werden:
2. Serotonin-Syndrom: Dieser Zustand kann lebensbedrohlich sein und Folgendes umfassen:
3. Visuelle Probleme
Nur einige Menschen sind für diese Probleme gefährdet. Möglicherweise möchten Sie sich einer Augenuntersuchung unterziehen, um festzustellen, ob Sie gefährdet sind, und eine vorbeugende Behandlung erhalten, wenn dies der Fall ist.
4. Schwere allergische Reaktionen:
5. Anormale Blutung: Fluvox 100 mgamine Maleat Tabletten und Antidepressiva können Ihr Risiko für Blutungen oder Blutergüsse erhöhen, insbesondere wenn Sie den Blutverdünner Warfarin (Coumadin®, Jantoven®) oder ein nichtsteroidales entzündungshemmendes Arzneimittel (NSAIDs, wie Ibuprofen, Naproxen oder Aspirin).
6. Krampfanfälle oder Krämpfe
7. Manische Episoden:
8. Veränderungen des Appetits oder des Gewichts. Größe und Gewicht von Kindern und Jugendlichen sollten während der Behandlung überwacht werden.
9. Niedriger Salz- (Natrium-)Spiegel im Blut. Ältere Menschen sind möglicherweise einem höheren Risiko ausgesetzt. Zu den Symptomen können gehören:
10. Sexuelle Probleme (Dysfunktion). Die Einnahme von selektiven Serotonin-Wiederaufnahmehemmern (SSRIs), einschließlich Fluvox 50-mgamin-Maleat-Tabletten, kann sexuelle Probleme verursachen.
Sprechen Sie mit Ihrem medizinischen Betreuer, wenn Sie während der Behandlung mit Fluvox 50-mgamin-Maleat-Tabletten irgendwelche Veränderungen Ihrer Sexualfunktion bemerken oder wenn Sie Fragen oder Bedenken zu sexuellen Problemen haben. Möglicherweise gibt es Behandlungen, die Ihr Arzt vorschlagen kann.
Beenden Sie die Einnahme von Fluvoxaminmaleat-Tabletten nicht, ohne vorher mit Ihrem Arzt gesprochen zu haben.
Ein zu schnelles Absetzen von Fluvoxaminmaleat-Tabletten kann zu schwerwiegenden Symptomen führen, einschließlich:
Was sind Fluvoxaminmaleat-Tabletten?
Fluvoxaminmaleat-Tabletten sind ein verschreibungspflichtiges Arzneimittel zur Behandlung von Zwangsstörungen (OCD). Es ist wichtig, mit Ihrem Arzt über die Risiken der Behandlung von Zwangsstörungen und auch über die Risiken einer Nichtbehandlung zu sprechen. Sie sollten alle Behandlungsoptionen mit Ihrem Arzt besprechen.
Sprechen Sie mit Ihrem Arzt, wenn Sie nicht glauben, dass sich Ihr Zustand durch die Behandlung mit Fluvox 100 mgamine Maleat-Tabletten bessert.
Wer sollte Fluvox 100mgamine Maleate Tablets nicht einnehmen?
Nehmen Sie Fluvoxaminmaleat-Tabletten nicht ein, wenn Sie:
Personen, die Fluvoxaminmaleat-Tabletten zeitnah zu einem MAOI einnehmen, können schwerwiegende oder sogar lebensbedrohliche Nebenwirkungen haben. Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines dieser Symptome haben:
Was sollte ich meinem medizinischen Betreuer vor der Einnahme von Fluvox 50 mgaminmaleat-Tabletten mitteilen? Fragen Sie nach, wenn Sie sich nicht sicher sind.
Bevor Sie mit Fluvoxaminmaleat-Tabletten beginnen, informieren Sie Ihren Arzt, wenn Sie:
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen, einschließlich verschreibungspflichtiger und nicht verschreibungspflichtiger Arzneimittel, Vitamine und Kräuterergänzungen. Fluvoxaminmaleat-Tabletten und einige Arzneimittel können miteinander interagieren, möglicherweise nicht so gut wirken oder schwerwiegende Nebenwirkungen verursachen.
Ihr Arzt oder Apotheker kann Ihnen sagen, ob die Einnahme von Fluvoxaminmaleat-Tabletten zusammen mit Ihren anderen Arzneimitteln unbedenklich ist. Beginnen oder beenden Sie keine Arzneimittel, während Sie Fluvoxaminmaleat-Tabletten einnehmen, ohne vorher mit Ihrem Arzt gesprochen zu haben.
Wenn Sie Fluvox 100 mg Aminmaleat-Tabletten einnehmen, sollten Sie keine anderen Arzneimittel einnehmen, die Fluvoxamin enthalten, einschließlich: LUVOX 50 mg CR®
Wie sollte ich Fluvoxaminmaleat-Tabletten einnehmen?
Was sollte ich während der Einnahme von Fluvox 50mgamine Maleate Tablets vermeiden?
Fluvox 100 mgamine Maleate Tabletten können Schläfrigkeit verursachen oder Ihre Fähigkeit beeinträchtigen, Entscheidungen zu treffen, klar zu denken oder schnell zu reagieren. Sie sollten nicht Auto fahren, schwere Maschinen bedienen oder andere gefährliche Aktivitäten ausüben, bis Sie wissen, wie Fluvoxaminmaleat-Tabletten auf Sie wirken. Trinken Sie während der Anwendung von Fluvoxaminmaleat-Tabletten keinen Alkohol.
Welche Nebenwirkungen kann Fluvox 100mgamine Maleate Tablets haben?
Angstgefühl oder Schlafstörungen
Häufige mögliche Nebenwirkungen bei Personen, die Fluvox 100mgamine Maleate Tabletten einnehmen, umfassen:
Andere Nebenwirkungen bei Kindern und Jugendlichen sind:
Informieren Sie Ihren Arzt, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt. Dies sind nicht alle möglichen Nebenwirkungen von Fluvox 50mgamine Maleate Tablets. Weitere Informationen erhalten Sie von Ihrem Arzt oder Apotheker.
RUFEN SIE IHREN ARZT FÜR ÄRZTLICHE RATSCHLÄGE ÜBER NEBENWIRKUNGEN AN. SIE KÖNNEN NEBENWIRKUNGEN unter 1-800-308-6755 oder der FDA unter 1-800-FDA-1088 MELDEN
Wie soll ich Fluvox 50mgamine Maleate Tablets aufbewahren?
Lagern Sie Fluvoxaminmaleat-Tabletten bei Raumtemperatur zwischen 15 °C und 30 °C (59 °F bis 86 °F).
Bewahren Sie Fluvoxaminmaleat-Tabletten und alle Arzneimittel außerhalb der Reichweite von Kindern auf.
Allgemeine Informationen zu Fluvox 100mgamine Maleate Tabletten
Medikamente werden manchmal für andere als die in einem Medikationsleitfaden aufgeführten Zwecke verschrieben. Verwenden Sie Fluvoxamine Maleate Tablets nicht für einen Zustand, für den es nicht verschrieben wurde. Geben Sie Fluvox 100 mg Aminmaleat-Tabletten nicht an andere Personen weiter, selbst wenn sie unter der gleichen Erkrankung leiden. Es kann ihnen schaden.
Dieser Arzneimittelleitfaden fasst die wichtigsten Informationen zu Fluvoxaminmaleat-Tabletten zusammen. Wenn Sie weitere Informationen wünschen, wenden Sie sich an Ihren Arzt. Sie können Ihren Arzt oder Apotheker um Informationen zu Fluvoxaminmaleat-Tabletten bitten, die für medizinisches Fachpersonal geschrieben sind.
Weitere Informationen zu Fluvox 50-mgamin-Maleat-Tabletten erhalten Sie gebührenfrei unter 1-800-308-6755 oder unter www.anipharmaceuticals.com.
Welche Inhaltsstoffe sind in Fluvoxaminmaleat-Tabletten enthalten?
Wirkstoff: Fluvoxaminmaleat
Inaktive Zutaten:
Die 25-mg-Tabletten: Carnaubawachs, Hypromellose, Mannitol, Polyethylenglycol, Polysorbat 80, Quellstärke (Kartoffel), Siliciumdioxid, Natriumstearylfumarat, Stärke (Mais) und Titandioxid.
Die 50-mg- und 100-mg-Tabletten: Zusätzlich zu den oben genannten Hilfsstoffen enthalten sie synthetische Eisenoxide.
Dieser Medikationsleitfaden wurde von der US Food and Drug Administration genehmigt.