Duricef 250mg, 500mg Cefadroxil Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Duricef und wie wird es angewendet?
Duricef (Cefadroxil) ist ein Cephalosporin-Antibiotikum, das zur Behandlung vieler verschiedener Arten von Infektionen verwendet wird, die durch Bakterien verursacht werden. Der Markenname Duricef wird eingestellt und Cefadroxil ist in generischer Form erhältlich.
Welche Nebenwirkungen hat Duricef?
Häufige Nebenwirkungen von Duricef (Cefadroxil) sind:
Informieren Sie Ihren Arzt, wenn Sie unwahrscheinliche, aber sehr schwerwiegende Nebenwirkungen von Duricef (Cefadroxil) haben, einschließlich:
BEZEICHNUNG
DURICEF (Cefadroxil) ist ein halbsynthetisches Cephalosporin-Antibiotikum, das zur oralen Verabreichung bestimmt ist. Es ist ein weißes bis gelblich-weißes kristallines Pulver. Es ist wasserlöslich und säurestabil. Es wird chemisch als 5-Thia-1-azabicyclo[4.2.0]oct-2-en-2-carbonsäure, 7-[[amino(4-hydroxyphenyl)acetyl]amino]-3-methyl-8-oxo bezeichnet -, Monohydrat[6R-[6α,7β(R*)]]-. Es hat die Formel C16H17N3O5S•H20 und das Molekulargewicht 381,40. Es hat die folgende Strukturformel:
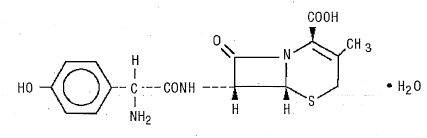
DURICEF (Cefadroxil) Filmtabletten, 1 g, enthalten die folgenden Hilfsstoffe: mikrokristalline Cellulose, Hydroxypropylmethylcellulose, Magnesiumstearat, Polyethylenglycol, Polysorbat 80, Simethicon-Emulsion und Titandioxid.
DURICEF (Cefadroxil) zur oralen Suspension enthält die folgenden inaktiven Bestandteile: FD&C Yellow No. 6, Aromen (natürlich und künstlich), Polysorbat 80, Natriumbenzoat, Saccharose und Xanthangummi.
DURICEF (Cefadroxil)-Kapseln enthalten die folgenden inaktiven Inhaltsstoffe: D&C Red Nr. 28, FD&C Blue Nr. 1, FD&C Red Nr. 40, Gelatine, Magnesiumstearat und Titandioxid.
INDIKATIONEN
DURICEF (Cefadroxil) ist indiziert zur Behandlung von Patienten mit Infektionen, die durch empfindliche Stämme der bezeichneten Organismen bei den folgenden Erkrankungen verursacht werden:
Durch E. coli verursachte Harnwegsinfektionen; P. mirabilis und Klebsiella-Arten.
Durch Staphylokokken und/oder Streptokokken verursachte Infektionen der Haut und Hautstruktur.
Pharyngitis und/oder Tonsillitis, verursacht durch Streptococcus pyogenes (beta-hämolysierende Streptokokken der Gruppe A).
Notiz: Es hat sich gezeigt, dass nur Penicillin bei intramuskulärer Verabreichung zur Prophylaxe von rheumatischem Fieber wirksam ist. DURICEF (Cefadroxil) ist im Allgemeinen wirksam bei der Eradikation von Streptokokken aus dem Oropharynx. Es liegen jedoch keine Daten vor, die die Wirksamkeit von DURICEF (Cefadroxil) zur Prophylaxe eines nachfolgenden rheumatischen Fiebers belegen.
Notiz: Kultur- und Empfindlichkeitstests sollten vor und während der Therapie eingeleitet werden. Nierenfunktionsuntersuchungen sollten durchgeführt werden, wenn dies angezeigt ist.
Um die Entwicklung arzneimittelresistenter Bakterien zu verringern und die Wirksamkeit von DURICEF (Cefadroxil) und anderen antibakteriellen Arzneimitteln aufrechtzuerhalten, sollte DURICEF (Cefadroxil) nur zur Behandlung oder Vorbeugung von Infektionen angewendet werden, die nachweislich oder mit starkem Verdacht auf empfindliche Bakterien zurückzuführen sind. Wenn Kultur- und Empfindlichkeitsinformationen verfügbar sind, sollten diese bei der Auswahl oder Änderung der antibakteriellen Therapie berücksichtigt werden. In Ermangelung solcher Daten können lokale Epidemiologie und Anfälligkeitsmuster zur empirischen Auswahl der Therapie beitragen.
DOSIERUNG UND ANWENDUNG
DURICEF (Cefadroxil) ist säurestabil und kann unabhängig von den Mahlzeiten oral verabreicht werden. Die Verabreichung zusammen mit Nahrung kann hilfreich sein, um potenzielle gastrointestinale Beschwerden zu lindern, die gelegentlich mit einer oralen Cephalosporin-Therapie verbunden sind.
Erwachsene
Harnwegsinfektion: Bei unkomplizierten Infektionen der unteren Harnwege (z. B. Zystitis) beträgt die übliche Dosierung 1 oder 2 g pro Tag in einer einzelnen (qd) oder geteilten Dosis (bid).
Bei allen anderen Harnwegsinfektionen beträgt die übliche Dosierung 2 g pro Tag in geteilten Dosen (bid).
Haut- und Hautstrukturinfektionen: Bei Haut- und Hautstrukturinfektionen beträgt die übliche Dosierung 1 g pro Tag in Einzeldosen (qd) oder geteilten Dosen (bid).
Pharyngitis und Tonsillitis: Behandlung von beta-hämolytischer Streptokokken-Pharyngitis und Tonsillitis der Gruppe A – 1 g pro Tag in Einzeldosen (qd) oder geteilten Dosen (bid) für 10 Tage.
Kinder
Bei Harnwegsinfektionen beträgt die empfohlene Tagesdosis für Kinder 30 mg/kg/Tag in aufgeteilten Dosen alle 12 Stunden. Bei Pharyngitis, Tonsillitis und Impetigo beträgt die empfohlene Tagesdosis für Kinder 30 mg/kg/Tag in einer Einzeldosis oder in gleichmäßig aufgeteilten Dosen alle 12 Stunden. Bei anderen Haut- und Hautstrukturinfektionen beträgt die empfohlene Tagesdosis 30 mg/kg/Tag in gleichmäßig aufgeteilten Dosen alle 12 Stunden. Bei der Behandlung von beta-hämolytischen Streptokokkeninfektionen sollte eine therapeutische Dosis von DURICEF (Cefadroxil) für mindestens 10 Tage verabreicht werden.
Siehe Tabelle für die tägliche Gesamtdosis für Kinder.
Nierenfunktionsstörung
Bei Patienten mit eingeschränkter Nierenfunktion sollte die Dosierung von Cefadroxil-Monohydrat entsprechend der Kreatinin-Clearance-Raten angepasst werden, um eine Akkumulation des Arzneimittels zu verhindern. Folgender Zeitplan wird vorgeschlagen. Bei Erwachsenen beträgt die Anfangsdosis 1000 mg DURICEF (Cefadroxil) und die Erhaltungsdosis (basierend auf der Kreatinin-Clearance-Rate [ml/min/1,73 M2]) 500 mg in den unten aufgeführten Zeitintervallen.
Patienten mit Kreatinin-Clearance-Raten über 50 ml/min können wie Patienten mit normaler Nierenfunktion behandelt werden.
WIE GELIEFERT
DURICEF® (Cefadroxil-Monohydrat, USP) 500 mg Kapseln: undurchsichtige, kastanienbraune und weiße Hartgelatinekapseln mit dem Aufdruck „PPP“ und „784“ an einem Ende und „DURICEF (Cefadroxil)“ und „500 mg“ am anderen Ende .
Kapseln werden wie folgt geliefert:
N 0430-0780-19....................Flasche mit 50 Stück
Bei kontrollierter Raumtemperatur von 15° - 30° C (59° - 86° F) lagern.
DURICEF® (Cefadroxil) 1 Gramm Tabletten: weiß bis gebrochen weiß, oben halbiert, oval, mit dem Aufdruck „PPP“ auf der einen Seite der Halbierung und „785“ auf der anderen Seite der Halbierung. Tabletten werden wie folgt geliefert:
N 0430-0781-19.......................Flasche mit 50 Stück
Bei kontrollierter Raumtemperatur von 15° - 30° C (59° - 86° F) lagern.
DURICEF® (Cefadroxil) zur oralen Suspension hat einen Orangen-Ananas-Geschmack und wird wie folgt geliefert:
250 mg/5 ml.................................N 0430-2782-15 50-ml-Flasche
Vor der Rekonstitution: Bei kontrollierter Raumtemperatur von 15° - 30° C (59° - 86° F) lagern.
Hergestellt von Bristol-Myers Squibb Co. Princeton, NJ 08543. Für Warner Chilcott Company, Inc. Fajardo, PR 00738. Vertrieben von Warner Chilcott (US), Inc. Rockaway, NJ 07866. Überarbeitet im April 2007. FDA Revisionsdatum: 6/ 5/2007
NEBENWIRKUNGEN
Magen-Darm
Das Auftreten pseudomembranöser Colitis-Symptome kann während oder nach einer Antibiotikabehandlung auftreten (vgl WARNUNGEN ). Dyspepsie, Übelkeit und Erbrechen wurden selten berichtet. Auch Durchfall ist aufgetreten.
Überempfindlichkeit
Allergien (in Form von Hautausschlag, Urtikaria, Angioödem und Juckreiz) wurden beobachtet. Diese Reaktionen ließen normalerweise nach Absetzen des Medikaments nach. Anaphylaxie wurde ebenfalls berichtet.
Sonstiges
Andere Reaktionen waren Leberfunktionsstörungen einschließlich Cholestase und Erhöhungen der Serumtransaminasen, genitaler Pruritus, genitale Moniliasis, Vaginitis, mäßige vorübergehende Neutropenie, Fieber. Agranulozytose, Thrombozytopenie, idiosynkratisches Leberversagen, Erythema multiforme, Stevens-Johnson-Syndrom, Serumkrankheit und Arthralgie wurden selten berichtet.
Zusätzlich zu den oben aufgeführten Nebenwirkungen, die bei mit Cefadroxil behandelten Patienten beobachtet wurden, wurden die folgenden Nebenwirkungen und veränderten Labortests für Antibiotika der Cephalosporin-Klasse berichtet:
Toxische epidermale Nekrolyse, Bauchschmerzen, Superinfektion, Nierenfunktionsstörung, toxische Nephropathie, aplastische Anämie, hämolytische Anämie, Blutung, verlängerte Prothrombinzeit, positiver Coombs-Test, erhöhter BUN, erhöhtes Kreatinin, erhöhte alkalische Phosphatase, erhöhte Aspartataminotransferase (AST), erhöht Alaninaminotransferase (ALT), erhöhtes Bilirubin, erhöhtes LDH, Eosinophilie, Panzytopenie, Neutropenie.
Mehrere Cephalosporine wurden mit der Auslösung von Krampfanfällen in Verbindung gebracht, insbesondere bei Patienten mit eingeschränkter Nierenfunktion, wenn die Dosis nicht reduziert wurde (siehe DOSIERUNG UND VERABREICHUNG und ÜBERDOSIERUNG ). Wenn im Zusammenhang mit der medikamentösen Therapie Krampfanfälle auftreten, sollte das Medikament abgesetzt werden. Bei klinischer Indikation kann eine antikonvulsive Therapie gegeben werden.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Arzneimittel-/Labortest-Wechselwirkungen
Positive direkte Coombs-Tests wurden während der Behandlung mit den Cephalosporin-Antibiotika berichtet. Bei hämatologischen Studien oder bei Transfusions-Cross-Matching-Verfahren, wenn Antiglobulintests auf der kleinen Seite durchgeführt werden, oder bei Coombs-Tests bei Neugeborenen, deren Mütter vor der Geburt Cephalosporin-Antibiotika erhalten haben, sollte berücksichtigt werden, dass ein positiver Coombs-Test darauf zurückzuführen sein kann Arzneimittel.
WARNUNGEN
BEVOR EINE THERAPIE MIT DURICEF (Cefadroxil) EINGELEITET WIRD, SOLLTE SORGFÄLTIG ABGEFRAGT WERDEN, OB DER PATIENT FRÜHERE ÜBERSENSIBILITÄTSREAKTIONEN AUF CEFADROXTL, CEPHALOSPORINE, PENICILLINE ODER ANDERE ARZNEIMITTEL HAT. WENN DIESES PRODUKT AN PENICILLIN-EMPFINDLICHE PATIENTEN GEGEBEN WERDEN SOLLTE, SOLLTE VORSICHT GEGEBEN WERDEN, DA EINE QUERSENSITIVITÄT ZWISCHEN BETA-LACTAM-ANTIBIOTIKA EINDEUTIG DOKUMENTIERT WURDE UND BEI BIS ZU 10 % DER PATIENTEN MIT EINER VORGESCHICHTENEN PENICILLIN-ALLERGIE AUFTRETEN KANN.
WENN EINE ALLERGISCHE REAKTION AUF DURICEF (Cefadroxil) auftritt, SETZEN SIE DAS ARZNEIMITTEL AB. SCHWERE AKUTE ÜBERSENSIBILITÄTSREAKTIONEN KÖNNEN EINE BEHANDLUNG MIT Epinephrin UND ANDERE NOTFALLMASSNAHMEN, EINSCHLIESSLICH SAUERSTOFF, INTRAVENÖSE FLÜSSIGKEITEN, INTRAVENÖSE ANTIHISTAMINE, KORTIKOSTEROIDE, PRESSORAMINE UND ATEMWEGSMANAGEMENT ERFORDERLICH MACHEN, WIE KLINISCH INDIVIDUELL.
Clostridium difficile-assoziierte Diarrhoe (CDAD) wurde bei der Anwendung von fast allen antibakteriellen Mitteln, einschließlich DURICEF (Cefadroxil), berichtet, und der Schweregrad kann von leichter Diarrhoe bis hin zu tödlicher Colitis reichen. Die Behandlung mit antibakteriellen Mitteln verändert die normale Flora des Dickdarms, was zu einem übermäßigen Wachstum von C. difficile führt.
C. difficile produziert die Toxine A und B, die zur Entstehung von CD AD beitragen. Hypertoxin produzierende Stämme von C. difficile verursachen eine erhöhte Morbidität und Mortalität, da diese Infektionen gegenüber einer antimikrobiellen Therapie refraktär sein können und eine Kolektomie erfordern können. CD AD muss bei allen Patienten in Betracht gezogen werden, die nach der Anwendung von Antibiotika an Durchfall leiden. Eine sorgfältige Anamnese ist erforderlich, da berichtet wurde, dass CD AD mehr als zwei Monate nach der Verabreichung von antibakteriellen Mitteln auftritt.
Wenn CD AD vermutet oder bestätigt wird, muss die laufende Antibiotikaanwendung, die nicht gegen C. difficile gerichtet ist, möglicherweise eingestellt werden. Je nach klinischer Indikation sollte ein angemessenes Flüssigkeits- und Elektrolytmanagement, eine Proteinergänzung, eine antibiotische Behandlung von C. difficile und eine chirurgische Untersuchung eingeleitet werden.
VORSICHTSMASSNAHMEN
Allgemein
DURICEF (Cefadroxil) sollte bei deutlich eingeschränkter Nierenfunktion (Kreatinin-Clearance-Rate von weniger als 50 ml/min/1,73 M2) mit Vorsicht angewendet werden. (Sehen DOSIERUNG UND ANWENDUNG .) Bei Patienten mit bekannter oder vermuteter Nierenfunktionsstörung sollten vor und während der Therapie sorgfältige klinische Beobachtungen und geeignete Laboruntersuchungen durchgeführt werden.
Die Verschreibung von DURICEF (Cefadroxil) ohne nachgewiesene oder dringend vermutete bakterielle Infektion oder ohne prophylaktische Indikation bringt dem Patienten wahrscheinlich keinen Nutzen und erhöht das Risiko der Entwicklung arzneimittelresistenter Bakterien.
Eine längere Anwendung von DURICEF (Cefadroxil) kann zu einem übermäßigen Wachstum von honsuszeptiblen Organismen führen. Eine sorgfältige Beobachtung des Patienten ist unerlässlich. Wenn während der Therapie eine Superinfektion auftritt, sollten geeignete Maßnahmen ergriffen werden.
DURICEF (Cefadroxil) sollte bei Personen mit Magen-Darm-Erkrankungen in der Vorgeschichte, insbesondere Kolitis, mit Vorsicht verschrieben werden.
Karzinogenese, Mutagenese und Beeinträchtigung der Fruchtbarkeit
Es wurden keine Langzeitstudien zur Bestimmung des kanzerogenen Potentials durchgeführt. Es wurden keine genetischen Toxizitätstests durchgeführt.
Schwangerschaft: Schwangerschaftskategorie B
Reproduktionsstudien wurden an Mäusen und Ratten mit bis zum 11-Fachen der Humandosis durchgeführt und ergaben keine Hinweise auf eine Beeinträchtigung der Fruchtbarkeit oder eine Schädigung des Fötus durch Cefadroxil-Monohydrat. Es gibt jedoch keine ausreichenden und gut kontrollierten Studien bei Schwangeren. Da Reproduktionsstudien an Tieren die menschliche Reaktion nicht immer vorhersagen, sollte dieses Medikament während der Schwangerschaft nur angewendet werden, wenn dies eindeutig erforderlich ist.
Arbeit und Lieferung
Die Anwendung von DURICEF (Cefadroxil) während der Wehen und der Geburt wurde nicht untersucht. Eine Behandlung sollte nur erfolgen, wenn dies eindeutig erforderlich ist.
Stillende Mutter
Vorsicht ist geboten, wenn Cefadroxil-Monohydrat einer stillenden Mutter verabreicht wird.
Pädiatrische Verwendung
(Sehen DOSIERUNG UND ANWENDUNG. )
Geriatrische Verwendung
Von etwa 650 Patienten, die Cefadroxil zur Behandlung von Harnwegsinfektionen in drei klinischen Studien erhielten, waren 28 % 60 Jahre und älter, während 16 % 70 Jahre und älter waren. Von etwa 1.000 Patienten, die Cefadroxil zur Behandlung von Haut- und Hautstrukturinfektionen in 14 klinischen Studien erhielten, waren 12 % 60 Jahre und älter, während 4 % 70 Jahre und älter waren. Insgesamt wurden keine Unterschiede in der Sicherheit zwischen den älteren Patienten in diesen Studien und jüngeren Patienten beobachtet. Klinische Studien mit Cefadroxil für die. Die Behandlung von Pharyngitis oder Tonsillitis schloss keine ausreichende Anzahl von Patienten ab 65 Jahren ein, um festzustellen, ob sie anders ansprechen als jüngere Patienten. Andere berichtete klinische Erfahrungen mit Cefadroxil haben keine Unterschiede im Ansprechen zwischen älteren und jüngeren Patienten festgestellt, aber eine größere Empfindlichkeit einiger älterer Personen kann nicht ausgeschlossen werden.
Cefadroxil wird im Wesentlichen über die Nieren ausgeschieden, und bei Patienten mit eingeschränkter Nierenfunktion ist eine Dosisanpassung indiziert (vgl DOSIERUNG UND VERABREICHUNG: Nierenfunktionsstörung ). Da bei älteren Patienten mit größerer Wahrscheinlichkeit eine eingeschränkte Nierenfunktion vorliegt, sollte die Dosis sorgfältig ausgewählt werden, und es kann sinnvoll sein, die Nierenfunktion zu überwachen.
ÜBERDOSIS
Eine Studie mit Kindern unter sechs Jahren legte nahe, dass die Einnahme von weniger als 250 mg/kg Cephalosporinen nicht mit signifikanten Ergebnissen verbunden ist. Außer allgemeiner Unterstützung und Beobachtung sind keine Maßnahmen erforderlich. Bei Mengen über 250 mg/kg Magenentleerung einleiten.
Bei fünf anurischen Patienten wurde gezeigt, dass durchschnittlich 63 % einer oralen Dosis von 1 g während einer 6- bis 8-stündigen Hämodialysesitzung aus dem Körper extrahiert werden.
KONTRAINDIKATIONEN
DURICEF (Cefadroxil) ist kontraindiziert bei Patienten mit bekannter Allergie gegen Antibiotika der Cephalosporin-Gruppe.
KLINISCHE PHARMAKOLOGIE
DURICEF (Cefadroxil) wird nach oraler Verabreichung schnell resorbiert. Nach Einzeldosen von 500 mg und 1000 mg betrugen die durchschnittlichen maximalen Serumkonzentrationen etwa 16 bzw. 28 |ag/ml. Messbare Konzentrationen waren 12 Stunden nach der Verabreichung vorhanden. Über 90 % des Arzneimittels werden innerhalb von 24 Stunden unverändert mit dem Urin ausgeschieden. Die Spitzenkonzentrationen im Urin betragen etwa 1800 pg/ml während des Zeitraums nach einer oralen Einzeldosis von 500 mg. Erhöhungen der Dosierung führen im Allgemeinen zu einem proportionalen Anstieg der Konzentration von DURICEF (Cefadroxil-Monohydrat, USP) im Urin. Die Antibiotikakonzentration im Urin wurde nach einer Dosis von 1 g für 20 bis 22 Stunden deutlich über der MHK empfindlicher Pathogene im Urin gehalten.
Mikrobiologie
In-vitro-Tests zeigen, dass die Cephalosporine aufgrund ihrer Hemmung der Zellwandsynthese bakterizid sind. Es wurde gezeigt, dass Cefadroxil sowohl in vitro als auch bei klinischen Infektionen gegen die folgenden Organismen aktiv ist (siehe INDIKATIONEN ):
Beta-hämolytische Streptokokken Staphylokokken, einschließlich Penicillinase-produzierender Stämme Streptococcus (Diplococcus) pneumoniae Escherichia coli Proteus mirabilis Klebsiella-Spezies Moraxella (Branhamella) catarrhalis
Notiz: Die meisten Stämme von Entercoccus faecalis (früher Streptococcus faecalis) und Enterococcus faecium (früher Streptococcus faecium) sind resistent gegen DURICEF (Cefadroxil). Es ist nicht aktiv gegen die meisten Stämme von Enterobacter-Spezies, Morganella morganii (ehemals Proteus morganii) und P. vulgaris. Es hat keine Aktivität gegen Pseudomonas-Spezies und Acinetobacter calcoaceticus (ehemals Mima- und Herellea-Spezies).
Empfindlichkeitstests: Diffusionstechniken
Die Verwendung von Antibiotika-Empfindlichkeitstestmethoden, die den Zonendurchmesser messen, ergibt eine genaue Schätzung der Antibiotika-Empfindlichkeit. Ein solches Standardverfahren1, das zur Verwendung mit Blättchen empfohlen wurde, um die Empfindlichkeit von Organismen gegenüber Cefadroxil zu testen, verwendet das Blättchen der Cephalosporin-Klasse (Cephalothin). Die Interpretation beinhaltet die Korrelation der im Scheibentest erhaltenen Durchmesser mit der minimalen Hemmkonzentration (MHK) für Cefadroxil.
Berichte aus dem Labor, die Ergebnisse des standardmäßigen Single-Blättchen-Empfindlichkeitstests mit einem 30-µg-Cephalothin-Blättchen enthalten, sollten gemäß den folgenden Kriterien interpretiert werden:
Ein Bericht von „anfällig“ weist darauf hin, dass der Erreger wahrscheinlich durch allgemein erreichbare Blutspiegel gehemmt wird. Ein Bericht über „mittlere Empfindlichkeit“ deutet darauf hin, dass der Organismus anfällig wäre, wenn eine hohe Dosis verwendet wird oder wenn die Infektion auf Gewebe und Flüssigkeiten (z. B. Urin) beschränkt ist, in denen hohe Antibiotikaspiegel erreicht werden. Ein Bericht von „Resistenz“ weist darauf hin, dass erreichbare Konzentrationen des Antibiotikums wahrscheinlich nicht hemmend wirken und eine andere Therapie gewählt werden sollte.
Standardisierte Verfahren erfordern die Verwendung von Laborkontrollorganismen. Die 30-µg-Cephalothinscheibe sollte die folgenden Zonendurchmesser ergeben:
Verdünnungstechniken
Bei Verwendung der NCCLS-Agarverdünnungs- oder Bouillonverdünnungsmethode (einschließlich Mikroverdünnung)2 oder einer gleichwertigen Methode kann ein Bakterienisolat als empfindlich angesehen werden, wenn der MHK-Wert (minimale Hemmkonzentration) für Cephalothin 8 µg/ml oder weniger beträgt. Organismen gelten als resistent, wenn die MHK 32 µg/ml oder mehr beträgt. Organismen mit einem MHK-Wert von weniger als 32 µg/ml, aber mehr als 8 µg/ml sind intermediär.
Wie bei Standarddiffusionsmethoden erfordern Verdünnungsverfahren die Verwendung von Laborkontrollorganismen. Standard-Cephalothinpulver sollte MHK-Werte im Bereich von 0,12 µg/ml und 0,5 µg/ml für Staphylococcus aureus ATCC 29213 ergeben. Vox Escherichia coli ATCC 25922, der MHK-Bereich sollte zwischen 4,0 µg/ml und 16,0 µg/ml liegen. Für Streptococcus faecalis ATCC 29212 sollte der MHK-Bereich zwischen 8,0 und 32,0 µg/ml liegen.
VERWEISE
1. National Committee for Clinical Laboratory Standards, Approved Standard, Performance Standards for Antimicrobial Disk Susceptibility Test, 4th Edition, Vol. 1, No. 10 (7): M2-A4, Villanova, PA, April 1990.
2. National Committee for Clinical Laboratory Standards, Approved Standard: Methods for Dilution Antimicrobial susceptibility tests for Bacteria that Grow Aerobically, 2nd Edition, Vol. 2, No. 10 (8): M7-A2, Villanova, PA, April 1990.
INFORMATIONEN ZUM PATIENTEN
Die Patienten sollten darauf hingewiesen werden, dass antibakterielle Arzneimittel einschließlich DURICEF (Cefadroxil) nur zur Behandlung bakterieller Infektionen angewendet werden sollten. Sie behandeln keine Virusinfektionen (z. B. Erkältung). Wenn DURICEF (Cefadroxil) zur Behandlung einer bakteriellen Infektion verschrieben wird, sollten die Patienten darüber aufgeklärt werden, dass das Medikament genau nach Anweisung eingenommen werden sollte, obwohl es üblich ist, dass sie sich zu Beginn der Therapie besser fühlen. Das Auslassen von Dosen oder das Nichtbeenden des vollständigen Therapiezyklus kann (1) die Wirksamkeit der sofortigen Behandlung verringern und (2) die Wahrscheinlichkeit erhöhen, dass Bakterien Resistenzen entwickeln und in Zukunft nicht mehr mit DURICEF (Cefadroxil) oder anderen antibakteriellen Arzneimitteln behandelbar sind .
Durchfall ist ein häufiges Problem, das durch Antibiotika verursacht wird und normalerweise endet, wenn das Antibiotikum abgesetzt wird. Manchmal können Patienten nach Beginn der Behandlung mit Antibiotika wässrigen und blutigen Stuhl (mit oder ohne Magenkrämpfe und Fieber) sogar noch zwei oder mehr Monate nach Einnahme der letzten Dosis des Antibiotikums entwickeln. In diesem Fall sollten die Patienten so schnell wie möglich ihren Arzt kontaktieren.