Floxin 100mg, 200mg, 400mg Ofloxacin Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Floxin und wie wird es angewendet?
Floxin 200 mg ist ein verschreibungspflichtiges Medikament zur Behandlung der Symptome vieler verschiedener bakterieller Infektionen wie Lungenentzündung, Hautinfektionen, Bronchitis und akute entzündliche Erkrankungen des Beckens. Floxin kann allein oder mit anderen Medikamenten verwendet werden.
Floxin gehört zu einer Klasse von Medikamenten namens Fluorchinolone.
Es ist nicht bekannt, ob Floxin 200 mg bei Kindern sicher und wirksam ist.
Welche Nebenwirkungen kann Floxin haben?
Floxin 100 mg kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigsten Nebenwirkungen von Floxin gehören:
Teilen Sie dem Arzt mit, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Floxin. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
WARNUNG
Fluorchinolone, einschließlich FLOXIN® (Ofloxacin), sind in allen Altersgruppen mit einem erhöhten Risiko für Sehnenentzündungen und Sehnenrisse verbunden. Dieses Risiko ist bei älteren Patienten, die normalerweise über 60 Jahre alt sind, bei Patienten, die Kortikosteroide einnehmen, und bei Patienten mit Nieren-, Herz- oder Lungentransplantation weiter erhöht (siehe WARNHINWEISE).
Fluorchinolone, einschließlich FLOXIN® (Ofloxacin), können Muskelschwäche bei Personen mit Myasthenia gravis verschlimmern. Vermeiden Sie FLOXIN® (Ofloxacin) bei Patienten mit bekannter Vorgeschichte von Myasthenia gravis (siehe WARNHINWEISE).
Um die Entwicklung von arzneimittelresistenten Bakterien zu verringern und die Wirksamkeit von FLOXIN® (Ofloxacin-Tabletten) Tabletten und anderen antibakteriellen Arzneimitteln aufrechtzuerhalten, sollten FLOXIN® (Ofloxacin-Tabletten) Tabletten nur zur Behandlung oder Vorbeugung von Infektionen angewendet werden, bei denen es sich um nachgewiesene oder dringend vermutete Infektionen handelt durch Bakterien verursacht.
BEZEICHNUNG
FLOXIN® (Ofloxacin-Tabletten) Tabletten ist ein synthetisches Breitspektrum-Antibiotikum zur oralen Verabreichung. Chemisch gesehen ist Ofloxacin, ein fluoriertes Carboxychinolon, das Racemat, (±)-9-Fluor-2,3-dihydro-3-methyl-10-(4-methyl-1-piperazinyl)-7oxo-7H-pyrido[1, 2,3-de]-1,4-Benzoxazin-6-Carbonsäure. Die chemische Struktur ist:
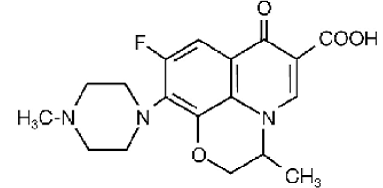
Seine empirische Formel lautet C18H20FN3O4 und sein Molekulargewicht beträgt 361,4. Ofloxacin ist ein cremefarbenes bis blassgelbes kristallines Pulver. Das Molekül liegt bei den pH-Bedingungen im Dünndarm als Zwitterion vor. Die relativen Löslichkeitseigenschaften von Ofloxacin bei Raumtemperatur gemäß USP-Nomenklatur weisen darauf hin, dass Ofloxacin in wässrigen Lösungen mit einem pH-Wert zwischen 2 und 5 als löslich angesehen wird. Es ist in wässrigen Lösungen mit einem pH-Wert von 7 sparsam bis leicht löslich (die Löslichkeit fällt auf 4 mg/ml) und in wässrigen Lösungen mit einem pH-Wert über 9 frei löslich. Ofloxacin hat das Potenzial, mit vielen Metallionen stabile Koordinationsverbindungen zu bilden. Dieses in-vitro-Chelationspotential hat die folgende Bildungsreihenfolge: Fe+3 > Al+3 > Cu+2 > Ni+2 > Pb+2 > Zn+2 > Mg+2 > Ca+2 > Ba+2.
FLOXIN® (Ofloxacin) Tabletten enthalten die folgenden Hilfsstoffe: wasserfreie Lactose, modifizierte Maisstärke, Hydroxypropylcellulose, Hypromellose, Magnesiumstearat, Polyethylenglykol, Polysorbat 80, Natriumstärkeglykolat, Titandioxid und können auch synthetisches gelbes Eisenoxid enthalten.
INDIKATIONEN
Um die Entwicklung von arzneimittelresistenten Bakterien zu verringern und die Wirksamkeit von FLOXIN® (Ofloxacin-Tabletten) Tabletten und anderen antibakteriellen Arzneimitteln aufrechtzuerhalten, sollten FLOXIN® (Ofloxacin-Tabletten) Tabletten nur zur Behandlung oder Vorbeugung von Infektionen angewendet werden, bei denen es sich um nachgewiesene oder dringend vermutete Infektionen handelt durch anfällige Bakterien verursacht. Wenn Kultur- und Empfindlichkeitsinformationen verfügbar sind, sollten diese bei der Auswahl oder Änderung der antibakteriellen Therapie berücksichtigt werden. In Ermangelung solcher Daten können lokale Epidemiologie und Anfälligkeitsmuster zur empirischen Auswahl der Therapie beitragen.
FLOXIN® (Ofloxacin-Tabletten) Tabletten sind indiziert zur Behandlung von Erwachsenen mit leichten bis mittelschweren Infektionen (sofern nicht anders angegeben), die durch empfindliche Stämme der bezeichneten Mikroorganismen bei den unten aufgeführten Infektionen verursacht werden. Bitte sehen DOSIERUNG UND ANWENDUNG für konkrete Empfehlungen.
Akute bakterielle Exazerbationen einer chronischen Bronchitis aufgrund von Haemophilus influenzae oder Streptococcus pneumoniae.
Ambulant erworbene Pneumonie aufgrund von Haemophilus influenzae oder Streptococcus pneumoniae.
Unkomplizierte Haut- und Hautstrukturinfektionen aufgrund von Methicillin-empfindlichem Staphylococcus aureus, Streptococcus pyogenes oder Proteus mirabilis.
Akute, unkomplizierte urethrale und zervikale Gonorrhoe aufgrund von Neisseria gonorrhoeae. (Sehen WARNUNGEN .)
Nongonokokken-Urethritis und Zervizitis durch Chlamydia trachomatis. (Sehen WARNUNGEN .)
Mischinfektionen der Harnröhre und des Gebärmutterhalses aufgrund von Chlamydia trachomatis und Neisseria gonorrhoeae. (Sehen WARNUNGEN .)
Akute entzündliche Erkrankungen des Beckens (einschließlich schwerer Infektion) aufgrund von Chlamydia trachomatis und/oder Neisseria gonorrhoeae. (Sehen WARNUNGEN .)
HINWEIS: Wenn der Verdacht besteht, dass anaerobe Mikroorganismen zur Infektion beitragen, sollte eine geeignete Therapie gegen anaerobe Erreger eingeleitet werden.
Unkomplizierte Zystitis durch Citrobacter diversus, Enterobacter aerogenes, Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis oder Pseudomonas aeruginosa.
Komplizierte Harnwegsinfektionen durch Escherichia coli, Klebsiella pneumoniae, Proteus mirabilis, Citrobacter diversus* oder Pseudomonas aeruginosa*.
Prostatitis wegen Escherichia coli.
* = Obwohl die Behandlung von Infektionen durch diesen Organismus in diesem Organsystem ein klinisch signifikantes Ergebnis zeigte, wurde die Wirksamkeit bei weniger als 10 Patienten untersucht.
Vor der Behandlung sollten geeignete Kultur- und Empfindlichkeitstests durchgeführt werden, um die Erreger der Infektion zu isolieren und zu identifizieren und ihre Empfindlichkeit gegenüber Ofloxacin zu bestimmen. Eine Behandlung mit Ofloxacin kann begonnen werden, bevor die Ergebnisse dieser Tests bekannt sind; Sobald Ergebnisse vorliegen, sollte eine geeignete Therapie fortgesetzt werden.
Wie bei anderen Arzneimitteln dieser Klasse können einige Stämme von Pseudomonas aeruginosa während der Behandlung mit Ofloxacin ziemlich schnell Resistenzen entwickeln. Während der Therapie regelmäßig durchgeführte Kultur- und Empfindlichkeitstests geben nicht nur Aufschluss über die therapeutische Wirkung des antimikrobiellen Mittels, sondern auch über das mögliche Auftreten einer bakteriellen Resistenz.
DOSIERUNG UND ANWENDUNG
Die übliche Dosis von FLOXIN® (Ofloxacin-Tabletten) Tabletten beträgt 200 mg bis 400 mg oral alle 12 Stunden, wie in der folgenden Dosierungstabelle beschrieben. Diese Empfehlungen gelten für Patienten mit normaler Nierenfunktion (dh Kreatinin-Clearance > 50 ml/min). Für Patienten mit veränderter Nierenfunktion (d. h. Kreatinin-Clearance Patienten mit eingeschränkter Nierenfunktion Unterabschnitt.
Antazida, die Calcium, Magnesium oder Aluminium enthalten; Sucralfat; zweiwertige oder dreiwertige Kationen wie Eisen; oder zinkhaltige Multivitamine; oder Videx® (Didanosin) sollten nicht innerhalb von zwei Stunden vor oder innerhalb von zwei Stunden nach der Einnahme von Ofloxacin eingenommen werden. (Sehen VORSICHTSMASSNAHMEN .)
Patienten mit eingeschränkter Nierenfunktion : Die Dosierung sollte bei Patienten mit einer Kreatinin-Clearance
Wenn nur das Serum-Kreatinin bekannt ist, kann die folgende Formel verwendet werden, um die Kreatinin-Clearance abzuschätzen.
Frauen: 0,85 x der für Männer errechnete Wert
Das Serum-Kreatinin sollte einen Steady-State der Nierenfunktion darstellen.
Patienten mit Zirrhose:
Die Ausscheidung von Ofloxacin kann bei Patienten mit schweren Leberfunktionsstörungen (z. B. Zirrhose mit oder ohne Aszites) reduziert sein. Eine Höchstdosis von 400 mg Ofloxacin pro Tag sollte daher nicht überschritten werden.
WIE GELIEFERT
FLOXIN® (Ofloxacin-Tabletten) Tabletten sind als 200 mg hellgelbe, 300 mg weiße und 400 mg blassgoldene, ovale, geradkantige, überzogene Tabletten erhältlich. Jede Tablette ist durch den Aufdruck „FLOXIN (Ofloxacin)“ und die entsprechende Stärke gekennzeichnet. FLOXIN® (Ofloxacin) Tabletten sind in Flaschen in den folgenden Konfigurationen verpackt:
200mg Tabletten - Flaschen mit 50 ( NDC 0062 - 1540-02)
300mg Tabletten - Flaschen mit 50 ( NDC 0062 - 1541-02)
400mg Tabletten - Flaschen mit 100 ( NDC 0062 - 1542-01)
FLOXIN® (Ofloxacin) Tabletten sollten in gut verschlossenen Behältern aufbewahrt werden. Bei 25 °C (77 °F) lagern; Ausflüge erlaubt bis 15-30°C (59-86°F).
Von Kindern fern halten.
Ortho-McNeil, Division of Ortho-McNeil-Janssen Pharmaceuticals, Inc. Raritan, NJ USA 08869. Ausgestellt im Januar 2011
NEBENWIRKUNGEN
Das Folgende ist eine Zusammenstellung der Daten für Ofloxacin, basierend auf klinischer Erfahrung mit oralen und intravenösen Darreichungsformen. Die Inzidenz arzneimittelbedingter Nebenwirkungen bei Patienten während der klinischen Studien der Phasen 2 und 3 betrug 11 %. Unter den Patienten, die eine Mehrfachdosistherapie erhielten, brachen 4 % Ofloxacin aufgrund von Nebenwirkungen ab.
In klinischen Studien wurden die folgenden Ereignisse bei Patienten, die Mehrfachdosen von Ofloxacin erhielten, als wahrscheinlich arzneimittelbedingt angesehen:
Übelkeit 3 %, Schlaflosigkeit 3 %, Kopfschmerzen 1 %, Schwindel 1 %, Durchfall 1 %, Erbrechen 1 %, Hautausschlag 1 %, Juckreiz 1 %, äußerer genitaler Juckreiz bei Frauen 1 %, Vaginitis 1 %, Dysgeusie 1 %.
In klinischen Studien waren die am häufigsten berichteten unerwünschten Ereignisse, unabhängig vom Zusammenhang mit dem Medikament:
Übelkeit 10 %, Kopfschmerzen 9 %, Schlaflosigkeit 7 %, äußerer genitaler Pruritus bei Frauen 6 %, Schwindel 5 %, Vaginitis 5 %, Durchfall 4 %, Erbrechen 4 %.
In klinischen Studien traten bei 1 bis 3 % der Patienten die folgenden Ereignisse auf, unabhängig vom Zusammenhang mit dem Medikament:
Bauchschmerzen und -krämpfe, Brustschmerzen, verminderter Appetit, Mundtrockenheit, Geschmacksstörung, Müdigkeit, Blähungen, Magen-Darm-Beschwerden, Nervosität, Pharyngitis, Pruritus, Fieber, Hautausschlag, Schlafstörungen, Somnolenz, Rumpfschmerzen, vaginaler Ausfluss, Sehstörungen und Verstopfung.
Zusätzliche Ereignisse, die in klinischen Studien mit einer Rate von weniger als 1 % auftraten, waren unabhängig vom Zusammenhang mit dem Medikament:
Körper als Ganzes: Asthenie, Schüttelfrost, Unwohlsein, Gliederschmerzen, Schmerzen, Epistaxis
Herz-Kreislauf-System: Herzstillstand, Ödeme, Bluthochdruck, Hypotonie, Herzklopfen, Vasodilatation
Magen-Darm-System: Dyspepsie
Genital-/Reproduktionssystem: Brennen, Reizung, Schmerzen und Hautausschlag der weiblichen Genitalien; Dysmenorrhoe; Menorrhagie; Metrorrhagie
Bewegungsapparat: Arthralgie, Myalgie
Nervöses System: Krampfanfälle, Angstzustände, kognitive Veränderungen, Depressionen, Traumanomalien, Euphorie, Halluzinationen, Parästhesien, Synkopen, Schwindel, Zittern, Verwirrtheit
Ernährung/Stoffwechsel: Durst, Gewichtsverlust
Atmungssystem: Atemstillstand, Husten, Schnupfen
Haut/Überempfindlichkeit: Angioödem, Schwitzen, Urtikaria, Vaskulitis
Besondere Sinne: verminderte Hörschärfe, Tinnitus, Photophobie
Harnsystem: Dysurie, häufiges Wasserlassen, Harnverhalt
Die folgenden Laboranomalien traten bei ≥ 1,0 % der Patienten auf, die mehrere Dosen Ofloxacin erhielten. Es ist nicht bekannt, ob diese Anomalien durch das Medikament oder die behandelten Grunderkrankungen verursacht wurden.
Hämatopoetisch: Anämie, Leukopenie, Leukozytose, Neutropenie, Neutrophilie, vermehrte Bandformen, Lymphozytopenie, Eosinophilie, Lymphozytose, Thrombozytopenie, Thrombozytose, erhöhte ESR
Leber: erhöht: alkalische Phosphatase, AST (SGOT), ALT (SGPT) Serumchemie: Hyperglykämie, Hypoglykämie, erhöhtes Kreatinin, erhöhter BUN Harn: Glukosurie, Proteinurie, Alkalinurie, Hyposthenie, Hämaturie, Pyurie
Unerwünschte Ereignisse nach der Markteinführung
Zusätzliche unerwünschte Ereignisse, unabhängig vom Zusammenhang mit dem Medikament, die aus weltweiten Marketingerfahrungen mit Chinolonen, einschließlich Ofloxacin, berichtet wurden:
Klinisch
Herz-Kreislauf-System: zerebrale Thrombose, Lungenödem, Tachykardie, Hypotonie/Schock, Synkope, Torsades de Pointes
Endokrin/Stoffwechsel: Hyper- oder Hypoglykämie, insbesondere bei Diabetikern, die Insulin oder orale Antidiabetika erhalten (vgl VORSICHTSMASSNAHMEN : Allgemein und WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN .)
Magen-Darm-System: Leberfunktionsstörung einschließlich: Lebernekrose, Gelbsucht (cholestatisch oder hepatozellulär), Hepatitis; Darmperforation; Leberversagen (einschließlich tödlicher Fälle); pseudomembranöse Kolitis (das Einsetzen pseudomembranöser Kolitissymptome kann während oder nach einer antimikrobiellen Behandlung auftreten), gastrointestinale Blutung; Schluckauf, schmerzhafte Mundschleimhaut, Pyrosis (vgl WARNUNGEN .)
Genital-/Reproduktionssystem: vaginale Candidiasis
Hämatopoetisch: Anämie, einschließlich hämolytischer und aplastischer; Blutung, Panzytopenie, Agranulozytose, Leukopenie, reversible Knochenmarkdepression, Thrombozytopenie, thrombotisch-thrombozytopenische Purpura, Petechien, Ekchymose/Bluterguss (siehe WARNUNGEN .)
Bewegungsapparat: Sehnenentzündung/Ruptur; die Schwäche; Rhabdomyolyse (vgl WARNUNGEN .)
Nervöses System: Alpträume; Selbstmordgedanken oder -handlungen, Orientierungslosigkeit, psychotische Reaktionen, Paranoia; Phobie, Erregung, Unruhe, Aggressivität/Feindseligkeit, manische Reaktion, emotionale Labilität; periphere Neuropathie, Ataxie, Inkoordination; Exazerbation von: Myasthenia gravis und extrapyramidalen Störungen; Dysphasie, Benommenheit (vgl WARNUNGEN und VORSICHTSMASSNAHMEN .)
Atmungssystem: Dyspnoe, Bronchospasmus, allergische Pneumonitis, Stridor (vgl WARNUNGEN .)
Haut/Überempfindlichkeit: anaphylaktische (-toide) Reaktionen/Schock; Purpura, Serumkrankheit, Erythema multiforme/Stevens-Johnson-Syndrom, Erythema nodosum, exfoliative Dermatitis, Hyperpigmentierung, toxische epidermale Nekrolyse, Konjunktivitis, Photosensitivitäts-/Phototoxizitätsreaktion, vesikulobullöse Eruption (siehe WARNUNGEN und VORSICHTSMASSNAHMEN .)
Besondere Sinne: Diplopie, Nystagmus, verschwommenes Sehen, Geschmacks-, Geruchs-, Hör- und Gleichgewichtsstörungen, meist reversibel nach Absetzen
Harnsystem: Anurie, Polyurie, Nierensteine, Nierenversagen, interstitielle Nephritis, Hämaturie (vgl WARNUNGEN und VORSICHTSMASSNAHMEN .)
Labor
Hämatopoetisch: Verlängerung der Prothrombinzeit
Serumchemie: Azidose, Erhöhung von: Serumtriglyceriden, Serumcholesterin, Serumkalium, Leberfunktionstests einschließlich: GGTP, LDH, Bilirubin
Urin: Albuminurie, Candidurie
In klinischen Studien mit Mehrfachdosistherapie wurden bei Patienten, die sich einer Behandlung mit anderen Chinolonen unterzogen, ophthalmologische Anomalien, einschließlich Katarakte und mehrfache punktförmige linsenförmige Trübungen, festgestellt. Die Beziehung der Medikamente zu diesen Ereignissen ist derzeit nicht nachgewiesen.
CRYSTALLURIA und CYLINDRURIA WURDEN MIT ANDEREN QUINOLONEN BERICHTET.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Antazida, Sucralfat, Metallkationen, Multivitamine
Chinolone bilden Chelate mit Erdalkali- und Übergangsmetallkationen. Die Verabreichung von Chinolonen mit Antazida, die Calcium, Magnesium oder Aluminium enthalten, mit Sucralfat, mit zwei- oder dreiwertigen Kationen wie Eisen oder mit zinkhaltigen Multivitaminen oder mit Videx® (Didanosin) kann die Resorption von Chinolonen erheblich beeinträchtigen, was zu erheblichen systemischen Spiegeln führt niedriger als gewünscht. Diese Mittel sollten nicht innerhalb von zwei Stunden vor oder innerhalb von zwei Stunden nach der Ofloxacin-Gabe eingenommen werden. (Sehen DOSIERUNG UND ANWENDUNG .)
Koffein
Wechselwirkungen zwischen Ofloxacin und Koffein wurden nicht nachgewiesen.
Cimetidin
Cimetidin hat eine Interferenz mit der Elimination einiger Chinolone gezeigt. Diese Interferenz hat zu einer signifikanten Verlängerung der Halbwertszeit und der AUC einiger Chinolone geführt. Das Potenzial für Wechselwirkungen zwischen Ofloxacin und Cimetidin wurde nicht untersucht.
Cyclosporin
Erhöhte Serumspiegel von Cyclosporin wurden bei gleichzeitiger Anwendung von Cyclosporin mit einigen anderen Chinolonen berichtet. Das Potenzial für Wechselwirkungen zwischen Ofloxacin und Cyclosporin wurde nicht untersucht.
Arzneimittel, die durch Cytochrom-P450-Enzyme metabolisiert werden
Die meisten Chinolon-Antibiotika hemmen die Cytochrom-P450-Enzymaktivität. Dies kann bei gleichzeitiger Verabreichung mit Chinolonen zu einer verlängerten Halbwertszeit einiger Arzneimittel führen, die ebenfalls über dieses System metabolisiert werden (z. B. Cyclosporin, Theophyllin/Methylxanthine, Warfarin). Das Ausmaß dieser Hemmung variiert zwischen verschiedenen Chinolonen. (Sehen andere Arzneimittelwechselwirkungen .)
Nicht-steroidale entzündungshemmende Medikamente
Die gleichzeitige Verabreichung eines nichtsteroidalen Antirheumatikums mit einem Chinolon, einschließlich Ofloxacin, kann das Risiko einer ZNS-Stimulation und krampfartigen Anfällen erhöhen. (Sehen WARNUNGEN und VORSICHTSMASSNAHMEN : Allgemein .)
Probenecid
Es wurde berichtet, dass die gleichzeitige Anwendung von Probenecid mit bestimmten anderen Chinolonen die renale tubuläre Sekretion beeinflusst. Die Wirkung von Probenecid auf die Elimination von Ofloxacin wurde nicht untersucht.
Theophyllin
Steady-State-Theophyllinspiegel können ansteigen, wenn Ofloxacin und Theophyllin gleichzeitig verabreicht werden. Wie bei anderen Chinolonen kann die gleichzeitige Verabreichung von Ofloxacin die Halbwertszeit von Theophyllin verlängern, die Theophyllinspiegel im Serum erhöhen und das Risiko von Theophyllin-bedingten Nebenwirkungen erhöhen. Bei gleichzeitiger Anwendung von Ofloxacin sollten die Theophyllinspiegel engmaschig überwacht und gegebenenfalls die Theophyllindosis angepasst werden. Nebenwirkungen (einschließlich Krampfanfälle) können mit oder ohne Erhöhung des Theophyllinspiegels im Serum auftreten. (Sehen WARNUNGEN und VORSICHTSMASSNAHMEN : Allgemein .)
Warfarin
Von einigen Chinolonen wurde berichtet, dass sie die Wirkung des oralen Antikoagulans Warfarin oder seiner Derivate verstärken. Wenn ein Chinolon-Antibiotikum gleichzeitig mit Warfarin oder seinen Derivaten verabreicht wird, sollte daher die Prothrombinzeit oder ein anderer geeigneter Gerinnungstest engmaschig überwacht werden.
Antidiabetika (z. B. Insulin, Glyburid/Glibenclamid)
Da bei Patienten, die gleichzeitig mit Chinolonen und einem Antidiabetikum behandelt wurden, über Blutzuckerstörungen, einschließlich Hyperglykämie und Hypoglykämie, berichtet wurde, wird eine sorgfältige Überwachung des Blutzuckers empfohlen, wenn diese Arzneimittel gleichzeitig angewendet werden. (Sehen VORSICHTSMASSNAHMEN : Allgemein und INFORMATIONEN ZUM PATIENTEN .)
Wechselwirkung mit Labor- oder Diagnosetests
Einige Chinolone, einschließlich Ofloxacin, können unter Verwendung von im Handel erhältlichen Immunoassay-Kits zu falsch positiven Urin-Screening-Ergebnissen für Opiate führen. Eine Bestätigung positiver Opiat-Screenings durch spezifischere Methoden kann erforderlich sein.
WARNUNGEN
Tendinopathie und Sehnenriss
Fluorchinolone, einschließlich FLOXIN® (Ofloxacin), sind in allen Altersgruppen mit einem erhöhten Risiko für Sehnenentzündungen und Sehnenrisse verbunden. Diese Nebenwirkung betrifft am häufigsten die Achillessehne, und ein Riss der Achillessehne kann eine chirurgische Reparatur erfordern. Tendinitis und Sehnenrisse in der Rotatorenmanschette (der Schulter), der Hand, dem Bizeps, dem Daumen und anderen Sehnen wurden ebenfalls berichtet. Das Risiko, eine Fluorchinolon-assoziierte Tendinitis und einen Sehnenriss zu entwickeln, ist bei älteren Patienten, üblicherweise über 60 Jahren, bei Patienten, die Kortikosteroide einnehmen, und bei Patienten mit Nieren-, Herz- oder Lungentransplantation weiter erhöht. Zu den Faktoren, die neben dem Alter und der Anwendung von Kortikosteroiden das Risiko eines Sehnenrisses unabhängig voneinander erhöhen können, gehören anstrengende körperliche Aktivität, Nierenversagen und frühere Sehnenerkrankungen wie rheumatoide Arthritis. Bei Patienten, die Fluorchinolone einnahmen und die oben genannten Risikofaktoren nicht aufwiesen, wurde über Tendinitis und Sehnenrisse berichtet. Ein Sehnenriss kann während oder nach Abschluss der Therapie auftreten; Fälle, die bis zu mehrere Monate nach Abschluss der Therapie auftraten, wurden berichtet. FLOXIN® (Ofloxacin) sollte abgesetzt werden, wenn beim Patienten Schmerzen, Schwellungen, Entzündungen oder Sehnenrisse auftreten. Den Patienten sollte geraten werden, sich beim ersten Anzeichen einer Tendinitis oder eines Sehnenrisses auszuruhen und sich bezüglich eines Wechsels zu einem antimikrobiellen Arzneimittel, das kein Chinolon ist, an ihren Arzt zu wenden.
DIE SICHERHEIT UND WIRKSAMKEIT VON OFLOXACIN BEI PÄDIATRISCHEN PATIENTEN UND JUGENDLICHEN (UNTER 18 JAHREN), SCHWANGEREN UND STILLENDEN FRAUEN WURDEN NICHT NACHGEWIESEN. (Sehen VORSICHTSMASSNAHMEN : Pädiatrische Verwendung , Schwangerschaft , und Unterabschnitte für stillende Mütter .)
Bei unreifen Ratten erhöhte die orale Verabreichung von Ofloxacin mit dem 5- bis 16-fachen der empfohlenen maximalen Humandosis, basierend auf mg/kg oder dem 1- bis 3-fachen, basierend auf mg/m², die Inzidenz und den Schweregrad von Osteochondrose. Die Läsionen bildeten sich nach 13 Wochen Arzneimittelentzug nicht zurück. Auch andere Chinolone erzeugen ähnliche Erosionen in den gewichtstragenden Gelenken und andere Anzeichen von Arthropathie bei unreifen Tieren verschiedener Arten. (Sehen Tierpharmakologie .)
Exazerbation von Myasthenia gravis
Fluorchinolone, einschließlich FLOXIN® (Ofloxacin), haben eine neuromuskuläre Blockierungsaktivität und können Muskelschwäche bei Personen mit Myasthenia gravis verschlimmern. Nach der Markteinführung wurden schwerwiegende unerwünschte Ereignisse, einschließlich Todesfälle und Notwendigkeit einer Beatmungsunterstützung, mit der Anwendung von Fluorchinolonen bei Personen mit Myasthenia gravis in Verbindung gebracht. Vermeiden Sie FLOXIN® (Ofloxacin) bei Patienten mit bekannter Vorgeschichte von Myasthenia gravis. (Sehen INFORMATIONEN ZUM PATIENTEN und NEBENWIRKUNGEN : Unerwünschte Ereignisse nach der Markteinführung .)
Auswirkungen auf das zentrale Nervensystem
Krampfanfälle, erhöhter Hirndruck und toxische Psychosen wurden bei Patienten berichtet, die Chinolone, einschließlich Ofloxacin, erhielten. Chinolone, einschließlich Ofloxacin, können auch eine Stimulierung des zentralen Nervensystems verursachen, was zu Zittern, Unruhe/Erregung, Nervosität/Angst, Benommenheit, Verwirrtheit, Halluzinationen, Paranoia und Depression, Albträumen, Schlaflosigkeit und selten Selbstmordgedanken oder -handlungen führen kann. Diese Reaktionen können nach der ersten Dosis auftreten. Wenn diese Reaktionen bei Patienten auftreten, die Ofloxacin erhalten, sollte das Arzneimittel abgesetzt und geeignete Maßnahmen eingeleitet werden. Schlaflosigkeit kann bei Ofloxacin häufiger auftreten als bei einigen anderen Produkten aus der Klasse der Chinolone. Wie alle Chinolone sollte Ofloxacin bei Patienten mit einer bekannten oder vermuteten ZNS-Erkrankung, die zu Krampfanfällen prädisponieren oder die Krampfschwelle senken kann (z. B. schwere zerebrale Arteriosklerose, Epilepsie) oder bei Vorliegen anderer prädisponierender Risikofaktoren mit Vorsicht angewendet werden zu Krampfanfällen führen oder die Krampfschwelle senken (z. B. bestimmte medikamentöse Therapie, Nierenfunktionsstörung). (Sehen VORSICHTSMASSNAHMEN : Allgemein , INFORMATIONEN ZUM PATIENTEN , WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN und NEBENWIRKUNGEN .)
Überempfindlichkeitsreaktionen
Schwerwiegende und gelegentlich tödlich verlaufende Überempfindlichkeitsreaktionen und/oder anaphylaktische Reaktionen wurden bei Patienten berichtet, die eine Therapie mit Chinolonen, einschließlich Ofloxacin, erhielten. Diese Reaktionen treten häufig nach der ersten Dosis auf. Einige Reaktionen wurden von kardiovaskulärem Kollaps, Hypotonie/Schock, Krampfanfällen, Bewusstlosigkeit, Kribbeln, Angioödem (einschließlich Zungen-, Kehlkopf-, Rachen- oder Gesichtsödem/-schwellung), Atemwegsobstruktion (einschließlich Bronchospasmus, Kurzatmigkeit und akuter Atemwegserkrankung) begleitet Distress), Dyspnoe, Urtikaria, Juckreiz und andere schwerwiegende Hautreaktionen. Dieses Arzneimittel sollte beim ersten Auftreten eines Hautausschlags oder anderen Anzeichen einer Überempfindlichkeit sofort abgesetzt werden. Schwerwiegende akute Überempfindlichkeitsreaktionen können je nach klinischer Indikation eine Behandlung mit Epinephrin und andere Wiederbelebungsmaßnahmen erfordern, einschließlich Sauerstoff, intravenöse Flüssigkeiten, Antihistaminika, Kortikosteroide, Pressoramine und Atemwegsmanagement. (Sehen VORSICHTSMASSNAHMEN und NEBENWIRKUNGEN .)
Andere schwerwiegende und manchmal tödliche Ereignisse, einige aufgrund von Überempfindlichkeit und einige aufgrund unklarer Ätiologie, wurden selten bei Patienten berichtet, die eine Therapie mit Chinolonen, einschließlich Ofloxacin, erhielten. Diese Ereignisse können schwerwiegend sein und treten im Allgemeinen nach Verabreichung mehrerer Dosen auf. Klinische Manifestationen können eine oder mehrere der folgenden umfassen:
Das Medikament sollte beim ersten Auftreten von Hautausschlag, Gelbsucht oder anderen Anzeichen einer Überempfindlichkeit sofort abgesetzt und unterstützende Maßnahmen eingeleitet werden (siehe INFORMATIONEN ZUM PATIENTEN und NEBENWIRKUNGEN ).
Periphere Neuropathie
Seltene Fälle von sensorischer oder sensomotorischer axonaler Polyneuropathie, die kleine und/oder große Axone betraf und zu Parästhesien, Hypästhesien, Dysästhesien und Schwäche führte, wurden bei Patienten berichtet, die Chinolone, einschließlich Ofloxacin, erhielten. Ofloxacin sollte abgesetzt werden, wenn bei dem Patienten Symptome einer Neuropathie auftreten, einschließlich Schmerzen, Brennen, Kribbeln, Taubheitsgefühl und/oder Schwäche oder andere Veränderungen der Empfindung, einschließlich leichter Berührung, Schmerzen, Temperaturgefühl, Positionsgefühl und Vibrationsgefühl, um die Entwicklung von Neuropathie zu verhindern ein irreversibler Zustand.
Clostridium difficile-assoziierte Diarrhoe (CDAD) wurde bei der Anwendung von fast allen antibakteriellen Mitteln, einschließlich FLOXIN® (Ofloxacin), berichtet und kann in ihrer Schwere von leichter Diarrhoe bis hin zu tödlicher Colitis reichen. Die Behandlung mit antibakteriellen Mitteln verändert die normale Flora des Dickdarms, was zu einem übermäßigen Wachstum von C. difficile führt.
C. difficile produziert die Toxine A und B, die zur Entstehung von CDAD beitragen. Hypertoxin produzierende Stämme von C. difficile verursachen eine erhöhte Morbidität und Mortalität, da diese Infektionen gegenüber einer antimikrobiellen Therapie refraktär sein können und eine Kolektomie erfordern können. CDAD muss bei allen Patienten in Betracht gezogen werden, bei denen nach der Anwendung von Antibiotika Durchfall auftritt. Eine sorgfältige Anamnese ist erforderlich, da berichtet wurde, dass CDAD mehr als zwei Monate nach der Verabreichung von Antibiotika auftritt.
Wenn CDAD vermutet oder bestätigt wird, muss die laufende Anwendung von Antibiotika, die nicht gegen C. difficile gerichtet sind, möglicherweise eingestellt werden. Je nach klinischer Indikation sollte ein angemessenes Flüssigkeits- und Elektrolytmanagement, eine Proteinergänzung, eine antibiotische Behandlung von C. difficile und eine chirurgische Untersuchung eingeleitet werden. (Sehen NEBENWIRKUNGEN .)
Ofloxacin hat sich bei der Behandlung von Syphilis nicht als wirksam erwiesen.
Antimikrobielle Wirkstoffe, die kurzzeitig in hohen Dosen zur Behandlung von Gonorrhö eingesetzt werden, können die Symptome einer beginnenden Syphilis maskieren oder verzögern. Alle Patienten mit Gonorrhoe sollten sich zum Zeitpunkt der Diagnose einem serologischen Test auf Syphilis unterziehen. Bei Patienten, die wegen Gonorrhoe mit Ofloxacin behandelt werden, sollte nach drei Monaten ein serologischer Follow-up-Test auf Syphilis durchgeführt werden, und bei positivem Ergebnis sollte eine Behandlung mit einem geeigneten antimikrobiellen Mittel eingeleitet werden.

VORSICHTSMASSNAHMEN
Allgemein
Die Verschreibung von FLOXIN® (Ofloxacin-Tabletten) Tabletten ohne nachgewiesene oder dringend vermutete bakterielle Infektion oder eine prophylaktische Indikation bringt dem Patienten wahrscheinlich keinen Nutzen und erhöht das Risiko der Entwicklung arzneimittelresistenter Bakterien.
Bei Patienten, die Ofloxacin erhalten, sollte eine ausreichende Flüssigkeitszufuhr aufrechterhalten werden, um die Bildung eines hochkonzentrierten Urins zu verhindern.
Bei Vorliegen einer Nieren- oder Leberinsuffizienz/-beeinträchtigung ist Ofloxacin mit Vorsicht zu verabreichen. Bei Patienten mit bekannter oder vermuteter Nieren- oder Leberinsuffizienz/-beeinträchtigung sollten vor und während der Therapie eine sorgfältige klinische Beobachtung und geeignete Laboruntersuchungen durchgeführt werden, da die Elimination von Ofloxacin verringert sein kann. Bei Patienten mit eingeschränkter Nierenfunktion (Kreatinin-Clearance KLINISCHE PHARMAKOLOGIE und DOSIERUNG UND ANWENDUNG .)
Mittelschwere bis schwere Lichtempfindlichkeits-/Phototoxizitätsreaktionen, letztere können sich als übertriebene Sonnenbrandreaktionen (z. B. Brennen, Erythem, Exsudation, Bläschen, Blasenbildung, Ödeme) äußern, die lichtexponierte Bereiche betreffen (typischerweise das Gesicht, „V“-Bereich des Halses). , Streckseiten der Unterarme, Handrücken), können mit der Anwendung von Chinolonen nach Sonnen- oder UV-Lichteinwirkung in Verbindung gebracht werden. Daher sollte eine übermäßige Exposition gegenüber diesen Lichtquellen vermieden werden. Die medikamentöse Therapie sollte abgebrochen werden, wenn eine Lichtempfindlichkeit/Phototoxizität auftritt (siehe NEBENWIRKUNGEN / Unerwünschte Ereignisse nach der Markteinführung ).
Wie andere Chinolone sollte Ofloxacin bei jedem Patienten mit einer bekannten oder vermuteten ZNS-Störung, die zu Krampfanfällen prädisponieren oder die Krampfschwelle senken kann (z. B. schwere zerebrale Arteriosklerose, Epilepsie), oder bei Vorliegen anderer Risikofaktoren, die dies können, mit Vorsicht angewendet werden zu Krampfanfällen prädisponieren oder die Krampfschwelle senken (z. B. bestimmte medikamentöse Therapie, Nierenfunktionsstörung). (Sehen WARNUNGEN und WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN .)
Es wurde über eine mögliche Wechselwirkung zwischen oralen Antidiabetika (z. B. Glyburid/Glibenclamid) oder mit antimikrobiellen Wirkstoffen aus Insulin und Fluorchinolonen berichtet, die zu einer Potenzierung der hypoglykämischen Wirkung dieser Arzneimittel führt. Der Mechanismus für diese Wechselwirkung ist nicht bekannt. Wenn bei einem Patienten, der mit Ofloxacin behandelt wird, eine hypoglykämische Reaktion auftritt, setzen Sie Ofloxacin sofort ab und konsultieren Sie einen Arzt. (Sehen WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN und NEBENWIRKUNGEN .)
Wie bei jedem potenten Medikament ist während einer längeren Therapie eine regelmäßige Überprüfung der Organsystemfunktionen, einschließlich Nieren-, Leber- und hämatopoetischer Funktionen, ratsam. (Sehen WARNUNGEN und NEBENWIRKUNGEN .)
Torsade de pointes
Einige Chinolone, einschließlich Ofloxacin, wurden mit einer Verlängerung des QT-Intervalls im Elektrokardiogramm und seltenen Fällen von Arrhythmie in Verbindung gebracht. Seltene Fälle von Torsades de Pointes wurden während der Überwachung nach Markteinführung bei Patienten, die Chinolone, einschließlich Ofloxacin, erhielten, spontan berichtet. Ofloxacin sollte bei Patienten mit bekannter Verlängerung des QT-Intervalls, Patienten mit unkorrigierter Hypokaliämie und Patienten, die Antiarrhythmika der Klasse IA (Chinidin, Procainamid) oder Klasse III (Amiodaron, Sotalol) erhalten, vermieden werden.
Informationen für Patienten
Patienten sollten darauf hingewiesen werden
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Langzeitstudien zur Bestimmung des kanzerogenen Potenzials von Ofloxacin wurden nicht durchgeführt.
Ofloxacin war nicht mutagen im Ames-Bakterientest, im zytogenetischen In-vitro- und In-vivo-Assay, im Schwesterchromatid-Austausch (chinesischer Hamster und menschliche Zelllinien), bei der außerplanmäßigen DNA-Reparatur (UDS) mit menschlichen Fibroblasten, im Dominant-Letal-Assay oder im Maus-Mikronukleus-Assay. Ofloxacin war im UDS-Test mit Rattenhepatozyten und Maus-Lymphom-Assay positiv.
Schwangerschaft
Teratogene Wirkungen – Schwangerschaftskategorie C
Ofloxacin hat keine teratogenen Wirkungen bei oralen Dosen von bis zu 810 mg/kg/Tag (das 11-fache der empfohlenen maximalen Humandosis basierend auf mg/m² oder das 50-fache der empfohlenen maximalen Humandosis basierend auf mg/kg) und 160 mg/kg/Tag. Tag (das 4-fache der empfohlenen maximalen Humandosis basierend auf mg/m² oder das 10-fache der empfohlenen maximalen Humandosis basierend auf mg/kg) bei Verabreichung an trächtige Ratten bzw. Kaninchen. Zusätzliche Studien an Ratten mit oralen Dosen von bis zu 360 mg/kg/Tag (das 5-fache der empfohlenen maximalen Humandosis basierend auf mg/m² oder das 23-fache der empfohlenen maximalen Humandosis basierend auf mg/kg) zeigten keine nachteiligen Auswirkungen auf die späte fötale Entwicklung, Wehen, Geburt, Laktation, Lebensfähigkeit des Neugeborenen oder Wachstum des Neugeborenen. Dosen, die dem 50- bzw. 10-fachen der empfohlenen maximalen Humandosis von Ofloxacin (basierend auf mg/kg) entsprachen, waren bei Ratten bzw. Kaninchen fetotoxisch (dh verringertes fötales Körpergewicht und erhöhte fötale Sterblichkeit). Geringfügige Skelettvariationen wurden bei Ratten berichtet, die Dosen von 810 mg/kg/Tag erhielten, was mehr als das 10-fache der empfohlenen maximalen Humandosis, basierend auf mg/m², ist.
Es gibt jedoch keine adäquaten und gut kontrollierten Studien bei Schwangeren. Ofloxacin sollte während der Schwangerschaft nur angewendet werden, wenn der potenzielle Nutzen das potenzielle Risiko für den Fötus rechtfertigt. (Sehen WARNUNGEN .)
Stillende Mutter
Bei stillenden Frauen führte eine orale Einzeldosis von 200 mg Ofloxacin zu Konzentrationen von Ofloxacin in der Milch, die denen im Plasma ähnlich waren. Aufgrund der Möglichkeit schwerwiegender Nebenwirkungen von Ofloxacin bei gestillten Säuglingen sollte eine Entscheidung getroffen werden, ob das Stillen oder das Medikament abgesetzt werden soll, wobei die Bedeutung des Medikaments für die Mutter zu berücksichtigen ist. (Sehen WARNUNGEN und NEBENWIRKUNGEN .)
Pädiatrische Verwendung
Die Sicherheit und Wirksamkeit bei pädiatrischen Patienten und Jugendlichen unter 18 Jahren ist nicht erwiesen. Ofloxacin verursacht bei Jungtieren verschiedener Arten Arthropathie (Arthrose) und Osteochondrose. (Sehen WARNUNGEN .)
Geriatrische Verwendung
Geriatrische Patienten haben ein erhöhtes Risiko für die Entwicklung schwerer Sehnenerkrankungen einschließlich Sehnenriss, wenn sie mit einem Fluorchinolon wie FLOXIN® (Ofloxacin) behandelt werden. Dieses Risiko ist bei Patienten, die gleichzeitig eine Kortikosteroidtherapie erhalten, weiter erhöht. Tendinitis oder Sehnenruptur können die Achillessehne, Hand, Schulter oder andere Sehnenstellen betreffen und während oder nach Abschluss der Therapie auftreten; Fälle, die bis zu mehrere Monate nach der Behandlung mit Fluorchinolonen auftraten, wurden berichtet. Vorsicht ist geboten, wenn FLOXIN® (Ofloxacin) älteren Patienten verschrieben wird, insbesondere solchen, die Kortikosteroide einnehmen. Die Patienten sollten über diese potenzielle Nebenwirkung informiert und angewiesen werden, FLOXIN® (Ofloxacin) abzusetzen und sich an ihren Arzt zu wenden, wenn Symptome einer Tendinitis oder eines Sehnenrisses auftreten (siehe Eingerahmte Warnung , WARNUNGEN , und NEBENWIRKUNGEN / Berichte über unerwünschte Ereignisse nach der Markteinführung ).
In klinischen Phase-2/3-Studien mit Ofloxacin waren 688 Patienten (14,2 %) ≥ 65 Jahre alt. Davon waren 436 Patienten (9,0 %) zwischen 65 und 74 Jahre alt und 252 Patienten (5,2 %) waren 75 Jahre oder älter. Es gab keinen offensichtlichen Unterschied in der Häufigkeit oder Schwere von Nebenwirkungen bei älteren Erwachsenen im Vergleich zu jüngeren Erwachsenen. Die pharmakokinetischen Eigenschaften von Ofloxacin bei älteren Patienten sind denen bei jüngeren Patienten ähnlich. Die Medikamentenabsorption scheint vom Alter unbeeinflusst zu sein. Bei älteren Patienten mit eingeschränkter Nierenfunktion (Kreatinin-Clearance-Rate ≤ 50 ml/min) ist aufgrund der reduzierten Clearance von Ofloxacin eine Dosisanpassung erforderlich. In Vergleichsstudien waren die Häufigkeit und Schwere der meisten arzneimittelbedingten Ereignisse im Nervensystem bei Patienten ≥ 65 Jahren für Ofloxacin und Kontrollarzneimittel vergleichbar. Die einzigen identifizierten Unterschiede waren eine Zunahme von Berichten über Schlaflosigkeit (3,9 % vs. 1,5 %) und Kopfschmerzen (4,7 % vs. 1,8 %) unter Ofloxacin. Es ist wichtig zu beachten, dass diese geriatrischen Sicherheitsdaten aus 44 Vergleichsstudien stammen, in denen die Informationen zu Nebenwirkungen von 20 verschiedenen Kontrollen (andere Antibiotika oder Placebo) zum Vergleich mit Ofloxacin gepoolt wurden. Die klinische Bedeutung eines solchen Vergleichs ist nicht klar. (Sehen KLINISCHE PHARMAKOLOGIE und DOSIERUNG UND ANWENDUNG .)
Ältere Patienten können empfindlicher auf arzneimittelbedingte Wirkungen auf das QT-Intervall reagieren. Daher sollte bei gleichzeitiger Anwendung von Ofloxacin mit Arzneimitteln, die zu einer Verlängerung des QT-Intervalls führen können (z. B. Klasse-IA- oder Klasse-III-Antiarrhythmika), oder bei Patienten mit Risikofaktoren für Torsade de pointes (z. B. bekannte QT-Verlängerung, unkorrigierte Hypokaliämie) Vorsicht walten. (Sehen VORSICHTSMASSNAHMEN : Allgemein : Torsade de pointes )
ÜBERDOSIS
Informationen zur Überdosierung von Ofloxacin sind begrenzt. Ein Vorfall einer versehentlichen Überdosierung wurde berichtet. In diesem Fall erhielt eine erwachsene Frau 3 Gramm Ofloxacin intravenös über 45 Minuten. Eine 15 Minuten nach Beendigung der Infusion entnommene Blutprobe ergab einen Ofloxacin-Spiegel von 39,3 μg/ml. In 7 h war der Spiegel auf 16,2 μg/ml und nach 24 h auf 2,7 μg/ml gefallen. Während der Infusion entwickelte der Patient Schläfrigkeit, Übelkeit, Schwindel, Hitze- und Kältewallungen, subjektive Gesichtsschwellungen und -taubheit, undeutliche Sprache und leichte bis mäßige Orientierungslosigkeit. Alle Beschwerden bis auf den Schwindel ließen innerhalb von 1 h nach Absetzen der Infusion nach. Der Schwindel, der beim Stehen am lästigsten war, verschwand in ungefähr 9 Stunden. Berichten zufolge ergaben Labortests bei diesem Patienten keine klinisch signifikanten Veränderungen der Routineparameter.
Im Falle einer akuten Überdosierung sollte der Magen entleert werden. Der Patient sollte beobachtet und für eine angemessene Flüssigkeitszufuhr gesorgt werden. Ofloxacin wird durch Hämodialyse oder Peritonealdialyse nicht effizient entfernt.
KONTRAINDIKATIONEN
FLOXIN® (Ofloxacin-Tabletten) Tabletten sind kontraindiziert bei Personen mit einer Vorgeschichte von Überempfindlichkeit im Zusammenhang mit der Anwendung von Ofloxacin oder einem Mitglied der antimikrobiellen Wirkstoffgruppe der Chinolone.
KLINISCHE PHARMAKOLOGIE
Nach oraler Verabreichung beträgt die Bioverfügbarkeit von Ofloxacin in der Tablettenform etwa 98 %. Maximale Serumkonzentrationen werden ein bis zwei Stunden nach einer oralen Dosis erreicht. Die Resorption von Ofloxacin nach Einzel- oder Mehrfachdosen von 200 bis 400 mg ist vorhersehbar, und die Menge des resorbierten Arzneimittels steigt proportional mit der Dosis. Ofloxacin hat eine zweiphasige Elimination. Nach mehrfacher oraler Gabe im Steady-State betragen die Halbwertszeiten etwa 4-5 Stunden und 20-25 Stunden. Die längere Halbwertszeit macht jedoch weniger als 5 % der gesamten AUC aus. Die Akkumulation im Steady State kann anhand einer Halbwertszeit von 9 Stunden abgeschätzt werden. Die Gesamtclearance und das Verteilungsvolumen sind nach Einzel- oder Mehrfachdosen ungefähr gleich. Die Elimination erfolgt hauptsächlich renal. Im Folgenden sind die mittleren maximalen Serumkonzentrationen bei gesunden männlichen Probanden mit einem Gewicht von 70–80 kg nach oraler Einzeldosis von 200, 300 oder 400 mg Ofloxacin oder nach oraler Mehrfachdosis von 400 mg aufgeführt.
Steady-State-Konzentrationen wurden nach vier oralen Dosen erreicht, und die Fläche unter der Kurve (AUC) war etwa 40 % höher als die AUC nach Einzeldosen. Daher werden nach mehrfacher Gabe von 200-mg- und 300-mg-Dosen maximale Serumspiegel von 2,2 μg/ml bzw. 3,6 μg/ml im Steady-State vorhergesagt.
In vitro sind etwa 32 % des Arzneimittels im Plasma proteingebunden.
Die Einzeldosis- und Steady-State-Plasmaprofile der Ofloxacin-Injektion waren im Ausmaß der Exposition (AUC) mit denen von Ofloxacin-Tabletten vergleichbar, wenn die injizierbare und die Tablettenformulierung von Ofloxacin in gleichen Dosen (mg/mg) an dieselbe Gruppe von Probanden verabreicht wurden . Die nach intravenöser Verabreichung von 400 mg über 60 Minuten erreichte mittlere Steady-State-AUC(0-12) betrug 43,5 μg•h/ml; die nach oraler Gabe von 400 mg erreichte mittlere AUC(0-12) im Steady State betrug 41,2 μg•h/ml (zwei einseitiger t-Test, 90 % Konfidenzintervall war 103-109). (Sehen folgendes Diagramm .)
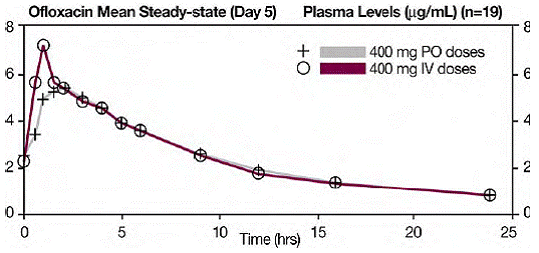
Zwischen 0 und 6 Stunden nach Verabreichung einer oralen Einzeldosis von 200 mg Ofloxacin an 12 gesunde Probanden betrug die durchschnittliche Ofloxacin-Konzentration im Urin etwa 220 μg/ml. Zwischen 12 und 24 Stunden nach der Verabreichung betrug der durchschnittliche Ofloxacin-Spiegel im Urin ungefähr 34 μg/ml.
Nach oraler Verabreichung der empfohlenen therapeutischen Dosen wurde Ofloxacin in Blasenflüssigkeit, Zervix, Lungengewebe, Eierstöcken, Prostataflüssigkeit, Prostatagewebe, Haut und Sputum nachgewiesen. Die mittlere Konzentration von Ofloxacin in jeder dieser verschiedenen Körperflüssigkeiten und Gewebe nach einer oder mehreren Dosen betrug das 0,8- bis 1,5-fache des gleichzeitigen Plasmaspiegels. Derzeit liegen nur unzureichende Daten zur Verteilung oder Konzentration von Ofloxacin in der Zerebrospinalflüssigkeit oder im Hirngewebe vor.
Ofloxacin hat einen Pyridobenzoxazinring, der das Ausmaß des Metabolismus der Ausgangsverbindung zu verringern scheint. Zwischen 65 % und 80 % einer verabreichten oralen Ofloxacin-Dosis werden innerhalb von 48 Stunden nach der Einnahme unverändert über die Nieren ausgeschieden. Studien zeigen, dass weniger als 5 % einer verabreichten Dosis als Desmethyl- oder N-Oxid-Metabolite im Urin wiedergefunden werden. Vier bis acht Prozent einer Ofloxacin-Dosis werden mit dem Stuhl ausgeschieden. Dies deutet auf eine geringe biliäre Ausscheidung von Ofloxacin hin.
Die Verabreichung von FLOXIN® (Ofloxacin) mit Nahrung hat keinen Einfluss auf Cmax und AUC∞ des Medikaments, aber Tmax wird verlängert.
Die Clearance von Ofloxacin ist bei Patienten mit eingeschränkter Nierenfunktion verringert (Kreatinin-Clearance-Rate ≤ 50 ml/min), und eine Dosisanpassung ist erforderlich. (Sehen VORSICHTSMASSNAHMEN : Allgemein und DOSIERUNG UND ANWENDUNG .)
Nach oraler Verabreichung an gesunde ältere Probanden (65-81 Jahre) werden die maximalen Plasmakonzentrationen normalerweise ein bis zwei Stunden nach einmaliger und mehrfacher zweimal täglicher Gabe erreicht, was darauf hindeutet, dass die Rate der oralen Resorption unabhängig von Alter oder Geschlecht ist. Die mittleren maximalen Plasmakonzentrationen bei älteren Probanden waren 9-21 % höher als die bei jüngeren Probanden beobachteten. Geschlechtsspezifische Unterschiede in den pharmakokinetischen Eigenschaften älterer Patienten wurden beobachtet. Die maximalen Plasmakonzentrationen waren bei älteren Frauen um 114 % bzw. 54 % höher als bei älteren Männern nach einmaliger und mehrfacher zweimal täglicher Gabe. [Diese Interpretation basierte auf Studienergebnissen aus zwei getrennten Studien.] Die Plasmakonzentrationen steigen dosisabhängig mit steigender Dosis nach oraler Einzeldosis und im Steady State. Bei den Werten des Verteilungsvolumens wurden keine Unterschiede zwischen älteren und jüngeren Probanden beobachtet. Wie bei jüngeren Probanden erfolgt die Elimination bei älteren Probanden hauptsächlich über die renale Ausscheidung als unveränderter Wirkstoff, obwohl bei älteren Probanden weniger Wirkstoff aus der renalen Ausscheidung wiedergefunden wird. Wie bei jüngeren Probanden wurden bei älteren Patienten weniger als 5 % einer verabreichten Dosis als Desmethyl- und N-Oxid-Metabolite im Urin wiedergefunden. Bei älteren Probanden wurde eine längere Plasmahalbwertszeit von etwa 6,4 bis 7,4 Stunden beobachtet, verglichen mit 4 bis 5 Stunden bei jungen Probanden. Bei älteren Personen wird im Vergleich zu jüngeren Personen eine langsamere Elimination von Ofloxacin beobachtet, was möglicherweise auf die bei älteren Personen beobachtete reduzierte Nierenfunktion und renale Clearance zurückzuführen ist. Da bekannt ist, dass Ofloxacin im Wesentlichen über die Nieren ausgeschieden wird und ältere Patienten eher eine eingeschränkte Nierenfunktion haben, ist eine Dosisanpassung für ältere Patienten mit eingeschränkter Nierenfunktion erforderlich, wie für alle Patienten empfohlen. (Sehen VORSICHTSMASSNAHMEN : Allgemein und DOSIERUNG UND ANWENDUNG .)
Mikrobiologie
Ofloxacin ist ein Chinolon-Antibiotikum. Der Wirkungsmechanismus von Ofloxacin und anderen Fluorchinolon-Antimikrobiotika umfasst die Hemmung der bakteriellen Topoisomerase IV und der DNA-Gyrase (beide Topoisomerasen vom Typ II), Enzyme, die für die DNA-Replikation, -Transkription, -Reparatur und -Rekombination erforderlich sind.
Ofloxacin hat eine In-vitro-Aktivität gegen ein breites Spektrum gramnegativer und grampositiver Mikroorganismen. Ofloxacin wirkt oft bakterizid bei Konzentrationen, die gleich oder geringfügig höher als die inhibitorischen Konzentrationen sind.
Fluorchinolone, einschließlich Ofloxacin, unterscheiden sich in chemischer Struktur und Wirkungsweise von Aminoglykosiden, Makroliden und β-Lactam-Antibiotika, einschließlich Penicillinen. Fluorchinolone können daher gegen Bakterien wirksam sein, die gegen diese antimikrobiellen Mittel resistent sind.
Eine Resistenz gegenüber Ofloxacin aufgrund einer spontanen Mutation in vitro tritt selten auf (Bereich: 10-9 bis 10-11). Obwohl eine Kreuzresistenz zwischen Ofloxacin und einigen anderen Fluorchinolonen beobachtet wurde, können einige Mikroorganismen, die gegen andere Fluorchinolone resistent sind, gegenüber Ofloxacin empfindlich sein.
Ofloxacin hat sich sowohl in vitro als auch bei klinischen Infektionen als wirksam gegen die meisten Stämme der folgenden Mikroorganismen erwiesen, wie in beschrieben INDIKATIONEN UND VERWENDUNG Abschnitt:
Aerobe Gram-positive Mikroorganismen
Staphylococcus aureus (Methicillin-empfindliche Stämme) Streptococcus pneumoniae (Penicillin-empfindliche Stämme) Streptococcus pyogenes
Aerobe Gram-negative Mikroorganismen
Citrobacter (diversus) koseri Enterobacter aerogenes Escherichia coli Haemophilus influenzae Klebsiella pneumoniae Neisseria gonorrhoeae Proteus mirabilis Pseudomonas aeruginosa
Wie bei anderen Arzneimitteln dieser Klasse können einige Stämme von Pseudomonas aeruginosa während der Behandlung mit Ofloxacin ziemlich schnell Resistenzen entwickeln.
Andere Mikroorganismen
Chlamydia trachomatis
Die folgenden In-vitro-Daten sind verfügbar, ihre klinische Bedeutung ist jedoch nicht bekannt.
Ofloxacin weist in vitro minimale Hemmkonzentrationen (MHK-Werte) von 2 μg/ml oder weniger gegen die meisten (≥ 90 %) Stämme der folgenden Mikroorganismen auf; Die Sicherheit und Wirksamkeit von Ofloxacin bei der Behandlung klinischer Infektionen durch diese Mikroorganismen wurden jedoch nicht in angemessenen und gut kontrollierten Studien nachgewiesen.
Aerobe Gram-positive Mikroorganismen
Staphylococcus epidermidis (Methicillin-empfindliche Stämme) Staphylococcus saprophyticus Streptococcus pneumoniae (Penicillin-resistente Stämme)
Aerobe Gram-negative Mikroorganismen
Acinetobacter calcoaceticus Bordetella pertussis Citrobacter freundii Enterobacter cloacae Haemophilus ducreyi Klebsiella oxytoca Moraxella catarrhalis Morganella morganii Proteus vulgaris Providencia rettgeri Providencia stuartii Serratia marcescens
Anaerobe Mikroorganismen
Clostridium perfringes
Andere Mikroorganismen
Chlamydia pneumoniae Gardnerella vaginalis Legionella pneumophila Mycoplasma hominis Mycoplasma pneumoniae Ureaplasma urealyticum
Ofloxacin ist nicht wirksam gegen Treponema pallidum (vgl WARNUNGEN .)
Viele Stämme anderer Streptokokkenarten, Enterococcus-Arten und Anaerobier sind gegen Ofloxacin resistent.
Empfindlichkeitstests
Verdünnungstechniken
Zur Bestimmung der minimalen Hemmkonzentrationen (MHK-Werte) antimikrobieller Mittel werden quantitative Methoden eingesetzt. Diese MHK-Werte liefern Schätzungen der Empfindlichkeit von Bakterien gegenüber antimikrobiellen Verbindungen. Die MHK-Werte sollten nach einem standardisierten Verfahren bestimmt werden. Standardisierte Verfahren basieren auf einer Verdünnungsmethode1 (Brühe oder Agar) oder gleichwertig mit standardisierten Inokulumkonzentrationen und standardisierten Konzentrationen von Ofloxacin-Pulver. Die MHK-Werte sollten nach folgenden Kriterien interpretiert werden:
Zum Testen von Enterobacteriaceae, Methicillin-empfindlichen Staphylococcus aureus und Pseudomonas aeruginosa:
Zum Testen von Haemophilus influenzae:a
a Dieser Interpretationsstandard gilt nur für Mikrodilutions-Bouillon-Empfindlichkeitstests mit Haemophilus influenzae unter Verwendung von Haemophilus-Testmedium1
Das derzeitige Fehlen von Daten zu resistenten Stämmen schließt es aus, andere Ergebnisse als „anfällig“ zu definieren. Stämme mit MHK-Ergebnissen, die auf eine „nicht empfindliche“ Kategorie hindeuten, sollten für weitere Tests an ein Referenzlabor geschickt werden.
Zum Testen von Neisseria gonorrhoeae:b
b Diese Interpretationsstandards gelten nur für Agar-Verdünnungstests unter Verwendung von GC-Agarbasis und 1 % definiertem Wachstumszusatz, inkubiert in 5 % CO2.
Zum Testen von Streptococcus pneumoniae und Streptococcus pyogenes:c
c Diese Interpretationsstandards gelten nur für Mikroverdünnungs-Bouillon-Empfindlichkeitstests unter Verwendung von kationenadjustierter Mueller-Hinton-Bouillon mit 2-5 % lysiertem Pferdeblut.
Ein Bericht „anfällig“ weist darauf hin, dass der Erreger wahrscheinlich gehemmt wird, wenn die antimikrobielle Verbindung im Blut die normalerweise erreichbare Konzentration erreicht. Ein Bericht mit „Zwischenergebnis“ weist darauf hin, dass das Ergebnis als zweideutig betrachtet werden sollte und der Test wiederholt werden sollte, wenn der Mikroorganismus nicht vollständig empfindlich gegenüber alternativen, klinisch geeigneten Arzneimitteln ist. Diese Kategorie impliziert eine mögliche klinische Anwendbarkeit an Körperstellen, an denen das Arzneimittel physiologisch konzentriert ist, oder in Situationen, in denen eine hohe Arzneimitteldosis verwendet werden kann. Diese Kategorie bietet auch eine Pufferzone, die verhindert, dass kleine unkontrollierte technische Faktoren zu großen Diskrepanzen bei der Interpretation führen. Ein Bericht „resistent“ weist darauf hin, dass der Erreger wahrscheinlich nicht gehemmt wird, wenn die antimikrobielle Verbindung im Blut die normalerweise erreichbare Konzentration erreicht; andere Therapie gewählt werden.
Standardisierte Empfindlichkeitstestverfahren erfordern die Verwendung von Laborkontrollmikroorganismen, um die technischen Aspekte der Laborverfahren zu kontrollieren. Standard-Ofloxacin-Pulver sollte die folgenden MHK-Werte aufweisen:
Diffusionstechniken
Quantitative Methoden, die die Messung von Zonendurchmessern erfordern, liefern auch reproduzierbare Schätzungen der Empfindlichkeit von Bakterien gegenüber antimikrobiellen Verbindungen. Ein solches standardisiertes Verfahren2 erfordert die Verwendung standardisierter Inokulumkonzentrationen. Bei diesem Verfahren werden mit 5 μg Ofloxacin imprägnierte Papierscheiben verwendet, um die Empfindlichkeit von Mikroorganismen gegenüber Ofloxacin zu testen.
Berichte des Labors, die Ergebnisse des standardmäßigen Einzelscheiben-Empfindlichkeitstests mit einem 5-μg-Ofloxacin-Blättchen liefern, sollten gemäß den folgenden Kriterien interpretiert werden:
Zum Testen von Enterobacteriaceae, Methicillin-empfindlichen Staphylococcus aureus und Pseudomonas aeruginosa:
Zum Testen von Haemophilus influenzae:g
Dieser Zonendurchmesser-Standard gilt nur für Scheibendiffusionstests mit Haemophilus influenzae unter Verwendung von Haemophilus-Testmedium (HTM)2, inkubiert in 5 % CO2.
Das derzeitige Fehlen von Daten zu resistenten Stämmen schließt es aus, andere Ergebnisse als „anfällig“ zu definieren. Stämme, deren Zonendurchmesserergebnisse auf eine Kategorie „nicht empfindlich“ hindeuten, sollten zur weiteren Prüfung an ein Referenzlabor geschickt werden.
Zum Testen von Neisseria gonorrhoeae: h
h Diese Zonendurchmesser-Standards gelten nur für Scheibendiffusionstests unter Verwendung von GC-Agarbasis und 1 % definiertem Wachstumszusatz, inkubiert in 5 % CO2
Zum Testen von Streptococcus pneumoniae und Streptococcus pyogenes:i
i Diese Zonendurchmesser-Standards gelten nur für Blättchendiffusionstests, die mit Mueller-Hinton-Agar durchgeführt werden, der mit 5 % defibriniertem Schafblut ergänzt und in 5 % CO2 inkubiert wird.
Die Interpretation sollte wie oben für Ergebnisse mit Verdünnungstechniken angegeben erfolgen. Die Interpretation umfasst die Korrelation des im Scheibentest erhaltenen Durchmessers mit der MHK für Ofloxacin.
Wie bei standardisierten Verdünnungstechniken erfordern Diffusionsmethoden die Verwendung von Laborkontrollmikroorganismen, die verwendet werden, um die technischen Aspekte der Laborverfahren zu kontrollieren. Für die Diffusionstechnik sollte die 5-μg-Ofloxacin-Scheibe die folgenden Zonendurchmesser in diesen Labor-Qualitätskontrollstämmen aufweisen:
Tierpharmakologie
Es wurde gezeigt, dass Ofloxacin, wie auch andere Arzneimittel der Klasse der Chinolone, Arthropathien (Arthrose) bei unreifen Hunden und Ratten verursacht. Außerdem sind diese Arzneimittel mit einem erhöhten Auftreten von Osteochondrose bei Ratten im Vergleich zu dem bei mit Vehikel behandelten Ratten beobachteten Auftreten verbunden. (Sehen WARNUNGEN .) Es gibt keine Hinweise auf Arthropathien bei ausgewachsenen Hunden bei intravenösen Dosen bis zum 3-fachen der empfohlenen maximalen Humandosis (auf mg/m²-Basis oder 5-fach auf mg/kg-Basis) über einen einwöchigen Expositionszeitraum.
Langfristige, hochdosierte systemische Anwendung anderer Chinolone bei Versuchstieren hat Linsentrübungen verursacht; dieser Befund wurde jedoch in keinem Tierversuch mit Ofloxacin beobachtet.
Bei Tieren, die mit anderen Chinolonen behandelt wurden, wurden verringerte Serumglobulin- und Proteinspiegel beobachtet. In einer Ofloxacin-Studie wurde bei weiblichen Cynomolgus-Affen, die ein Jahr lang täglich 40 mg/kg Ofloxacin oral verabreicht bekamen, eine geringfügige Abnahme der Serumglobulin- und -proteinspiegel festgestellt. Diese Veränderungen wurden jedoch als innerhalb normaler Grenzen für Affen liegend angesehen.
Kristallurie und Augentoxizität wurden bei keinem der mit Ofloxacin behandelten Tiere beobachtet.
VERWEISE
1. Nationales Komitee für klinische Laborstandards. Methoden zur Verdünnung Antibiotika-Empfindlichkeitstests für Bakterien, die aerob wachsen - Vierte Auflage. Genehmigtes Standard-NCCLS-Dokument M7-A4, Vol. 17, Nr. 2, NCCLS, Wayne, PA, Januar 1997.
2. Nationales Komitee für klinische Laborstandards. Leistungsstandards für Anfälligkeitstests für antimikrobielle Datenträger – Sechste Ausgabe. Genehmigtes Standard-NCCLS-Dokument M2-A6, Vol. 17, Nr. 1, NCCLS, Wayne, PA, Januar 1997.
INFORMATIONEN ZUM PATIENTEN
ARZNEIMITTEL-LEITFADEN
FLOXIN® [Floxin] (Ofloxacin)
Lesen Sie den mit FLOXIN® (Ofloxacin) gelieferten Medikationsleitfaden, bevor Sie mit der Einnahme beginnen und jedes Mal, wenn Sie eine Nachfüllung erhalten. Möglicherweise gibt es neue Informationen. Dieser Medikationsleitfaden ersetzt nicht das Gespräch mit Ihrem Gesundheitsdienstleister über Ihren Gesundheitszustand oder Ihre Behandlung.
Was sind die wichtigsten Informationen, die ich über FLOXIN® (Ofloxacin) wissen sollte?
FLOXIN® (Ofloxacin) gehört zu einer Klasse von Antibiotika, die Fluorchinolone genannt werden. FLOXIN® (Ofloxacin) kann Nebenwirkungen verursachen, die schwerwiegend sein oder sogar zum Tod führen können. Wenn Sie eine der folgenden schwerwiegenden Nebenwirkungen bemerken, suchen Sie sofort medizinische Hilfe auf. Sprechen Sie mit Ihrem Arzt darüber, ob Sie FLOXIN® (Ofloxacin) weiterhin einnehmen sollten.
Siehe den Abschnitt „ Welche Nebenwirkungen kann FLOXIN® (Ofloxacin) haben? “ für weitere Informationen zu Nebenwirkungen.
Was ist FLOXIN® (Ofloxacin)?
FLOXIN® (Ofloxacin) ist ein Fluorchinolon-Antibiotikum, das bei Erwachsenen zur Behandlung bestimmter Infektionen angewendet wird, die durch bestimmte Keime, sogenannte Bakterien, verursacht werden. Es ist nicht bekannt, ob FLOXIN® (Ofloxacin) sicher ist und bei Personen unter 18 Jahren wirkt. Kinder unter 18 Jahren haben ein höheres Risiko, während der Einnahme von FLOXIN® (Ofloxacin) Probleme mit Knochen, Gelenken oder Sehnen (Muskel-Skelett-System) wie Schmerzen oder Schwellungen zu bekommen.
Manchmal werden Infektionen eher durch Viren als durch Bakterien verursacht. Beispiele hierfür sind virale Infektionen der Nasennebenhöhlen und der Lunge, wie z. B. Erkältung oder Grippe. Antibiotika einschließlich FLOXIN® (Ofloxacin) töten Viren nicht ab.
Rufen Sie Ihren Arzt an, wenn Sie glauben, dass sich Ihr Zustand während der Einnahme von FLOXIN® (Ofloxacin) nicht bessert.
Wer sollte FLOXIN® (Ofloxacin) nicht einnehmen?
Nehmen Sie FLOXIN® (Ofloxacin) nicht ein, wenn Sie jemals eine schwere allergische Reaktion auf ein als Fluorchinolon bekanntes Antibiotikum hatten oder wenn Sie allergisch gegen einen der Inhaltsstoffe von FLOXIN® (Ofloxacin) sind. Fragen Sie Ihren Arzt, wenn Sie sich nicht sicher sind. Siehe die Liste der Inhaltsstoffe von FLOXIN® (Ofloxacin) am Ende dieses Arzneimittelleitfadens.
Was sollte ich meinem Arzt vor der Einnahme von FLOXIN® (Ofloxacin) mitteilen?
Sehen " Was sind die wichtigsten Informationen, die ich über FLOXIN® (Ofloxacin) wissen sollte? ”
Informieren Sie Ihren Arzt über alle Ihre Erkrankungen, auch wenn Sie:
Informieren Sie Ihren Arzt über alle Arzneimittel, die Sie einnehmen, einschließlich verschreibungspflichtiger und nicht verschreibungspflichtiger Arzneimittel, Vitamine, Kräuter- und Nahrungsergänzungsmittel. FLOXIN® (Ofloxacin) und andere Arzneimittel können sich gegenseitig beeinflussen und Nebenwirkungen verursachen. Informieren Sie Ihren Arzt insbesondere, wenn Sie Folgendes einnehmen:
Fragen Sie Ihren Arzt, wenn Sie sich nicht sicher sind, ob eines Ihrer Arzneimittel oben aufgeführt ist.
Informieren Sie sich über die Medikamente, die Sie einnehmen. Führen Sie eine Liste Ihrer Arzneimittel und zeigen Sie diese Ihrem Arzt und Apotheker, wenn Sie ein neues Arzneimittel erhalten.
Wie sollte ich FLOXIN® (Ofloxacin) einnehmen?
Was sollte ich während der Einnahme von FLOXIN® (Ofloxacin) vermeiden?
Welche Nebenwirkungen kann FLOXIN® (Ofloxacin) haben?
FLOXIN® (Ofloxacin) kann Nebenwirkungen verursachen, die schwerwiegend sein oder sogar zum Tod führen können. Sehen " Was sind die wichtigsten Informationen, die ich über FLOXIN® (Ofloxacin) wissen sollte? ”
Weitere schwerwiegende Nebenwirkungen von FLOXIN® (Ofloxacin) sind:
FLOXIN® (Ofloxacin) kann zu falsch-positiven Urin-Screening-Ergebnissen für Opiate führen, wenn Tests mit einigen im Handel erhältlichen Kits durchgeführt werden. Ein positives Ergebnis sollte mit einem spezifischeren Test bestätigt werden.
Dies sind nicht alle möglichen Nebenwirkungen von FLOXIN® (Ofloxacin). Informieren Sie Ihren Arzt über jede Nebenwirkung, die Sie stört oder die nicht abklingt.
Rufen Sie Ihren Arzt für medizinischen Rat zu Nebenwirkungen an. Sie können Nebenwirkungen der FDA unter 1-800-FDA-1088 melden.
Wie soll ich FLOXIN® (Ofloxacin) aufbewahren?
Allgemeine Informationen zu FLOXIN® (Ofloxacin)
Medikamente werden manchmal für andere als die in einem Medikationsleitfaden aufgeführten Zwecke verschrieben. Verwenden Sie FLOXIN® (Ofloxacin) nicht für einen Zustand, für den es nicht verschrieben ist. Geben Sie FLOXIN® (Ofloxacin) nicht an andere Personen, selbst wenn sie die gleichen Symptome wie Sie haben. Es kann ihnen schaden.
Dieser Arzneimittelratgeber fasst die wichtigsten Informationen zu FLOXIN® (Ofloxacin) zusammen. Wenn Sie weitere Informationen über FLOXIN® (Ofloxacin) wünschen, sprechen Sie mit Ihrem Arzt. Sie können Ihren Arzt oder Apotheker um Informationen über FLOXIN® (Ofloxacin) bitten, die für medizinisches Fachpersonal geschrieben sind. Weitere Informationen erhalten Sie telefonisch unter 1-800-526-7736.
Welche Inhaltsstoffe enthält FLOXIN®?