Procardia 30mg Nifedipine Verwendung, Nebenwirkungen, Stärke und Dosierung. Preis in Online-Apotheke. Generika medikamente rezeptfrei.
Was ist Procardia 30 mg und wie wird es angewendet?
Procardia ist ein verschreibungspflichtiges Arzneimittel zur Behandlung der Symptome von Brustschmerzen (Angina pectoris), Bluthochdruck (Hypertonie) und pulmonaler Hypertonie. Procardia 30 mg kann allein oder zusammen mit anderen Medikamenten verwendet werden.
Procardia gehört zu einer Klasse von Arzneimitteln, die Kalziumkanalblocker genannt werden; Kalziumkanalblocker, Dihydrophyridin.
Es ist nicht bekannt, ob Procardia bei Kindern sicher und wirksam ist.
Welche Nebenwirkungen kann Procardia haben?
Prokardie kann schwerwiegende Nebenwirkungen verursachen, einschließlich:
Suchen Sie sofort medizinische Hilfe auf, wenn Sie eines der oben aufgeführten Symptome haben.
Zu den häufigsten Nebenwirkungen von Procardia 30 mg gehören:
Teilen Sie dem Arzt mit, wenn Sie eine Nebenwirkung haben, die Sie stört oder die nicht abklingt.
Dies sind nicht alle möglichen Nebenwirkungen von Procardia. Für weitere Informationen fragen Sie Ihren Arzt oder Apotheker.
BEZEICHNUNG
PROCARDIA® (Nifedipin) ist ein antianginöses Medikament, das zu einer Klasse pharmakologischer Wirkstoffe, den Kalziumkanalblockern, gehört. Nifedipin ist 3,5-Pyridindicarbonsäure, 1,4-Dihydro-2,6-dimethyl-4-(2-nitrophenyl)-, dimethylester, C17H18N2O6, und hat die Strukturformel:
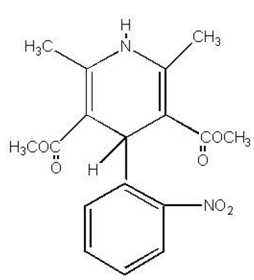
Nifedipin ist eine gelbe kristalline Substanz, praktisch unlöslich in Wasser, aber löslich in Ethanol. Es hat ein Molekulargewicht von 346,3. PROCARDIA-Kapseln sind als Weichgelatinekapseln zur oralen Verabreichung formuliert, die jeweils 10 mg Nifedipin enthalten.
Inerte Inhaltsstoffe in der Formulierung sind: Glycerin; Pfefferminz Öl; Polyethylenglycol; Weichgelatinekapseln (die Yellow 6 enthalten und rotes Eisenoxid und andere inerte Inhaltsstoffe enthalten können); und Wasser. Die 10-mg-Kapseln enthalten außerdem Saccharin-Natrium.
INDIKATIONEN
Vasospastische Angina
PROCARDIA (Nifedipin) ist indiziert zur Behandlung von vasospastischer Angina pectoris, bestätigt durch eines der folgenden Kriterien: 1) klassisches Anginamuster in Ruhe, begleitet von einer ST-Strecken-Hebung, 2) durch Ergonovin hervorgerufene Angina pectoris oder Koronararterienspasmus, oder 3) angiographisch nachgewiesen Koronararterienkrampf. Bei Patienten, die sich einer Angiographie unterzogen haben, ist das Vorhandensein einer signifikanten fixierten obstruktiven Erkrankung nicht unvereinbar mit der Diagnose einer vasospastischen Angina, vorausgesetzt, dass die oben genannten Kriterien erfüllt sind. PROCARDIA 30 mg kann auch verwendet werden, wenn das klinische Erscheinungsbild auf eine mögliche vasospastische Komponente hindeutet, aber wenn ein Vasospasmus nicht bestätigt wurde, z. B. wenn der Schmerz eine variable Schwelle bei Anstrengung hat oder wenn Angina auf Nitrate und/oder adäquate Dosen von Betablockern nicht anspricht.
Chronisch stabile Angina pectoris (klassische anstrengungsassoziierte Angina pectoris)
PROCARDIA 30 mg ist indiziert zur Behandlung von chronisch stabiler Angina (anstrengungsassoziierte Angina) ohne Anzeichen von Vasospasmus bei Patienten, die trotz angemessener Dosen von Betablockern und/oder organischen Nitraten symptomatisch bleiben oder diese Mittel nicht vertragen.
Bei chronisch stabiler Angina (anstrengungsassoziierte Angina) war PROCARDIA in kontrollierten Studien mit einer Dauer von bis zu acht Wochen bei der Verringerung der Angina-Häufigkeit und der Erhöhung der Belastungstoleranz wirksam, aber die Bestätigung der anhaltenden Wirksamkeit und die Bewertung der langfristigen Sicherheit bei diesen Patienten sind unvollständig .
Kontrollierte Studien mit einer kleinen Anzahl von Patienten deuten darauf hin, dass die gleichzeitige Anwendung von PROCARDIA 30 mg und Betablockern bei Patienten mit chronisch stabiler Angina pectoris von Vorteil sein kann, aber die verfügbaren Informationen reichen nicht aus, um die Auswirkungen einer gleichzeitigen Behandlung zuverlässig vorherzusagen, insbesondere bei Patienten mit eingeschränkter linksventrikulärer Funktion oder Herzleitungsstörungen. Bei Einleitung einer solchen Begleittherapie muss der Blutdruck engmaschig überwacht werden, da es durch die kombinierten Wirkungen der Arzneimittel zu einer schweren Hypotonie kommen kann. (Sehen WARNUNGEN .)
DOSIERUNG UND ANWENDUNG
Die Dosierung von PROCARDIA 30 mg, die zur Unterdrückung von Angina benötigt wird und vom Patienten toleriert werden kann, muss durch Titration ermittelt werden. Zu hohe Dosen können zu Hypotonie führen.
Die Therapie sollte mit der 10-mg-Kapsel begonnen werden. Die Anfangsdosis beträgt eine 10-mg-Kapsel, die dreimal täglich unzerkaut geschluckt wird. Der übliche wirksame Dosisbereich beträgt 10–20 mg dreimal täglich. Einige Patienten, insbesondere solche mit Anzeichen von Koronararterienspasmen, sprechen nur auf höhere Dosen, häufigere Verabreichung oder beides an. Bei solchen Patienten können Dosen von 20–30 mg drei- oder viermal täglich wirksam sein. Dosen über 120 mg täglich sind selten erforderlich. Mehr als 180 mg pro Tag werden nicht empfohlen.
In den meisten Fällen sollte die Titration von PROCARDIA über einen Zeitraum von 7–14 Tagen erfolgen, damit der Arzt das Ansprechen auf jede Dosisstufe beurteilen und den Blutdruck überwachen kann, bevor er mit höheren Dosen fortfährt.
Wenn die Symptome dies rechtfertigen, kann die Titration schneller erfolgen, vorausgesetzt, der Patient wird häufig untersucht. Basierend auf der körperlichen Aktivität des Patienten, der Attackenhäufigkeit und dem sublingualen Nitroglycerinverbrauch kann die Dosis von PROCARDIA 30 mg von 10 mg 3-mal täglich auf 20 mg 3-mal täglich und dann auf 30 mg 3-mal täglich über einen Zeitraum von drei Tagen erhöht werden.
Bei Krankenhauspatienten unter engmaschiger Überwachung kann die Dosis je nach Bedarf in 10-mg-Schritten über vier bis sechs Stunden erhöht werden, um Schmerzen und Arrhythmien aufgrund von Ischämie zu kontrollieren. Eine Einzeldosis sollte 30 mg selten überschreiten.
Vermeiden Sie die gleichzeitige Anwendung von Nifedipin mit Grapefruitsaft (siehe KLINISCHE PHARMAKOLOGIE und WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN ).
Nach Absetzen von PROCARDIA wurde kein „Rebound-Effekt“ beobachtet. Wenn jedoch ein Absetzen von PROCARDIA erforderlich ist, empfiehlt die solide klinische Praxis, die Dosis unter engmaschiger ärztlicher Überwachung schrittweise zu verringern.
Gleichzeitige Verabreichung mit anderen antianginösen Arzneimitteln
Sublinguales Nitroglyzerin kann bei Bedarf zur Kontrolle akuter Manifestationen von Angina, insbesondere während der Titration von PROCARDIA, eingenommen werden. Sehen WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN , für Informationen zur gleichzeitigen Anwendung von PROCARDIA 30 mg mit Betablockern oder langwirksamen Nitraten.
WIE GELIEFERT
PROCARDIA Weichgelatinekapseln sind erhältlich in:
100er-Flaschen: 10 mg ( NDC 0069-2600-66)
Die Kapseln sollten vor Licht und Feuchtigkeit geschützt und bei kontrollierter Raumtemperatur, 59° bis 77°F (15° bis 25°C) in der Originalverpackung des Herstellers gelagert werden.
Vertrieb durch: Pfizer Labs, Division of Pfizer Inc, NY, NY 10017. Überarbeitet: Juli 2016
NEBENWIRKUNGEN
In kontrollierten Mehrfachdosisstudien in den Vereinigten Staaten und im Ausland, in denen Nebenwirkungen spontan berichtet wurden, traten Nebenwirkungen häufig auf, waren aber im Allgemeinen nicht schwerwiegend und erforderten selten einen Therapieabbruch oder eine Dosisanpassung. Die meisten waren erwartete Folgen der gefäßerweiternden Wirkung von PROCARDIA.
Es gibt auch eine große unkontrollierte Erfahrung mit über 2100 Patienten in den Vereinigten Staaten. Die meisten Patienten litten an vasospastischer oder resistenter Angina pectoris, und etwa die Hälfte wurde gleichzeitig mit betaadrenergen Blockern behandelt. Die häufigsten Nebenwirkungen waren:
Inzidenz ca. 10 %
Herz-Kreislauf: periphere Ödeme
Zentrales Nervensystem: Schwindel oder Benommenheit
Magen-Darm: Brechreiz
Systemisch: Kopfschmerzen und Hitzewallungen, Schwäche
Inzidenz ca. 5 %
Herz-Kreislauf: vorübergehende Hypotonie
Inzidenz 2 % oder weniger
Herz-Kreislauf: Herzklopfen
Atmung: verstopfte Nase und Brustkorb, Kurzatmigkeit
Magen-Darm: Durchfall, Verstopfung, Krämpfe, Blähungen
Bewegungsapparat: Entzündung, Gelenksteifheit, Muskelkrämpfe
Zentrales Nervensystem: Zittern, Nervosität, Nervosität, Schlafstörungen, verschwommenes Sehen, Gleichgewichtsstörungen
Sonstiges: Dermatitis, Pruritus, Urtikaria, Fieber, Schwitzen, Schüttelfrost, sexuelle Schwierigkeiten
Inzidenz ca. 0,5 %
Herz-Kreislauf: Synkope (meist bei Initialdosierung und/oder Dosissteigerung), Erythromelalgie
Inzidenz weniger als 0,5 %
Hämatologisch: Thrombozytopenie, Anämie, Leukopenie, Purpura
Magen-Darm: allergische Hepatitis
Gesicht und Hals: Angioödem (meist oropharyngeales Ödem mit Atembeschwerden bei einigen Patienten), Gingivahyperplasie
ZNS: Depressionen, paranoides Syndrom
Besondere Sinne: vorübergehende Erblindung auf dem Höhepunkt des Plasmaspiegels, Tinnitus
Urogenital: Nykturie, Polyurie
Sonstiges: Arthritis mit ANA (+), exfoliative Dermatitis, Gynäkomastie
Bewegungsapparat: Myalgie
Einige dieser Nebenwirkungen scheinen dosisabhängig zu sein. Periphere Ödeme traten bei etwa einem von 25 Patienten bei Dosen von weniger als 60 mg pro Tag und bei etwa einem von acht Patienten bei Dosen von 120 mg pro Tag oder mehr auf. Vorübergehende Hypotonie, die im Allgemeinen von leichter bis mäßiger Schwere war und selten ein Absetzen der Therapie erforderte, trat bei einem von 50 Patienten mit weniger als 60 mg pro Tag und bei einem von 20 Patienten mit 120 mg pro Tag oder mehr auf.
Sehr selten war die Einleitung einer Therapie mit PROCARDIA 30 mg mit einer Zunahme der Angina pectoris verbunden, möglicherweise aufgrund einer damit verbundenen Hypotonie. Vorübergehender einseitiger Sehverlust ist ebenfalls aufgetreten.
Darüber hinaus wurden bei diesen Patienten schwerwiegendere unerwünschte Ereignisse beobachtet, die nicht ohne weiteres vom natürlichen Krankheitsverlauf zu unterscheiden waren. Es bleibt jedoch möglich, dass einige oder viele dieser Ereignisse drogenbedingt waren. Ein Myokardinfarkt trat bei etwa 4 % der Patienten und eine dekompensierte Herzinsuffizienz oder ein Lungenödem bei etwa 2 % auf. Ventrikuläre Arrhythmien oder Überleitungsstörungen traten jeweils bei weniger als 0,5 % der Patienten auf.
In einer Untergruppe von über 1000 Patienten, die 30 mg PROCARDIA zusammen mit einer Betablocker-Therapie erhielten, unterschieden sich das Muster und die Häufigkeit von Nebenwirkungen nicht von denen der gesamten Gruppe der mit PROCARDIA (Nifedipin) behandelten Patienten. (Sehen VORSICHTSMASSNAHMEN .)
In einer Untergruppe von etwa 250 Patienten mit der Diagnose dekompensierter Herzinsuffizienz sowie Angina pectoris (etwa 10 % der gesamten Patientenpopulation) traten bei jeweils einem von acht Patienten Schwindel oder Benommenheit, periphere Ödeme, Kopfschmerzen oder Hitzewallungen auf. Hypotonie trat bei etwa einem von 20 Patienten auf. Eine Synkope trat bei etwa einem von 250 Patienten auf. Ein Myokardinfarkt oder Symptome einer dekompensierten Herzinsuffizienz traten jeweils bei etwa einem von 15 Patienten auf. Vorhof- oder ventrikuläre Rhythmusstörungen traten jeweils bei etwa einem von 150 Patienten auf.
Nach der Markteinführung gab es seltene Berichte über durch Nifedipin verursachte exfoliative Dermatitis. Es gab seltene Berichte über Nebenwirkungen von exfoliativer oder bullöser Haut (wie Erythema multiforme, Stevens-Johnson-Syndrom und toxische epidermale Nekrolyse) und Lichtempfindlichkeitsreaktionen. Akute generalisierte exanthematische Pustulose wurde ebenfalls berichtet.
WECHSELWIRKUNGEN MIT ANDEREN MEDIKAMENTEN
Beta-adrenerge Blocker
(Sehen INDIKATIONEN UND VERWENDUNG und WARNUNGEN .) Erfahrungen mit über 1400 Patienten in einer nicht vergleichenden klinischen Studie haben gezeigt, dass die gleichzeitige Verabreichung von PROCARDIA 30 mg und Betablockern normalerweise gut vertragen wird, aber es gab gelegentlich Literaturberichte, die darauf hindeuten, dass die Kombination die Wahrscheinlichkeit einer dekompensierten Herzinsuffizienz erhöhen kann. schwere Hypotonie oder Exazerbation einer Angina pectoris.
Lang wirkende Nitrate
PROCARDIA 30 mg kann sicher zusammen mit Nitraten verabreicht werden, es wurden jedoch keine kontrollierten Studien zur Bewertung der antianginösen Wirksamkeit dieser Kombination durchgeführt.
Digitalis
Da vereinzelt über Patienten mit erhöhten Digoxinspiegeln berichtet wurde und da eine mögliche Wechselwirkung zwischen Digoxin und Nifedipin besteht, wird empfohlen, die Digoxinspiegel zu Beginn, bei der Anpassung und beim Absetzen von Nifedipin zu überwachen, um eine mögliche Über- oder Unterdigitalisierung zu vermeiden .
Chinidin
Es gab seltene Berichte über eine Wechselwirkung zwischen Chinidin und Nifedipin (mit einem verringerten Plasmaspiegel von Chinidin).
Cumarin-Antikoagulanzien
Es gab seltene Berichte über eine verlängerte Prothrombinzeit bei Patienten, die Cumarin-Antikoagulanzien einnahmen und denen PROCARDIA verabreicht wurde. Die Beziehung zur PROCARDIA-Therapie ist jedoch ungewiss.
Cimetidin
Eine Studie mit sechs gesunden Probanden hat einen signifikanten Anstieg der maximalen Nifedipin-Plasmaspiegel (80 %) und der Fläche unter der Kurve (74 %) nach einer einwöchigen Behandlung mit 1000 mg Cimetidin pro Tag und 40 mg Nifedipin pro Tag gezeigt Tag. Ranitidin erzeugte kleinere, nicht signifikante Anstiege. Die Wirkung kann durch die bekannte Hemmung von Cimetidin auf das hepatische Cytochrom P-450 vermittelt werden, das Enzymsystem, das wahrscheinlich für den First-Pass-Metabolismus von Nifedipin verantwortlich ist. Wenn eine Nifedipin-Therapie bei einem Patienten begonnen wird, der derzeit Cimetidin erhält, wird eine vorsichtige Titration empfohlen.
Nifedipin wird durch CYP3A4 metabolisiert. Die gleichzeitige Anwendung von Nifedipin mit Phenytoin, einem Induktor von CYP3A4, senkt die systemische Nifedipin-Exposition um etwa 70 %. Vermeiden Sie die gleichzeitige Anwendung von Nifedipin mit Phenytoin oder anderen bekannten CYP3A4-Induktoren oder erwägen Sie eine alternative antihypertensive Therapie.
CYP3A-Inhibitoren wie Fluconazol, Itraconazol, Clarithromycin, Erythromycin, Nefazodon, Fluoxetin, Saquinavir, Indinavir und Nelfinavir können bei gleichzeitiger Anwendung zu einer erhöhten Nifedipin-Exposition führen. Sorgfältige Überwachung und Dosisanpassung können erforderlich sein; erwägen Sie, Nifedipin mit der niedrigsten verfügbaren Dosis zu beginnen, wenn es gleichzeitig mit diesen Medikamenten gegeben wird.
Andere Interaktionen
Grapefruitsaft
Die gleichzeitige Anwendung von Nifedipin mit Grapefruitsaft führte zu ungefähr einer Verdopplung der AUC und Cmax von Nifedipin ohne Veränderung der Halbwertszeit. Die erhöhten Plasmakonzentrationen resultieren höchstwahrscheinlich aus der Hemmung des CYP 3A4-bezogenen First-Pass-Metabolismus. Vermeiden Sie die Einnahme von Grapefruit und Grapefruitsaft während der Einnahme von Nifedipin.
WARNUNGEN
Übermäßige Hypotonie
Obwohl die blutdrucksenkende Wirkung von PROCARDIA 30 mg bei den meisten Patienten gering ist und gut vertragen wird, kam es gelegentlich bei Patienten zu übermäßiger und schlecht vertragener Hypotonie. Diese Reaktionen traten normalerweise während der anfänglichen Titration oder zum Zeitpunkt der anschließenden Dosiserhöhung auf. Obwohl bei Patienten unter PROCARDIA 30 mg allein selten eine übermäßige Hypotonie auftrat, kann dies häufiger bei Patienten auftreten, die gleichzeitig mit Betablockern behandelt werden. Obwohl für diesen Zweck nicht zugelassen, wurden PROCARDIA und andere Nifedipin-Kapseln mit sofortiger Freisetzung (oral und sublingual) zur akuten Blutdrucksenkung verwendet. Mehrere gut dokumentierte Berichte beschreiben Fälle von schwerer Hypotonie, Myokardinfarkt und Tod, wenn Nifedipin mit sofortiger Freisetzung auf diese Weise verwendet wurde. PROCARDIA Kapseln sollten nicht zur akuten Blutdrucksenkung angewendet werden.
Schwere Hypotonie und/oder erhöhter Flüssigkeitsbedarf wurden bei Patienten berichtet, die PROCARDIA 30 mg zusammen mit einem Betablocker erhielten und sich einer Koronararterien-Bypass-Operation unter Verwendung einer Hochdosis-Fentanyl-Anästhesie unterzogen. Die Wechselwirkung mit hochdosiertem Fentanyl scheint auf die Kombination von PROCARDIA und einem Betablocker zurückzuführen zu sein, aber die Möglichkeit, dass sie mit PROCARDIA 30 mg allein, mit niedrigen Dosen von Fentanyl, bei anderen chirurgischen Eingriffen oder mit anderen narkotischen Analgetika auftreten kann, kann dies nicht sein ausgeschlossen. Bei mit PROCARDIA behandelten Patienten, bei denen eine Operation mit hochdosierter Fentanyl-Anästhesie in Betracht gezogen wird, sollte sich der Arzt dieser potenziellen Probleme bewusst sein und, sofern es der Zustand des Patienten zulässt, ausreichend Zeit (mindestens 36 Stunden) einräumen, damit PROCARDIA 30 mg ausgewaschen werden kann Der Körper vor der Operation.
Erhöhte Angina pectoris und/oder Myokardinfarkt
In seltenen Fällen, insbesondere bei Patienten mit schwerer obstruktiver Koronararterienerkrankung, kam es zu Beginn der Behandlung mit PROCARDIA 30 mg oder zum Zeitpunkt einer Dosiserhöhung zu einer gut dokumentierten erhöhten Häufigkeit, Dauer und/oder Schwere von Angina pectoris oder akutem Myokardinfarkt. Der Mechanismus dieses Effektes ist nicht bestimmt.
Mehrere gut kontrollierte, randomisierte Studien untersuchten die Anwendung von schnell freigesetztem Nifedipin bei Patienten, die gerade einen Myokardinfarkt erlitten hatten. In keiner dieser Studien schien Nifedipin mit sofortiger Wirkstofffreisetzung einen Nutzen zu bringen. In einigen Studien hatten Patienten, die Nifedipin mit sofortiger Freisetzung erhielten, signifikant schlechtere Ergebnisse als Patienten, die Placebo erhielten. PROCARDIA 30 mg Kapseln sollten nicht innerhalb der ersten ein bis zwei Wochen nach einem Myokardinfarkt verabreicht werden, und sie sollten auch bei einem akuten Koronarsyndrom (wenn ein Infarkt unmittelbar bevorsteht) vermieden werden.
Verwendung bei essentieller Hypertonie
PROCARDIA 30 mg und andere Nifedipin-Kapseln mit sofortiger Wirkstofffreisetzung wurden auch zur langfristigen Kontrolle der essentiellen Hypertonie verwendet, obwohl PROCARDIA 30 mg-Kapseln für diesen Zweck nicht zugelassen wurden und keine ordnungsgemäß kontrollierten Studien durchgeführt wurden, um eine angemessene Dosis oder ein geeignetes Dosisintervall festzulegen für eine solche Behandlung. PROCARDIA 30 mg Kapseln sollten nicht zur Kontrolle der essentiellen Hypertonie verwendet werden.
Beta-Blocker-Entzug
Patienten, die kürzlich Betablocker abgesetzt haben, können ein Entzugssyndrom mit verstärkter Angina pectoris entwickeln, wahrscheinlich im Zusammenhang mit einer erhöhten Empfindlichkeit gegenüber Katecholaminen. Der Beginn der Behandlung mit PROCARDIA 30 mg wird dieses Auftreten nicht verhindern und es ist zu erwarten, dass es durch die Auslösung einer reflektorischen Katecholaminfreisetzung verschlimmert wird. Es gab gelegentliche Berichte über verstärkte Angina pectoris in einer Situation, in der ein Betablocker-Entzug und eine Behandlung mit PROCARDIA begonnen wurden. Es ist wichtig, Betablocker möglichst ausschleichen zu lassen, anstatt sie abrupt abzusetzen, bevor Sie mit PROCARDIA beginnen.
Kongestive Herzinsuffizienz
Selten haben Patienten, in der Regel solche, die einen Betablocker erhalten, nach Beginn der Behandlung mit PROCARDIA eine Herzinsuffizienz entwickelt. Bei Patienten mit festsitzender Aortenstenose besteht möglicherweise ein höheres Risiko für ein solches Ereignis, da der entlastende Effekt von PROCARDIA 30 mg für diese Patienten aufgrund ihrer festen Impedanz für den Fluss durch die Aortenklappe erwartungsgemäß von geringerem Nutzen wäre.
VORSICHTSMASSNAHMEN
Allgemein
Hypotonie
Da PROCARDIA den peripheren Gefäßwiderstand senkt, wird eine sorgfältige Überwachung des Blutdrucks während der anfänglichen Verabreichung und Titration von PROCARDIA 30 mg empfohlen. Eine engmaschige Überwachung wird besonders für Patienten empfohlen, die bereits Medikamente einnehmen, die bekanntermaßen den Blutdruck senken. (Sehen WARNUNGEN .)
Periphere Ödeme
Bei etwa einem von zehn mit PROCARDIA (Nifedipin) behandelten Patienten tritt ein leichtes bis mittelschweres peripheres Ödem auf, das typischerweise mit einer arteriellen Vasodilatation einhergeht und nicht auf eine linksventrikuläre Dysfunktion zurückzuführen ist. Dieses Ödem tritt hauptsächlich in den unteren Extremitäten auf und spricht normalerweise auf eine diuretische Therapie an. Bei Patienten, deren Angina pectoris durch dekompensierte Herzinsuffizienz kompliziert wird, sollte darauf geachtet werden, dieses periphere Ödem von den Auswirkungen einer zunehmenden linksventrikulären Dysfunktion zu unterscheiden.
Labortests
Seltene, normalerweise vorübergehende, aber gelegentlich signifikante Erhöhungen von Enzymen wie alkalischer Phosphatase, CPK, LDH, SGOT und SGPT wurden festgestellt. Der Zusammenhang mit der PROCARDIA-Therapie ist in den meisten Fällen ungewiss, in einigen Fällen jedoch wahrscheinlich. Diese Laboranomalien wurden selten mit klinischen Symptomen in Verbindung gebracht; es wurde jedoch über Cholestase mit oder ohne Gelbsucht berichtet. Seltene Fälle von allergischer Hepatitis wurden berichtet.
PROCARDIA 30 mg verringert wie andere Kalziumkanalblocker die Blutplättchenaggregation in vitro. Begrenzte klinische Studien haben bei einigen PROCARDIA-Patienten eine moderate, aber statistisch signifikante Verringerung der Thrombozytenaggregation und eine Verlängerung der Blutungszeit gezeigt. Es wird angenommen, dass dies eine Funktion der Hemmung des Calciumtransports durch die Blutplättchenmembran ist. Für diese Befunde wurde keine klinische Bedeutung nachgewiesen.
Positive direkte Coombs-Tests mit/ohne hämolytischer Anämie wurden berichtet, aber ein kausaler Zusammenhang zwischen der Verabreichung von PROCARDIA und der Positivität dieses Labortests, einschließlich Hämolyse, konnte nicht festgestellt werden.
Obwohl PROCARDIA 30 mg bei Patienten mit Nierenfunktionsstörung sicher angewendet wurde und über eine positive Wirkung berichtet wurde, wurde in bestimmten Fällen bei Patienten mit vorbestehender chronischer Niereninsuffizienz über seltene, reversible Erhöhungen von BUN und Serum-Kreatinin berichtet. Der Zusammenhang mit der PROCARDIA-Therapie ist in den meisten Fällen ungewiss, in einigen Fällen jedoch wahrscheinlich.
Karzinogenese, Mutagenese, Beeinträchtigung der Fruchtbarkeit
Nifedipin wurde zwei Jahre lang oral an Ratten verabreicht und erwies sich nicht als krebserregend. Bei Verabreichung an Ratten vor der Paarung verursachte Nifedipin eine verringerte Fertilität bei einer Dosis, die etwa dem 5-Fachen der maximal empfohlenen Dosis beim Menschen entsprach. Es gibt einen Literaturbericht über eine reversible Verringerung der Fähigkeit menschlicher Spermien, die von einer begrenzten Anzahl unfruchtbarer Männer erhalten wurden, die die empfohlenen Nifedipin-Dosen einnahmen, um in vitro an eine Eizelle zu binden und diese zu befruchten. In-vivo-Mutagenitätsstudien waren negativ.
Schwangerschaft
Es wurde gezeigt, dass Nifedipin bei Ratten und Kaninchen zu teratogenen Befunden führt, einschließlich digitaler Anomalien, die denen ähneln, die für Phenytoin berichtet wurden. Es wurde berichtet, dass digitale Anomalien bei anderen Vertretern der Dihydropyridin-Klasse auftreten und möglicherweise eine Folge eines beeinträchtigten uterinen Blutflusses sind. Die Verabreichung von Nifedipin war mit einer Reihe von embryotoxischen, plazentotoxischen und fetotoxischen Wirkungen verbunden, darunter verkümmerte Föten (Ratten, Mäuse, Kaninchen), Rippendeformitäten (Mäuse), Gaumenspalten (Mäuse), kleine Plazentas und unterentwickelte Chorionzotten (Affen), embryonal und fetale Todesfälle (Ratten, Mäuse, Kaninchen) und verlängerte Trächtigkeit/verringerte neonatale Überlebensrate (Ratten; bei anderen Spezies nicht untersucht). Auf mg/kg-Basis waren alle Dosen, die mit den teratogenen embryotoxischen oder fetotoxischen Wirkungen bei Tieren in Verbindung gebracht wurden, höher (5- bis 50-mal) als die maximal empfohlene Dosis von 120 mg/Tag beim Menschen. Auf mg/m²-Basis waren einige Dosen höher und einige niedriger als die maximal empfohlene Dosis für den Menschen, aber alle lagen in einer Größenordnung davon. Die Dosen, die mit plazentotoxischen Wirkungen bei Affen in Verbindung gebracht wurden, waren gleich oder niedriger als die empfohlene Höchstdosis für den Menschen auf mg/m²-Basis.
Es liegen keine adäquaten und gut kontrollierten Studien bei Schwangeren vor. PROCARDIA sollte während der Schwangerschaft nur angewendet werden, wenn der potentielle Nutzen das potentielle Risiko rechtfertigt.
Stillzeit
Nifedipin wird über die Muttermilch übertragen. PROCARDIA sollte während der Stillzeit nur angewendet werden, wenn der potentielle Nutzen das potentielle Risiko rechtfertigt.
Pädiatrische Verwendung
Sicherheit und Wirksamkeit bei pädiatrischen Patienten wurden nicht nachgewiesen. Die Anwendung bei Kindern und Jugendlichen wird nicht empfohlen.
Geriatrische Verwendung
Das Alter scheint einen signifikanten Einfluss auf die Pharmakokinetik von Nifedipin zu haben. Die Clearance ist verringert, was bei älteren Patienten zu einer höheren AUC führt. Diese Veränderungen sind nicht auf Veränderungen der Nierenfunktion zurückzuführen (vgl KLINISCHE PHARMAKOLOGIE , Pharmakokinetik ).
ÜBERDOSIS
Die Erfahrungen mit einer Nifedipin-Überdosierung sind begrenzt. Im Allgemeinen erfordert eine Überdosierung mit Nifedipin, die zu einer ausgeprägten Hypotonie führt, eine aktive kardiovaskuläre Unterstützung, einschließlich Überwachung der kardiovaskulären und respiratorischen Funktion, Anheben der Extremitäten und umsichtige Anwendung von Kalziuminfusionen, blutdrucksteigernden Mitteln und Flüssigkeiten. Es ist zu erwarten, dass die Clearance von Nifedipin bei Patienten mit eingeschränkter Leberfunktion verlängert ist. Da Nifedipin stark an Proteine gebunden ist, ist eine Dialyse wahrscheinlich nicht von Nutzen; Plasmapherese kann jedoch vorteilhaft sein.
KONTRAINDIKATIONEN
Bekannte Überempfindlichkeitsreaktion auf PROCARDIA.
KLINISCHE PHARMAKOLOGIE
PROCARDIA ist ein Calcium-Ionen-Einstromhemmer (Slow-Channel-Blocker oder Calcium-Ionen-Antagonist) und hemmt den transmembranösen Einstrom von Calcium-Ionen in den Herzmuskel und die glatte Muskulatur. Die kontraktilen Prozesse des Herzmuskels und der glatten Gefäßmuskulatur hängen von der Bewegung extrazellulärer Calciumionen in diese Zellen durch spezifische Ionenkanäle ab. PROCARDIA 30 mg hemmt selektiv den Einstrom von Calciumionen durch die Zellmembran des Herzmuskels und der glatten Gefäßmuskulatur, ohne die Calciumkonzentrationen im Serum zu verändern.
Wirkmechanismus
Die genauen Mittel, mit denen diese Hemmung Angina lindert, wurden noch nicht vollständig bestimmt, umfassen aber mindestens die folgenden zwei Mechanismen:
Entspannung und Vorbeugung von Spasmen der Koronararterien
PROCARDIA dilatiert die Hauptkoronararterien und Koronararteriolen, sowohl in normalen als auch in ischämischen Regionen, und ist ein wirksamer Inhibitor von Koronararterienspasmen, ob spontan oder ergonominduziert. Diese Eigenschaft erhöht die myokardiale Sauerstoffzufuhr bei Patienten mit Koronararterienspasmus und ist verantwortlich für die Wirksamkeit von PROCARDIA 30 mg bei vasospastischer (Prinzmetal- oder Variante) Angina. Ob dieser Effekt bei der klassischen Angina pectoris irgendeine Rolle spielt, ist nicht klar, aber Studien zur Belastungstoleranz haben keinen Anstieg des Produkts aus maximaler Belastungsfrequenz und Druck gezeigt, einem allgemein anerkannten Maß für die Sauerstoffverwertung. Dies deutet darauf hin, dass im Allgemeinen die Linderung von Spasmen oder Dilatation von Koronararterien kein wichtiger Faktor bei klassischer Angina ist.
Reduzierung der Sauerstoffnutzung
PROCARDIA reduziert regelmäßig den arteriellen Druck in Ruhe und bei einem bestimmten Belastungsniveau, indem es die peripheren Arteriolen erweitert und den gesamten peripheren Widerstand (Nachlast), gegen den das Herz arbeitet, verringert. Diese Entlastung des Herzens reduziert den myokardialen Energieverbrauch und den Sauerstoffbedarf und erklärt wahrscheinlich die Wirksamkeit von PROCARDIA bei chronisch stabiler Angina.
Pharmakokinetik und Stoffwechsel
PROCARDIA wird nach oraler Verabreichung schnell und vollständig resorbiert. Das Medikament ist 10 Minuten nach der oralen Verabreichung im Serum nachweisbar, und Spitzenwerte im Blut treten nach etwa 30 Minuten auf. Die Bioverfügbarkeit ist proportional zur Dosis von 10 bis 30 mg; Die Halbwertszeit ändert sich nicht signifikant mit der Dosis. Es gibt kaum einen Unterschied in der relativen Bioverfügbarkeit, wenn PROCARDIA-Kapseln oral verabreicht und entweder ganz geschluckt, gebissen und geschluckt oder gebissen und sublingual gehalten werden. Das Durchbeißen der Kapsel vor dem Schlucken führt jedoch zu etwas früheren Plasmakonzentrationen (27 ng/ml 10 Minuten nach 10 mg), als wenn die Kapseln intakt geschluckt werden. PROCARDIA 30 mg wird stark an Serumproteine gebunden. PROCARDIA wird weitgehend in inaktive Metaboliten umgewandelt und ungefähr 80 Prozent von PROCARDIA 30 mg und Metaboliten werden über die Nieren ausgeschieden. Die Eliminationshalbwertszeit von Nifedipin beträgt etwa zwei Stunden. Da die hepatische Biotransformation der vorherrschende Weg für die Disposition von Nifedipin ist, kann die Pharmakokinetik bei Patienten mit chronischer Lebererkrankung verändert sein. Patienten mit eingeschränkter Leberfunktion (Leberzirrhose) haben eine längere Dispositionshalbwertszeit und eine höhere Bioverfügbarkeit von Nifedipin als gesunde Probanden. Der Grad der Serumproteinbindung von Nifedipin ist hoch (92–98 %). Die Proteinbindung kann bei Patienten mit eingeschränkter Nieren- oder Leberfunktion stark reduziert sein.
Nach intravenöser Verabreichung war die Clearance von Nifedipin bei älteren gesunden Probanden im Vergleich zu jungen gesunden Probanden um 33 % verringert.
Hämodynamik
Wie andere Slow-Channel-Blocker übt PROCARDIA eine negativ inotrope Wirkung auf isoliertes Myokardgewebe aus. Dies wird selten, wenn überhaupt, bei intakten Tieren oder Menschen beobachtet, wahrscheinlich aufgrund von Reflexreaktionen auf seine gefäßerweiternden Wirkungen. Beim Menschen verursacht PROCARDIA 30 mg eine Verringerung des peripheren Gefäßwiderstands und einen Abfall des systolischen und diastolischen Drucks, der normalerweise gering ist (5-10 mm Hg systolisch), aber manchmal größer ist. Es gibt normalerweise einen kleinen Anstieg der Herzfrequenz, eine Reflexantwort auf die Vasodilatation. Messungen der Herzfunktion bei Patienten mit normaler Ventrikelfunktion haben im Allgemeinen einen kleinen Anstieg des Herzindex ohne größere Auswirkungen auf die Ejektionsfraktion, den linksventrikulären enddiastolischen Druck (LVEDP) oder das Volumen (LVEDV) festgestellt. Bei Patienten mit eingeschränkter Ventrikelfunktion haben die meisten akuten Studien eine gewisse Erhöhung der Ejektionsfraktion und eine Verringerung des linksventrikulären Füllungsdrucks gezeigt.
Elektrophysiologische Wirkungen
Obwohl PROCARDIA wie andere Mitglieder seiner Klasse die Sinusknotenfunktion und die atrioventrikuläre Erregungsleitung in isolierten myokardialen Präparaten verringert, wurden solche Wirkungen in Studien an intakten Tieren oder Menschen nicht beobachtet. In formellen elektrophysiologischen Studien, vorwiegend bei Patienten mit normaler Erregungsleitung, zeigte PROCARDIA 30 mg keine Tendenz, die atrioventrikuläre Erregungsleitung zu verlängern, die Erholungszeit der Sinusknoten zu verlängern oder die Sinusfrequenz zu verlangsamen.
INFORMATIONEN ZUM PATIENTEN
Keine Informationen bereitgestellt. Bitte wende dich an die WARNUNGEN und VORSICHTSMASSNAHMEN Abschnitte.